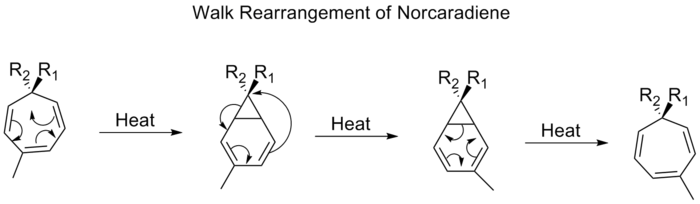
Reakcja sigmatropowa w chemii organicznej jest reakcją perykliczną. Reakcja sigmatropowa nie wykorzystuje katalizatora i obejmuje pojedynczą molekułę (niekatalizowany proces wewnątrzcząsteczkowy). Zmienia ona jedno wiązanie σ w inne wiązanie σ. Nazwa sigmatropowa jest wynikiem połączenia długoletniej nazwy "sigma" dla pojedynczych wiązań węgiel-węgiel i greckiego słowa tropos, oznaczającego zwrot. Jest to reakcja przegrupowania, która oznacza, że wiązania w cząsteczce przesuwają się między atomami bez pozostawienia jakichkolwiek atomów lub dodania do cząsteczki nowych atomów. W reakcji sigmatroptycznej podstawnik przemieszcza się z jednej części układu wiązań π do innej części w reakcji wewnątrzcząsteczkowej z jednoczesną rearanżacją układu π. Prawdziwe reakcje sigmatropowe zazwyczaj nie wymagają katalizatora. Niektóre reakcje sigmatropowe są katalizowane przez kwas Lewisa. W reakcjach sigmatropowych często występują katalizatory przejściowo-metalowe, które tworzą półprodukty w analogicznych reakcjach. Najbardziej znane z sigmatropowych przemian to [3,3] przemianę Cope'a, przemianę Claisena, przemianę Carrolla i syntezę indolową Fischera.
Co to jest reakcja sigmatropowa — podsumowanie mechanizmu
W najprostszym ujęciu reakcja sigmatropowa to przemieszczanie się wiązania σ w obrębie układu wysyconego i sprzężonego układu π w jednej cząsteczce, zachodzące zwykle w sposób koncertowany (bez pośrednich, izolowalnych karbokationów czy karboanionów). Przejście przebiega przez cykliczny stan przejściowy, w którym orbitali π i σ reorganizują się jednocześnie. Przebieg i dozwolenia reakcji kontrolowane są przez zasady zachowania symetrii orbitali (reguły Woodwarda–Hoffmanna), które decydują, czy dana przemiana może zajść w sposób suprafacjalny lub antarafacjalny i czy wymaga ogrzewania lub świecenia światłem.
Oznaczanie typu: zapis [i,j]
Reakcje sigmatropowe klasyfikuje się za pomocą zapisu [i,j], gdzie liczby i i j określają odległości, o które przemieszczane jest wiązanie σ względem dwóch końców sprzężonego układu π. Przykłady:
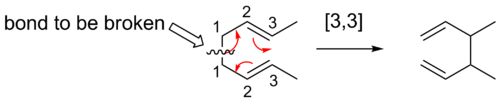
- [3,3] – typowy dla przemiany Cope'a i Claisena;
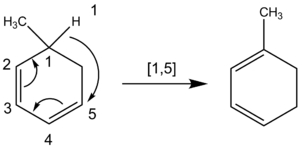
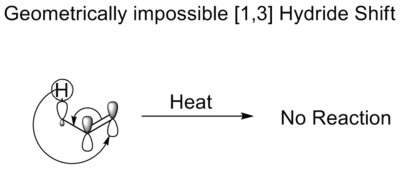
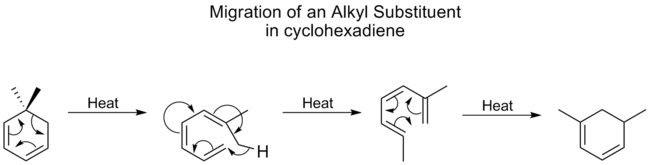
- [1,5] – często spotykane dla przesunięć atomów wodoru (1,5-hydrogen shift);
- [2,3], [3,2] i inne – występują w specyficznych układach i często mają różne efekty stereochemiczne.
Suprafacjalne i antarafacjalne przesunięcie
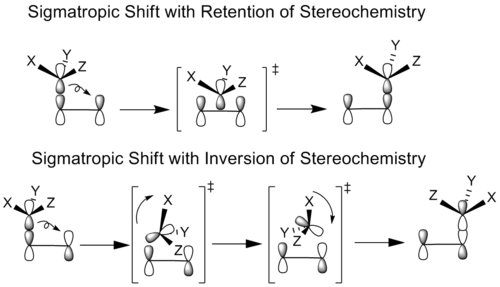
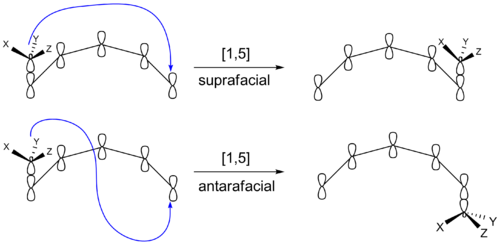
W przesunięciu suprafacjalnym migracja odbywa się po tej samej stronie układu π (konserwacja fazy orbitali bez zmiany strony), natomiast w przesunięciu antarafacjalnym migracja zachodzi z przeciwnej strony. W praktyce suprafacjalne procesy są łatwiejsze do zaistnienia w typowych cząsteczkach organicznych ze względu na ograniczenia geometryczne; antarafacjalne wymagają często elastycznych łańcuchów lub specjalnych topologii cząsteczek.
Przykłady reakcji
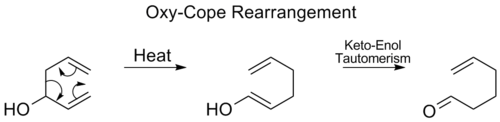
- Przemiana Cope'a ([3,3]) — klasyczna reakcja 1,5-dienów: 1,5-dien ulega przemianie przez sześcioczłonowy cykliczny stan przejściowy do izomeru. Przykładowo, układy 1,5-hexadienowe mogą izomeryzować do forma bardziej stabilnej energetycznie (reakcja często jest odwracalna, tzw. równowaga Cope'a). Wariantem jest oxy-Cope, gdzie obecność grupy hydroksylowej i jej deprotonacja (anion) znacząco przyspiesza przebieg i prowadzi do produktów enolowych lub karbonylowych.
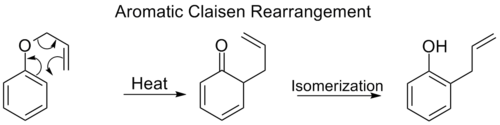
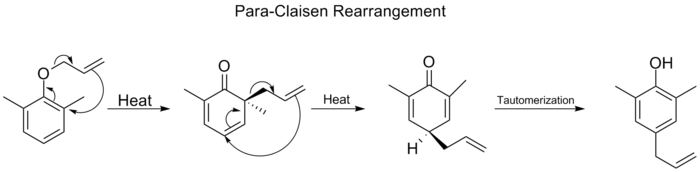
- Przemiana Claisena ([3,3]) — przemiana allylowych eterów winylowych (allyl vinyl ethers) do związków o nowym wiązaniu C–C, często prowadząca do γ,δ-nienasyconych aldehydów lub ketonów po dalszych przekształceniach. Mechanizm to także sześcioczłonowy, concertedny stan przejściowy; geometryczne ułożenie w stanie przejściowym (krzesłowy kontra łodziowy) wpływa na stereochemię produktu. Istnieją też warianty (Ireland–Claisen, Johnson–Claisen) wykorzystujące pochodne, aniony czy estry, które zwiększają kontrolę stereochemiczną i wydajność.
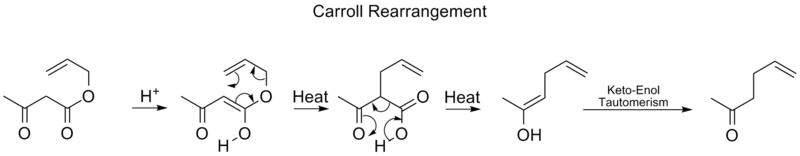
- Przemiana Carrolla — inna sigmatropowa przemiana wykorzystywana w syntezach C–C, często w kontekście przeniesienia allylowego.
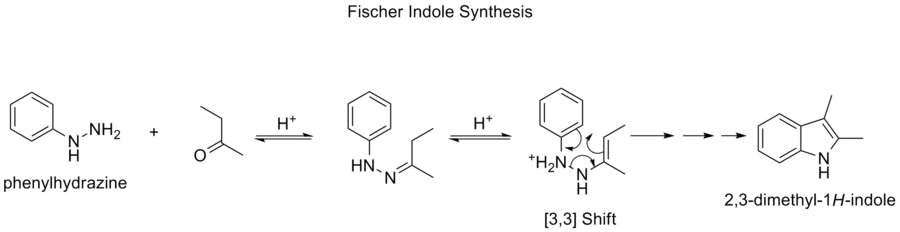
- Synteza indolowa Fischera — w przebiegu tej syntezy występują etapy perykliczne i sigmatropowe prowadzące do sformalizowanego przeorganizowania układu i budowy pierścienia indolowego.
Warunki i kataliza
Większość sigmatropowych przemian przebiega termicznie (wymaga podgrzania), jako że następuje przez stosunkowo wysokoenergetyczny stan przejściowy. Jednak:
- kataliza kwasami Lewisa może obniżać barierę aktywacji i zmieniać tor reakcji, co bywa wykorzystywane do zwiększenia szybkości lub kontroli stereochemii;
- katalizatory metaliczne (przejściowych metali) mogą prowadzić do analogicznych, lecz często stopniowych (stepwise) dróg reakcji, tworząc kompleksy pośrednie;
- warianty anionowe (np. oxy-Cope po deprotonacji) znacząco przyspieszają i zmieniają termodynamikę procesów.
Stereochemia i selektywność
Stereochemia produktów sigmatropowych zależy od konformacji i typu stanu przejściowego. Dla przemian [3,3] często można przewidzieć wynik stereochemiczny przy założeniu, że proces przebiega przez chair-podobny sześcioczłonowy stan przejściowy — konfiguracja podstawników w stanie przejściowym determinuje relacje cis/trans w produkcie. W praktyce kontrola stereochemii osiągana jest poprzez dobór substratów, grup ochronnych, katalizatorów oraz warunków reakcji.
Zastosowania w syntezie
Reakcje sigmatropowe są cennym narzędziem w syntezie organicznej, pozwalającym na:
- przenoszenie grup w obrębie cząsteczki bez konieczności używania zewnętrznych reagentów,
- tworzenie nowych wiązań C–C w kontrolowany sposób,
- budowę skomplikowanych układów cyklicznych i stereocentów, co jest szczególnie przydatne przy syntezie naturalnych produktów i leków.
Uwagi praktyczne
- Wiele sigmatropowych przemian jest odwracalnych — aby przesunąć równowagę na stronę produktu, projektuje się substraty tak, by produkt był termodynamicznie stabilniejszy (np. przez aromatyzację, koniugację z grupami elektrodonorowymi/elektroacceptorowymi).
- Monitorowanie przebiegu reakcji zwykle odbywa się za pomocą NMR i GC/MS; w przypadku reakcji o wysokiej bariery aktywacji stosuje się podwyższoną temperaturę lub katalizę.
- W projektowaniu syntez warto uwzględnić ograniczenia geometryczne — nie wszystkie [i,j] są łatwo osiągalne w suprafacjalnym trybie ze względu na topologię cząsteczki.
Podsumowując, reakcje sigmatropowe to klasa peryklicznych przemian wewnątrzcząsteczkowych o dużym znaczeniu w syntezie organicznej. Ich zrozumienie — zarówno reguł symetrii orbitalnej, jak i wpływu konformacji — jest kluczowe do efektywnego wykorzystania ich w konstrukcji złożonych cząsteczek.

![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)


![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)