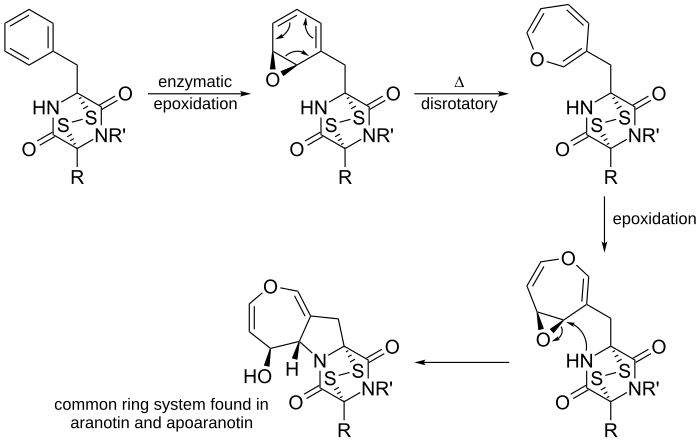
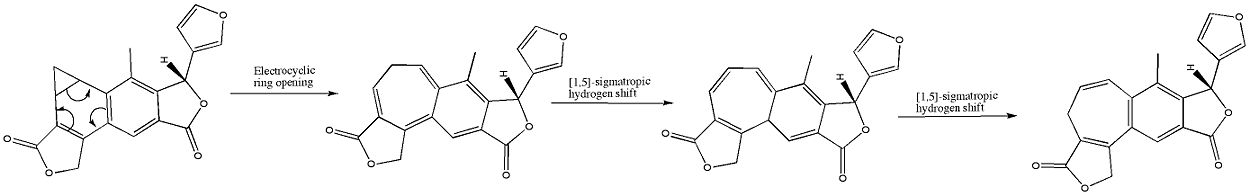
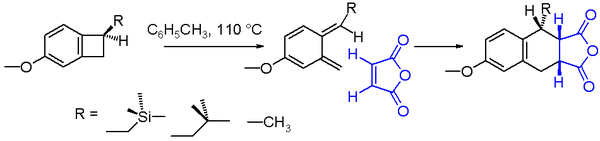
W chemii organicznej reakcja elektrocykliczna jest szczególnym rodzajem peryklicznej reakcji przegrupowania. Reakcja jest elektrocykliczna, gdy w jej wyniku jedno wiązanie pi ulega przemianie w wiązanie sigma (zamknięcie pierścienia, elektrocyklizacja) lub gdy jedno wiązanie sigma ulega przekształceniu w wiązanie pi (otwieranie pierścienia). Reakcje te przebiegają przez zorganizowane, cykliczne przejście orbitalne i wykazują kilka charakterystycznych cech:
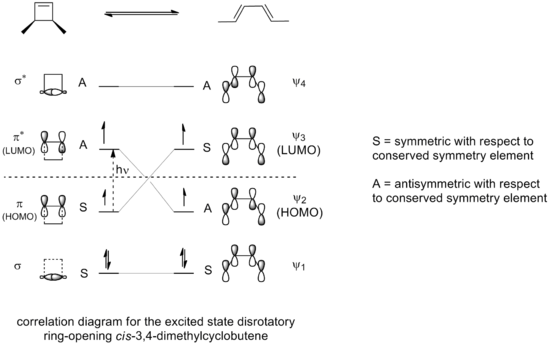
- reakcje elektrocykliczne mogą być napędzane przez światło (fotoindukowane) lub przez ciepło (termiczne) — w zależności od sposobu wzbudzenia elektrony zajmują inne orbitale;
- tryb reakcji (czyli czy przebiega konrotacyjnie czy dysrotacyjnie) jest określony liczbą elektronów π w układzie koniugowanym — stąd zależność od reguł symetrii orbitalnej;
- reakcja elektrocykliczna może zamknąć pierścień (elektrocyklizacja) lub otworzyć pierścień (np. otwarcie cyklobutenu do dienu);
- stereospecyficzność produktu jest określana przez sposób tworzenia się przejściowego — konrotacyjny lub dysrotacyjny — zgodnie z zasadami Woodward–Hoffmanna.
Podstawy teoretyczne: reguły Woodwarda–Hoffmanna i orbitale brzegowe
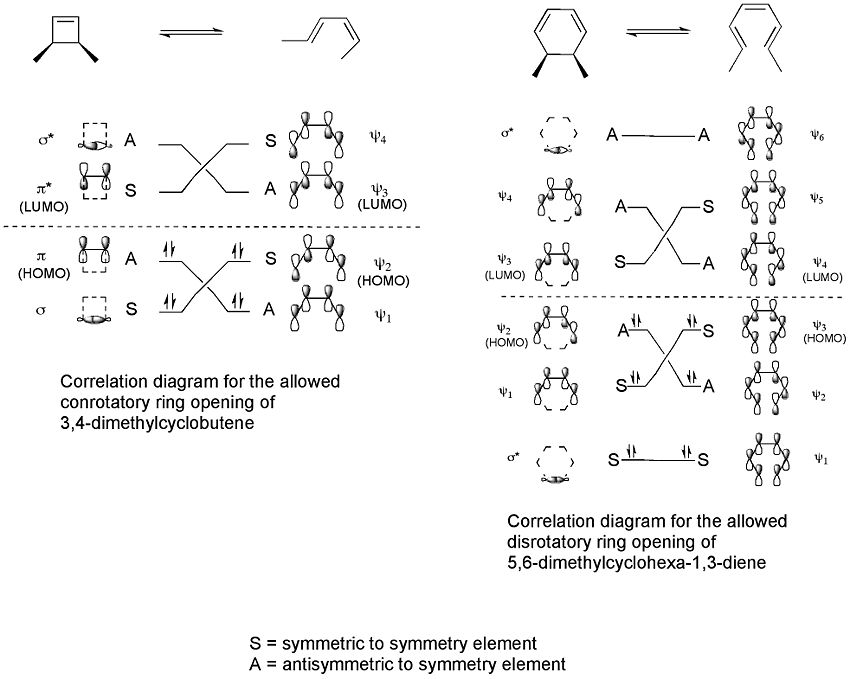
Kluczowym pojęciem wyjaśniającym wybór mechanizmu jest konserwacja symetrii orbitalnej. Zasady Woodwarda–Hoffmanna przewidują, które elektrocyklizacje są dozwolone (tj. przebiegają łatwo) w warunkach termicznych, a które są dozwolone w warunkach fotochemicznych. W praktyce stosuje się prostą regułę elektryczną opartą na liczbie elektronów π:
- Systemy 4n+2 elektronów π (np. 2π, 6π): termicznie preferują przebieg dysrotacyjny, fotochemicznie — konrotacyjny.
- Systemy 4n elektronów π (np. 4π, 8π): termicznie preferują przebieg konrotacyjny, fotochemicznie — dysrotacyjny.
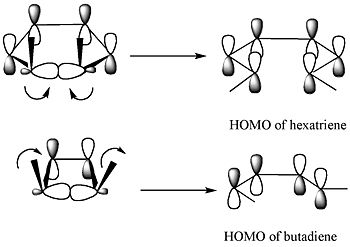
Wyjaśnienie orbitalne (metoda frontier-orbital) polega na porównaniu symetrii najwyżej obsadzonego orbitalu molekularnego (HOMO) reaktanta z symetrią orbitali produktu. Podczas rozrywania wiązania sigma i tworzenia pary orbitali π nowo powstałe p-orbitaly muszą być kompatybilne symetrycznie z HOMO produktu, aby przebieg był sprzyjany energetycznie.
Konrotacja i dysrotacja — co to oznacza stereochemicznie?
W elektrocyklizacji opisujemy dwa typy ruchu końców łańcucha prowadzącego do zamknięcia pierścienia:
- konrotacja (conrotatory) — oba końce łańcucha obracają się w tym samym kierunku (np. oba w prawo lub oba w lewo);
- dysrotacja (disrotatory) — końce łańcucha obracają się w przeciwnych kierunkach.
Ten wybór rotacji determinuje końcową konfigurację podstawników przy nowo powstałym wiązaniu sigma — od tego zależy, czy otrzymamy izomery cis/trans lub pary enancjomeryczne.
Torquoselektywność (momentoselektywność)
Momentoselektywność (z ang. torquoselectivity, czasem tłumaczona jako selektywność skrętu) odnosi się do kierunku, w którym obracają się podstawniki podczas procesu konrotacji lub dysrotacji. Nawet jeśli mechanizm dopuszcza obrót w obu kierunkach, efekty elektronowe i steryczne podstawników mogą ograniczać preferowany kierunek obrotu i prowadzić do przewagi jednego stereoisomeru nad drugim. Przy pełnej selektywności otrzymujemy niemal wyłącznie jeden stereoizomer; przy częściowej — mieszaninę z przewagą jednego z nich.
Przykłady i ilustracje
Klasycznym przykładem jest termiczne otwarcie pierścienia 3,4-dimetylocyklobutenu. Izomer cis daje wyłącznie cis,trans-2,4-heksadien, podczas gdy izomer trans prowadzi do trans,trans-2,4-heksadien. Ten stereospecyficzny wynik wynika z mechanizmu otwarcia pierścienia (konrotacyjnego lub dysrotacyjnego) i zgodności z symetrią orbitalną:
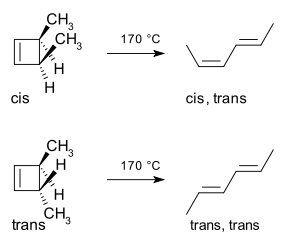
Metoda orbitali brzegowych wyjaśnia szczegóły: wiązanie sigma w reagencie otwiera się tak, że powstałe p-orbity mają tę samą symetrię co HOMO produktu (butadien). W omawianym przypadku otwarcie pierścienia zachodzi w sposób rotacyjny, który daje odpowiednie znaki fazowe orbitali po obu stronach przerwanej wiązki, co jest zgodne z formacją dozwolonego produktu:
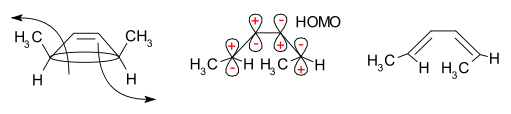
Nazarowska cyklizacja — specjalny przypadek
Nazarowska reakcja cyklizacyjna to przykład elektrocyklizacji zamykającej pierścień. Nazarow (Iwan N. Nazarow) odkrył, że diwinyloketony mogą ulegać elektrocyklizacji prowadzącej do cyklopentenonów — proces wykorzystywany często w syntezie złożonych systemów cyklicznych. Mechanizm typowo przebiega przez uwodornienie i powstanie karbokationu, który następnie zamyka się do cyklopentenonu; reakcja ta ma wielkie znaczenie w syntezach naturalnych i przemysłowych.
Inne przykłady i zastosowania
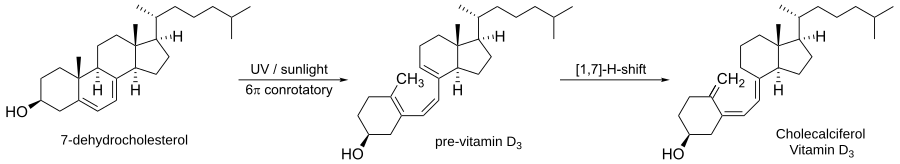
- 6π-elektrocyklizacja all-triene do cykloheksadienu — istotna w tworzeniu sześcioczłonowych układów aromatycznych i bicyklicznych struktur;
- fotochemiczne elektrocyklizacje stosowane do tworzenia cyklicznych struktur w syntezach asymetrycznych;
- wykorzystanie torquoselektywności i kataliz chemicznych do uzyskiwania wysokiej selektywności enancjomerycznej.
Stereospecyficzność, dowody eksperymentalne i praktyczne uwagi
Chemicy interesują się reakcjami elektrocyklicznymi, ponieważ ich stereochemia i mechanika potwierdzają przewidywania teoretyczne dotyczące zachowania symetrii orbitali molekularnych oraz zasad Woodwarda–Hoffmanna. Doświadczenia z izomerami geometrycznymi, badania kinetyczne oraz spektroskopia (np. NMR) pozwalają śledzić, czy reakcja przebiega konrotacyjnie czy dysrotacyjnie i jakimi produktami kończy się proces. W praktyce wpływ na wynik mają temperatura, światło, podstawnikowanie substratów oraz obecność katalizatorów lub czynników jonizujących.
Podsumowanie
Reakcje elektrocykliczne to ważna klasa reakcji pericyklicznych, łącząca wymiar teoretyczny (symetria orbitali, reguły Woodwarda–Hoffmanna) z praktyką syntez organicznych. Znajomość zasad konrotacji/dysrotacji, zależności od liczby elektronów π oraz efektów sterycznych i elektronowych podstawników pozwala przewidywać i kontrolować stereochemię otrzymywanych produktów.