Elektrony mają najmniejszy ładunek elektryczny. Ten ładunek elektryczny jest równy ładunkowi protonu, ale ma przeciwny znak. Z tego powodu elektrony są przyciągane przez protony jąder atomowych i zazwyczaj tworzą atomy. Masa elektronu jest około 1/1836 masy protonu.
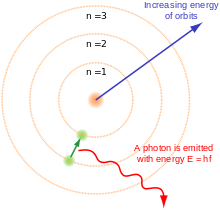
Jednym ze sposobów myślenia o położeniu elektronów w atomie jest wyobrażenie sobie, że orbitują one w stałych odległościach od jądra. W ten sposób elektrony w atomie istnieją w pewnej liczbie powłok elektronowych otaczających centralne jądro. Każdej powłoce elektronowej przypisany jest numer 1, 2, 3, i tak dalej, poczynając od tej, która znajduje się najbliżej jądra (powłoka najbardziej wewnętrzna). Każda powłoka może pomieścić pewną maksymalną liczbę elektronów. Rozmieszczenie elektronów w różnych powłokach nazywane jest układem elektronowym (lub formą lub kształtem elektronowym). Układ elektronowy może być przedstawiony za pomocą numeracji lub diagramu elektronowego. (Innym sposobem myślenia o rozmieszczeniu elektronów jest użycie mechaniki kwantowej do obliczenia ich orbitali atomowych).
Elektron jest jedną z rodzajów cząstek subatomowych zwanych leptonami. Elektron ma ujemny ładunek elektryczny. Elektron ma jeszcze jedną właściwość, zwaną spinem. Jego wartość spinu wynosi 1/2, co czyni go fermionem.
Podczas gdy większość elektronów znajduje się w atomach, inne poruszają się niezależnie w materii, lub razem jako promienie katodowe w próżni. W niektórych nadprzewodnikach elektrony poruszają się parami. Kiedy elektrony przepływają, przepływ ten nazywamy elektrycznością lub prądem elektrycznym.
Obiekt może być opisany jako "ujemnie naładowany", jeśli jest w nim więcej elektronów niż protonów, lub "dodatnio naładowany", jeśli jest w nim więcej protonów niż elektronów. Elektrony mogą przemieszczać się z jednego obiektu do drugiego, gdy są dotykane. Mogą być przyciągane do innego obiektu o przeciwnym ładunku lub odpychane, gdy oba obiekty mają ten sam ładunek. Kiedy obiekt jest "uziemiony", elektrony z naładowanego obiektu przechodzą do ziemi, czyniąc obiekt neutralnym. To właśnie robią piorunochrony (przewody odgromowe).
Reakcje chemiczne
Elektrony w swoich powłokach wokół atomu są podstawą reakcji chemicznych. Kompletne powłoki zewnętrzne, z maksymalną liczbą elektronów, są mniej reaktywne. Zewnętrzne powłoki z mniejszą ilością elektronów niż maksymalna są reaktywne. Liczba elektronów w atomach jest podstawą chemicznego układu okresowego.
Pomiar
Ładunek elektryczny może być bezpośrednio mierzony za pomocą urządzenia zwanego elektrometrem. Prąd elektryczny może być bezpośrednio mierzony za pomocą galwanometru. Pomiar dokonywany galwanometrem różni się od pomiaru dokonywanego elektrometrem. Obecnie przyrządy laboratoryjne są w stanie zawierać i obserwować pojedyncze elektrony.
Widzenie" elektronu
W warunkach laboratoryjnych oddziaływania pojedynczych elektronów mogą być obserwowane za pomocą detektorów cząstek, które pozwalają na pomiar specyficznych własności, takich jak energia, spin i ładunek. W jednym przypadku użyto pułapki Penninga, w której przez 10 miesięcy znajdował się pojedynczy elektron. Moment magnetyczny elektronu został zmierzony z dokładnością do jedenastu cyfr, co w 1980 roku było dokładnością większą niż dla jakiejkolwiek innej stałej fizycznej.
Pierwsze obrazy wideo rozkładu energii elektronu zostały uchwycone przez zespół z Uniwersytetu w Lund w Szwecji w lutym 2008 roku. Naukowcy użyli niezwykle krótkich błysków światła, zwanych impulsami attosekundowymi, które pozwoliły po raz pierwszy zaobserwować ruch elektronu. Rozmieszczenie elektronów w materiałach stałych może być również wizualizowane.
Antycząstki
Antycząstka elektronu nazywana jest pozytonem. Jest on identyczny z elektronem, ale przenosi ładunki elektryczne i inne o przeciwnym znaku. Kiedy elektron zderza się z pozytonem, mogą one rozpraszać się wzajemnie lub ulec całkowitej anihilacji, wytwarzając parę (lub więcej) fotonów promieniowania gamma.