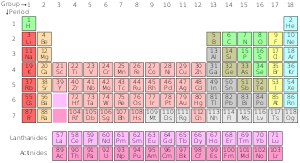
Układ okresowy pierwiastków chemicznych jest uporządkowanym wykazem znanych pierwiastków chemicznych. W tabeli pierwiastki umieszczone są w kolejności ich liczb atomowych, zaczynając od najmniejszej (1 — wodór). Liczba atomowa pierwiastka odpowiada liczbie protonów w jego jądrze atomu i jednoznacznie identyfikuje dany pierwiastek. W układzie okresowym pierwiastki są ułożone w okresy i grupy. Rząd pierwiastków w poprzek tabeli nazywamy okresem. Każdy okres ma numer od 1 do 7. Okres 1 zawiera tylko 2 pierwiastki: wodór i hel. Okresy 2 i 3 mają po 8 pierwiastków, okresy 4 i 5 po 18, a okresy 6 i 7 po 32 (wliczając bloki f — lantanoidy i aktynoidy). Pierwiastki w danym okresie mają kolejne liczby atomowe i stopniowo zmieniają się ich właściwości fizyczne i chemiczne wraz ze wzrostem liczby atomowej.
Grupy i ich znaczenie
Kolumna pierwiastków biegnąca w dół tabeli nazywana jest grupą. W standardowej tablicy okresowej jest 18 grup; każda ma numer od 1 do 18. Pierwiastki należące do tej samej grupy mają podobne konfiguracje elektronów zewnętrznych i zbliżoną liczbę elektronów walencyjnych, co przekłada się na podobne właściwości chemiczne. Przykłady istotnych grup:
- Grupa 1 — metale alkaliczne (np. cez), bardzo reaktywne metalicznie;
- Grupa 2 — metale ziem alkalicznych;
- Grupa 17 — halogeny, silnie reaktywne niemetale;
- Grupa 18 — gazy szlachetne (np. hel), charakteryzujące się niską reaktywnością; niektóre z nich (zwłaszcza cięższe jak ksenon) mogą jednak tworzyć związki.
Systemy numeracji grup
Istniały różne systemy numeracji grup. Jeden używał cyfr rzymskich, inne arabskich. W 1990 roku Międzynarodowa Unia Chemii Czystej i Stosowanej (IUPAC) przyjęła system arabskich numerów (1–18), aby ujednolicić oznaczenia stosowane przez naukowców na świecie.
Podział na metale, niemetale i metaloidy
W układzie okresowym wyróżnia się trzy główne kategorie pierwiastków: metale, metaloidy i niemetale. Ogólne tendencje są następujące:
- Elementy po lewej stronie i w dolnej części tablicy są zazwyczaj najbardziej metaliczne (łatwo oddają elektrony) — np. cez.
- Elementy po prawej górze są najmniej metaliczne (mają tendencję do przyjmowania elektronów) — np. hel jako gaz szlachetny; inne niemetale to tlen, fluor czy azot.
- Między metalami a niemetalami leżą metaloidy, które wykazują mieszane właściwości.
Trendy okresowe i właściwości
Układ okresowy służy chemikom do obserwowania wzorców i zależności między pierwiastkami. Do najważniejszych trendów należą:
- Promień atomowy: generalnie rośnie w dół grupy i maleje wzdłuż okresu z lewej do prawej;
- Energia jonizacji: czyli energia potrzebna do usunięcia elektronu, zwykle rośnie w okresie z lewej na prawo i maleje w dół grupy;
- Elektroujemność: wzrasta w okresie z lewej na prawo i maleje w dół grupy (skala Paulinga opisuje tę wielkość);
- Stopnie utlenienia i typowe związki: pierwiastki z tej samej grupy często tworzą podobne typy jonów i związków;
- Bloki elektronowe (s, p, d, f) odzwierciedlają, które orbitale są zapełniane i wpływają na chemiczne zachowanie pierwiastków.
Bloki układu okresowego
W układzie okresowym wyróżnia się bloki związane z typem zapełnianych orbitali:
- Blok s — grupy 1–2 (metale alkaliczne i ziem alkalicznych) oraz wodór i hel;
- Blok p — grupy 13–18 (zawiera wiele niemetali i metali lekkich);
- Blok d — przejściowe metale (grupy 3–12);
- Blok f — lantanoidy i aktynoidy, zwykle umieszczane pod główną tabelą.
Historia i wkład Mendelejewa
Układ okresowy został ukształtowany i spopularyzowany przez rosyjskiego chemika Dymitra IwanowiczaMendelejewa (1834-1907). Mendelejew ułożył pierwiastki według mas atomowych i przewidywał istnienie oraz właściwości jeszcze nieodkrytych pierwiastków, co później potwierdziły odkrycia. Na jego cześć nazwano pierwiastek o liczbie atomowej 101 — mendelewium.
Układ okresowy nadal ewoluuje: co pewien czas potwierdzane są nowe pierwiastki syntetyczne (szczególnie w ciężkich liczbach atomowych), a badania nad własnościami i zastosowaniami pierwiastków stale poszerzają naszą wiedzę. Dzięki tabeli okresowej naukowcy potrafią przewidywać reakcje chemiczne, projektować nowe związki i materiały oraz zrozumieć zależności między strukturą atomową a właściwościami makroskopowymi.