Gazy szlachetne to grupa pierwiastków chemicznych znajdujących się w grupie 18 układu okresowego. Przy standardowych warunkach wszystkie występują jako atomy pojedyncze (są monoatomowe), dlatego w stanie gazowym ich „cząsteczka” składa się z jednego atomu. Charakteryzują się niewielką reaktywnością — zwykle nie łączą się z innymi pierwiastkami — ponieważ mają trwałą konfigurację elektronową powłoki zewnętrznej (dla helu jest to pełna powłoka dwuelektronowa, dla pozostałych często nazywana „oktetem”). Do grupy tej należą sześć pierwiastków:
Występowanie i pozyskiwanie
Gazy szlachetne występują w powietrzu w śladowych ilościach: najobficiej obecny jest argon (około 0,93% objętości powietrza), podczas gdy pozostałe — neon, hel, krypton, xenon — występują w dużo mniejszych stężeniach; radon pojawia się jedynie lokalnie, jako produkt rozpadów promieniotwórczych. Suma zawartości gazów szlachetnych w atmosferze wynosi około 0,96%.
Większość gazów szlachetnych (neon, argon, krypton, xenon) pozyskuje się przez frakcjonowaną destylację skroplonego powietrza. Hel jest najczęściej odzyskiwany z gazu ziemnego (z złóż bogatych w helium), natomiast radon powstaje miejscowo w skałach i glebie na skutek rozpadów promieniotwórczych.
Właściwości fizyczne i chemiczne
Podstawowe cechy gazów szlachetnych:
- monoatomowość i gazowy stan skupienia w warunkach normalnych;
- bardzo niskie temperatury topnienia i wrzenia, które wzrastają w dół grupy (hel ma najniższą temperaturę wrzenia, a radon najwyższą spośród naturalnych gazów szlachetnych);
- małe wartości powinowactwa elektronowego, wysokie energie jonizacji — stąd niska reaktywność;
- przy wzroście liczby atomowej rośnie gęstość i polarowalność atomów, co wpływa na ich właściwości fizyczne i możliwość tworzenia delikatnych oddziaływań Van der Waalsa;
- pomimo ogólnej „obojętności” istnieją znane związki gazów szlachetnych (zwłaszcza xenonu i do pewnego stopnia kryptonu oraz argonu w specjalnych warunkach); hel praktycznie nie tworzy stabilnych związków chemicznych.
Kolory w lampach wyładowczych
W lampach wyładowczych (np. tzw. zimnych lampach katodowych) każdy gaz daje charakterystyczne barwy światła:
· 
Hel
· 
Neon
· 
Argon
· 
Krypton
· 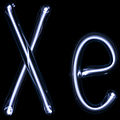
Xenon
Ununoctium (pierwiastek 118) jest prawdopodobnie następnym elementem w tej samej grupie, chociaż obecna oficjalna nazwa to oganesson (Og). Jego najbardziej stabilne izotopy mają ekstremalnie krótkie czasy życia (często mniejsze niż milisekunda), np. podawane 0,89 ms dla jednego z izotopów; po chwili ulega rozpadowi na inne pierwiastki (w opisach pojawia się m.in. rozpad do Ununhexium (pierwiastek 116)). Ogranicza to możliwość badania i praktycznego wykorzystania tego pierwiastka, a także sprawia, że jego właściwości mogą różnić się od przewidywań ze względu na silne efekty relatywistyczne.
Związki chemiczne
Pomimo nazwy „szlachetne” kilka z tych pierwiastków tworzy znane związki:
- Xenon tworzy fluorki (np. XeF2, XeF4, XeF6), tlenki (np. XeO3, XeO4) oraz związki z innymi niemetalami — to najbardziej „reaktywny” przedstawiciel grupy w normalnych warunkach laboratoryjnych;
- Krypton może tworzyć m.in. KrF2;
- Argon w bardzo niskich temperaturach i specjalnych warunkach utworzono związki typu HArF (zarejestrowany w matrycy niskotemperaturowej);
- Hel nie tworzy stabilnych związków w normalnych warunkach, lecz może tworzyć egzotyczne utlenki i związki w ekstremalnych eksperymentach teoretycznych/obserwacyjnych;
- Radon tworzy związki chemiczne, ale jego zastosowanie jest ograniczone przez radioaktywność i związane z nią zagrożenia zdrowotne.
Zastosowania
- Hel — chłodziwo w kriogenice (np. do magnetycznego rezonansu jądrowego, kriogenicznych badań), napełnianie balonów i sterowców, mieszanki oddechowe dla nurków, detekcja nieszczelności;
- Neon — reklamy świetlne i lampy wyładowcze (typowy czerwony/pomarańczowy kolor);
- Argon — gaz obojętny w procesach spawalniczych, wypełnianie żarówek i lamp, atmosfera ochronna przy pracach metalurgicznych i przy przechowywaniu materiałów wrażliwych na utlenianie;
- Krypton — specjalistyczne lampy błyskowe i wyładowcze, niektóre zastosowania w fotonice;
- Xenon — lampy ksenonowe (świetlne i do projektorów), substancje znieczulające (jako gaz anestetyczny w medycynie), paliwo do silników jonowych w technice kosmicznej;
- Radon — ze względu na promieniotwórczość związany raczej z zagrożeniem zdrowotnym (ryzyko raka płuc przy długiej ekspozycji) niż powszechnym zastosowaniem; w przeszłości wykorzystywano go w pewnych terapiach, ale obecnie raczej unika się jego stosowania.
Odkrycie i znaczące postacie w historii
Gazy szlachetne zostały rozpoznane i opisane pod koniec XIX wieku. Odkrycie argonu wiąże się z pracami Lorda Rayleigha (John William Strutt) i Sir Williama Ramsaya — Rayleigh wykazał różnicę gęstości azotu z powietrza i azotu otrzymanego z związków, co doprowadziło do wykrycia nowego gazu. Obaj naukowcy otrzymali Nagrody Nobla: Rayleigh — Nagrodę Nobla z fizyki (1904), Ramsay — Nagrodę Nobla w dziedzinie chemii (1904) za badania nad nowymi gazami, w tym nad gazami szlachetnymi i odkrycie kilku z nich.
Bezpieczeństwo i uwagi
Większość gazów szlachetnych jest nietoksyczna i obojętna chemicznie, ale mogą stwarzać zagrożenie w zamkniętych pomieszczeniach jako gazy duszące (wypierają tlen). Radon jest promieniotwórczy i uważa się go za czynnik ryzyka raka płuc — w domach budowanych na pewnych podłożach należy kontrolować jego stężenie. Przy pracy z ciekłym helem i innymi skroplonymi gazami obowiązują zasady bezpieczeństwa związane z ekstremalnie niskimi temperaturami i ryzykiem odmrożeń.
Podsumowując, gazy szlachetne to grupa pierwiastków o wspólnych cechach: monoatomowość, niska reaktywność, charakterystyczne właściwości fizyczne i szerokie zastosowanie przemysłowe oraz naukowe. Mimo swej „obojętności” niektóre z nich (szczególnie xenon) mogą tworzyć związki i odgrywać ważne role w technologii i medycynie.