Chemia metaloorganiczna to nauka o związkach chemicznych zawierających wiązania pomiędzy węglem a metalem. Łączy ona aspekty chemii nieorganicznej (badanie wiązań niewęglowych) i chemii organicznej (badanie wiązań węglowych).
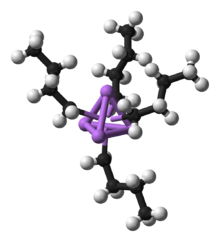
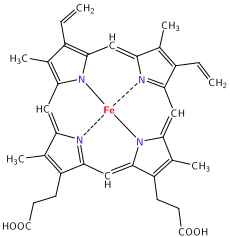
Przykładem związków metaloorganicznych jest tetraetyloołów; był on używany jako dodatek do paliw (benzyny ołowiowej) w przeszłości. Również metylokobalamina (witamina B12) jest powszechnym związkiem metaloorganicznym.
Co obejmuje chemia metaloorganiczna?
Chemia metaloorganiczna bada strukturę, własności, syntezę i reaktywność związków zawierających bezpośrednie wiązanie metal–węgiel (M–C). Obejmuje to zarówno proste związki, jak i rozbudowane kompleksy katalityczne oraz materiały funkcjonalne.
Podział i typy wiązań
- Alkilo- i arylometaloorganiczne – związki z wiązaniem M–C pochodzącym od grup alkilowych lub arylowych (np. metylokompleksy metali przejściowych).
- Karbonyle metaliczne – kompleksy zawierające ligandy CO (M–CO), ważne w katalizie i syntezie (charakteryzowane m.in. przez pasma w widmie IR).
- Hydridy metalowe – M–H, istotne w reakcjach addycji i transferu wodoru.
- Kompleksy π – wiązania metal–olefiny, metal–acetylid, często spotykane w katalizie reakcji na niesaturowanych związkach węglowych.
- Agostyczne oddziaływania i inne słabsze interakcje M···H–C, mające wpływ na geometrię i reaktywność kompleksów.
Przykłady znanych związków i katalizatorów
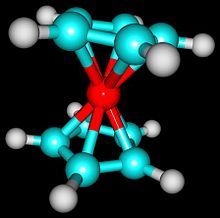
- Ferrocene – klasyczny związek typu "sandwich" (Fe w środku między pierścieniami cyklo-pienylowymi), ważny w historii chemii metaloorganicznej.
- Tetraetyloołów – historyczny dodatek do paliw (wspomniany wyżej), którego stosowanie zostało wycofane ze względu na toksyczność.
- Metylokobalamina – biologiczna forma kobalaminy (witamina B12), pokazująca związek metaloorganiczny w systemach biologicznych.
- Wilkinsonowy katalizator (RhCl(PPh3)3), katalizatory Grubbsa (metaloorganiczne kompleksy Ru) oraz kompleksy Pd stosowane w reakcjach sprzęgania (np. Suzuki, Heck) – kluczowe w syntezie organicznej i przemysłowej.
- Polimeryzacyjne katalizatory Zieglera–Nattа – metaloorganiczne związki używane do produkcji polietylenów i polipropylenów o określonych właściwościach.
Zastosowania
- Kataliza – metaloorganiczne kompleksy są fundamentem wielu reakcji przemysłowych i laboratoryjnych (np. hydrogenacja, metateza, sprzęgania krzyżowe).
- Materiały funkcjonalne – prekursory do tworzenia filmów cienkich, materiałów przewodzących, OLED-ów czy porowatych struktur typu MOF (metal–organic frameworks); warto zauważyć, że nie wszystkie MOF-y mają bezpośrednie wiązanie M–C, lecz pozostają blisko spokrewnione z chemią metaloorganiczną.
- Medycyna i biochemia – związki metaloorganiczne występują w bioczynnikach (np. B12), a także w badaniach nad lekami (np. niektóre związki metaloorganiczne wykazujące aktywność przeciwnowotworową); pola te często pokrywają się z chemią bioinorganiczną.
- Synteza organiczna – katalizatory metaloorganiczne umożliwiają wydajne tworzenie wiązań C–C i C–heteroatom, co jest fundamentem złożonej syntezy cząsteczek.
- Przemysł petrochemiczny i materiałowy – prekursory metaloorganiczne służą do modyfikacji olejów, tworzyw oraz produkcji półprzewodników.
Metody syntezy i reakcje charakterystyczne
Typowe drogi powstawania związków metaloorganicznych to transmetalcacja, addycja oksydacyjna, eliminacja redukcyjna, insertacja (np. wstawianie CO lub alkenów) oraz metody reaktywne z reagentami organometalicznymi (np. reagentami litowo- i magnezowymi). Reakcje te leżą u podstaw działania wielu katalizatorów i syntetycznych strategii.
Charakterystyka i metody analizy
- Spektroskopia NMR (w tym 13C, 1H, 31P) – dostarcza informacji o strukturze i środowisku ligandów.
- IR – szczególnie użyteczne do identyfikacji ligandów karbonylowych (pasma ν(CO)).
- Spektrometria mas – analiza masy cząsteczkowej i fragmentacji.
- Dyfrakcja rentgenowska – daje dokładne informacje o geometrii i odległościach atomowych w krysztale.
- Techniki elektrochemiczne – badanie stanów utlenienia i właściwości redoks.
Bezpieczeństwo i wpływ na środowisko
Wiele związków metaloorganicznych jest reaktywnych i niebezpiecznych (np. bardzo toksyczne Ni(CO)4, toksyczność związków ołowiu jak tetraetyloołów). Praca z nimi często wymaga stosowania atmosfery obojętnej (suchy azot lub argon), odpowiedniej aparatury i procedur BHP. Znaczący jest też aspekt środowiskowy — niektóre metaloorganiczne dodatki (jak ołów) zostały zakazane lub ograniczone ze względu na negatywny wpływ na zdrowie i środowisko.
Podsumowanie
Chemia metaloorganiczna to rozległa dziedzina łącząca elementy chemii nieorganicznej i organicznej, kluczowa dla rozwoju katalizy, materiałów funkcjonalnych i zrozumienia związków biologicznych zawierających metale. Jej narzędzia i osiągnięcia mają szerokie zastosowanie w przemyśle, medycynie i badaniach naukowych, ale wiążą się też z koniecznością zachowania ostrożności i dbałości o środowisko.