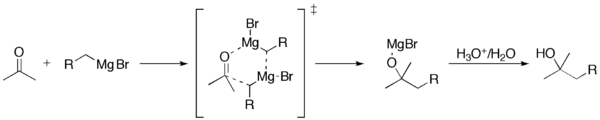
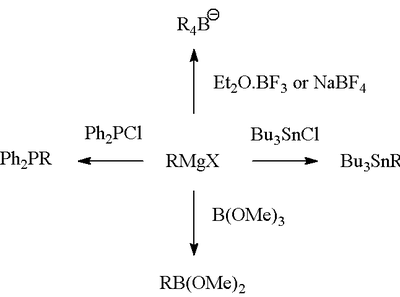
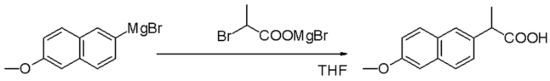
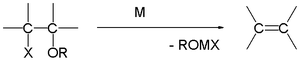
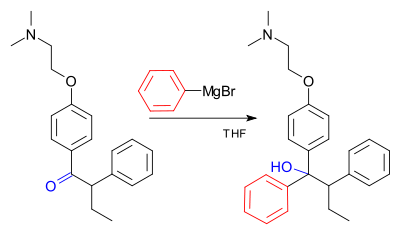
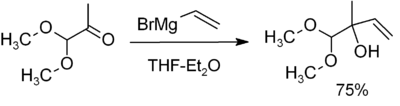Reakcja Grignarda (wymawiane /ɡriɲar/) jest metaloorganiczną reakcją chemiczną, w której halogenki alkilu lub arylu magnezu (odczynniki Grignarda) atakują elektrofilowe atomy węgla obecne w wiązaniach polarnych (na przykład w grupie karbonylowej, jak w przykładzie pokazanym poniżej). Odczynniki Grignarda działają jak nukleofile. Reakcja Grignarda powoduje powstanie wiązania węgiel-węgiel. Zmienia ona hybrydyzację wokół centrum reakcji. Reakcja Grignarda jest ważnym narzędziem w tworzeniu wiązań węglowo-węglowych. Może również tworzyć wiązania węgiel-fosfor, węgiel-cyna, węgiel-krzem, węgiel-boron i inne wiązania węgiel-heteroatom.
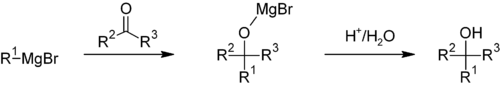
Jest to nukleofilna reakcja dodatku organometalicznego. Wysoka wartość pKa składnika alkilowego (pKa = ~45) sprawia, że reakcja jest nieodwracalna. Reakcje Grignarda nie są jonowe. Odczynnik Grignarda istnieje jako skupisko metaloorganiczne (w eterze).
Wadą odczynników Grignarda jest to, że łatwo reagują one z rozpuszczalnikami protonowymi (takimi jak woda) lub z grupami funkcyjnymi z kwaśnymi protonami, takimi jak alkohole i aminy. Wilgotność powietrza może zmienić wydajność wytwarzania odczynnika Grignarda z toczenia magnezu i halogenku alkilu. Jedną z wielu metod stosowanych w celu wykluczenia wody z atmosfery reakcyjnej jest suszenie płomieniem naczynia reakcyjnego w celu odparowania całej wilgoci, które jest następnie zamykane, aby zapobiec powrotowi wilgoci. Następnie chemicy używają ultradźwięków do aktywacji powierzchni magnezu, tak aby zużywała ona całą obecną wodę. Może to umożliwić tworzenie się odczynników Grignarda z mniejszą wrażliwością na obecność wody.
Kolejną wadą odczynników Grignarda jest to, że nie tworzą one łatwo wiązań węglowo-węglowych poprzez reakcję z halogenkami alkilowymi za pomocą mechanizmuSN2.
François Auguste Victor Grignard odkrył reakcje Grignarda i odczynniki. Zostały one nazwane na cześć tego francuskiego chemika (Uniwersytet w Nancy, Francja), który za tę pracę otrzymał w 1912 r. Nagrodę Nobla w dziedzinie chemii.
Mechanizm powstawania i charakter odczynników Grignarda
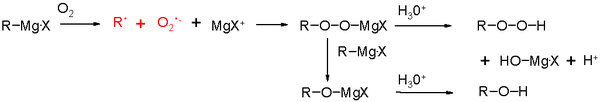
Odczynniki Grignarda mają ogólny wzór RMgX (R = alkil, aryl; X = Cl, Br, I). Powstają przez reakcję halogenku organicznego R–X z metalicznym magnezem w suchym eterze (np. eter dietylowy) lub w THF. Proces inicjacji obejmuje wstawienie magnezu do wiązania C–X; mechanizm może przebiegać przez etap transferu pojedynczego elektronu i krótkotrwałe rodniki lub przez bardziej złożone etapy agregacyjne, ale w warunkach stosowanych w syntezie praktycznej traktuje się produkt jako reagent o znacznym charakterze nukleofilowym (karboanionopodobnym), związany z kationem Mg2+ i rozpuszczalnikiem eterowym.
Reakcja z grupami karbonylowymi — typowy przebieg
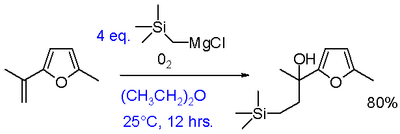
- Atak nukleofilowy: RMgX atakuje elektrofilowy atom węgla w grupie karbonylowej, tworząc tetraedryczny alkoksylan magnezu.
- Hydroliza (workup): po dodaniu wodnego środka kwaśnego (np. H3O+) alkoksylan ulega protonacji i uwalniana jest odpowiednia alkohol – produktyem zależnym od natury substratów (np. addycja do aldehydów daje alkohole drugorzędowe, do ketonów – trzeciorzędowe itp.).
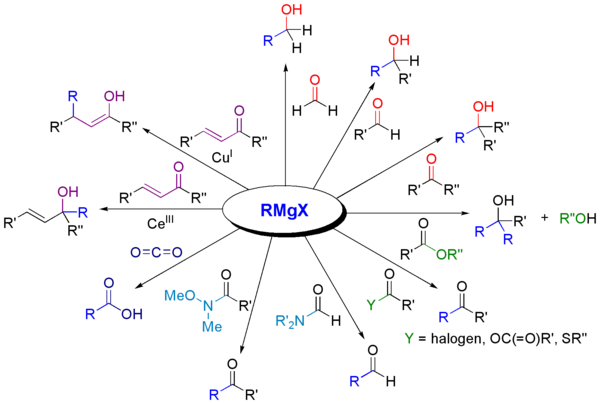
Przykłady reakcji i produkty
- aldehyd + RMgX → po uwodnieniu: alkohol drugorzędowy
- keton + RMgX → po uwodnieniu: alkohol trzeciorzędowy
- estery + 2 RMgX → po uwodnieniu: alkohol trzeciorzędowy (pośrednio przez keton i jego dalszą addycję)
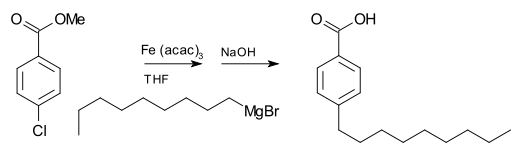
- CO2 + RMgX → po uwodnieniu: kwas karboksylowy (karboksylacja)
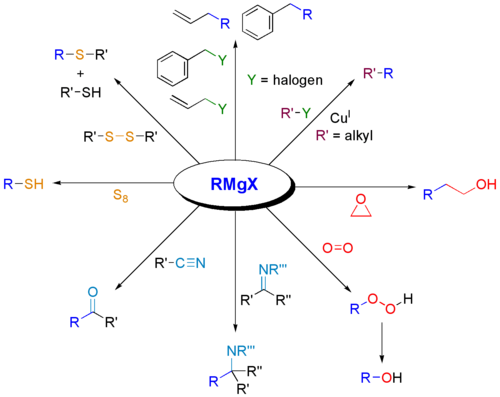
- epoksydy + RMgX → otwarcie pierścienia i powstanie alkoholu po uwodnieniu (z regułą ataku w mniej sterycznie zatłoczonym centrum)
- nitryle + RMgX → po hydrolizie: ketony (poprzez utworzenie iminowego kompleksu, następnie hydrolizę)
Warunki i rozpuszczalniki
Odczynniki Grignarda stabilizowane są przez etery (np. eter dietylowy) lub THF, które koordynują jon magnezowy i umożliwiają istnienie rozpuszczalnych kompleksów. Obowiązuje całkowite wyłączenie wilgoci i obecności grup funkcyjnych zawierających protons (–OH, –NH, –COOH), bo reagują one z RMgX, prowadząc do dezaktywacji (protonoliza) i powstawania węglowodorów R–H.
Ograniczenia i sposoby ich obejścia
- Wrażliwość na protony: konieczne jest stosowanie związków chroniących grupy funkcyjne (np. grupy ochronne dla alkoholi) lub użycie alternatywnych reagentów (np. odczynniki organolitowe w specyficznych przypadkach).
- Trudności w rekacji z halogenkami alkilowymi: bezpośrednia reakcja RMgX z R'–X w mechanizmie SN2 jest mało wydajna ze względu na tendencję do przebiegu przez transfer elektronowy i sprzęganie (np. reakcje Wurtza). Dlatego syntezy węglowo-węglowe zazwyczaj polegają na addycjach do karbonylów, karboksylacji CO2 czy otwieraniu epoksydów.
- Aktywacja magnezu: aby rozpocząć reakcję formowania RMgX, często stosuje się metody aktywacji Mg (czyszczenie powierzchni, dodatki jodu, bromku etylenu, ultradźwięki, użycie drobnych form Mg lub tzw. Rieke magnesium).
- Wybór halogenu: bromki i jodki zwykle reagują łatwiej niż chlorki; jednakże chlorki są tańsze i często używane przy odpowiedniej aktywacji.
Wariacje i udoskonalenia
- Reaktywniejsze formy Mg (np. Rieke Mg) umożliwiają tworzenie odczynników z mniej reaktywnych halogenków.
- Kompleksy z dodatkowymi solami, np. reagenty typu "Turbo-Grignard" (i-PrMgCl·LiCl), poprawiają rozpuszczalność i selektywność w niektórych transformacjach.
- Użycie in situ generowanych odczynników Grignarda w większych sekwencjach wieloetapowych pozwala uniknąć izolacji wrażliwych pośrednich związków.
Bezpieczeństwo i praktyka laboratoryjna
- Odczynniki Grignarda są silnie reaktywne i palne — należy pracować w suchym i beziskrowym środowisku, z dostępem do azbestu czy innych materiałów gaśniczych przy pracy z rozpuszczalnikami eterowymi.
- Przechowywanie: większość odczynników Grignarda przechowuje się w ściśle suchych i zamkniętych naczyniach; niektóre gotowe roztwory dostępne komercyjnie dostarczane są w substancjach rozpuszczalnikowych o znanej stężeniu.
- Workup: reakcje zwykle kończy się dodaniem rozcieńczonego kwasu (np. NH4Cl, H3O+) przy zachowaniu kontroli temperatury, bo reakcja protonolizy może być egzotermiczna.
Zastosowania syntetyczne
Reakcja Grignarda to podstawowe narzędzie w syntezach organicznych: budowa łańcuchów węglowych, syntezy alkoholi, wytwarzanie prekursorów farmaceutyków, materiałów i ligandów. Dzięki swojej uniwersalności i względnej prostocie jest często pierwszym wyborem przy tworzeniu nowych wiązań C–C w laboratoriach badawczych i przemysłowych.
Krótka nota historyczna
Odkrycie dokonane przez François Auguste Victora Grignarda otworzyło nowe możliwości w chemii organicznej — za tę pracę otrzymał on w 1912 r. Nagrodę Nobla w dziedzinie chemii.
Praktyczne wskazówki dla początkujących
- Upewnij się, że szkło jest suche i wygrzane; odstanie butelki z rozpuszczalnikiem nad sodem lub użycie młynka z osuszaczem zwiększa szanse powodzenia.
- Stosuj nadmiar R–X lub magnezu, jeśli inicjacja jest powolna; dodatki takie jak jod lub kilka kropli 1,2-dibromoetanu często „startują” reakcję.
- Kontroluj temperaturę przy wprowadzaniu substratów karbonylowych — addycja może być egzotermiczna i prowadzić do ubocznych reakcji, jeżeli dodajesz reagent zbyt szybko.
Podsumowując, reakcja Grignarda to wszechstronna i fundamentalna metoda w chemii organicznej, umożliwiająca tworzenie nowych wiązań C–C i wielu innych transformacji, jednak wymagająca starannego prowadzenia z uwagi na wrażliwość na protony i wilgoć.