Styren jest pewnym organicznym związkiem chemicznym o wzorze chemicznym C8H8. Jego struktura chemiczna składa się z grupy winylowej połączonej z pierścieniem benzenowym. Ten pierścień benzenowy sprawia, że styren jest związkiem aromatycznym. W temperaturze pokojowej i pod ciśnieniem styren jest klarowną, bezbarwną cieczą. Innymi nazwami styrenu mogą być: styrol, winylobenzen, fenyloten lub fenyloetylen.
Podstawowe właściwości fizyczne i chemiczne
- Wzór sumaryczny: C8H8.
- Masa molowa: ≈ 104,15 g·mol−1.
- Wygląd: bezbarwna, przejrzysta ciecz o charakterystycznym zapachu.
- Temperatura wrzenia: około 145 °C.
- Temperatura topnienia: około −30,6 °C.
- Gęstość: poniżej 1 g·cm−3 (około 0,9 g·cm−3 w temperaturze otoczenia).
- Lotność i zapalność: łatwo paruje i tworzy z powietrzem mieszaniny wybuchowe; należy traktować go jako substancję łatwopalną.
- Cechy chemiczne: typowy monomer do reakcji addycyjnej (polimeryzacja), podlega reakcji elektrofiliowej na pierścieniu aromatycznym oraz może ulegać utlenianiu i polimeryzacji samorzutnej.
Produkcja i surowce
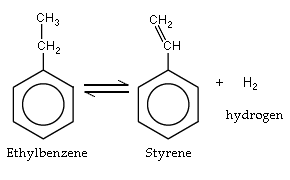
- Przemysłowo styren powstaje głównie przez dehydrogenację etylobenzenu (najczęściej katalityczną) lub jako produkt pośredni w przemyśle paliwowo-chemicznym.
- W procesach produkcyjnych stosuje się destylację i inne etapy oczyszczania; do monomeru dodaje się inhibitory (np. tert‑butylokatechol, TBC) aby zapobiegać polisomeryzacji w czasie przechowywania i transportu.
Polimeryzacja i najważniejsze produkty pochodne
- Polistyren (PS): homopolimer styrenu, szeroko stosowany w formie twardych tworzyw, pianek (EPS — spieniony polistyren) oraz w wersjach wysokoudarowych (HIPS).
- Kopolimery i modyfikacje: SAN (styren‑akrylonitryl), ABS (akrylonitryl‑butadien‑styren), SBS (styren‑butadien‑styren) — materiały o różnorodnych właściwościach mechanicznych i zastosowaniach.
- Surowiec dla kauczuków: styren jest składnikiem w produkcji kauczuków syntetycznych (np. SBR — styren‑butadienowy kauczuk).
- Żywice i farby: stosowany także jako monomer do żywic, spoiw i niektórych rodzajów powłok.
Zastosowania
- Produkcja tworzyw sztucznych: polistyrenu, ABS, SAN — wykorzystanie w opakowaniach, elementach AGD, częściach motoryzacyjnych, zabawkach.
- Materiały izolacyjne i opakowaniowe: spieniony polistyren (EPS i XPS).
- Przemysł chemiczny: surowiec do syntezy innych związków chemicznych i żywic.
- Przemysł motoryzacyjny i budowlany: części z tworzyw, izolacje, powłoki.
- Laboratoria i produkcja specjalistyczna: monomer do syntez i doświadczalnych kopolimeryzacji.
Zagrożenia dla zdrowia i środowiska
- Oddziaływanie na zdrowie: narażenie drogą wziewną lub kontaktem skórnym może powodować podrażnienia oczu i dróg oddechowych. Przy wyższych stężeniach możliwe są objawy działania narkotycznego (bóle głowy, zawroty, senność). Długotrwałe lub intensywne narażenie bywa związane z działaniem neurotoksycznym i innymi skutkami przewlekłymi.
- Rakotwórczość: międzynarodowe agencje oceniają styren jako związek o potencjalnym ryzyku rakotwórczym; oceny klasyfikacyjne i wymagania regulacyjne różnią się w zależności od organizacji i kraju — w literaturze naukowej i dokumentach instytucji takich jak IARC znajdują się szczegółowe analizy.
- Środowisko: styren łatwo paruje do atmosfery; w wodzie i glebie ulega procesom degradacji, ale może wykazywać toksyczność dla organizmów wodnych przy wysokich stężeniach. Emisje z zakładów przemysłowych i procesów spalania wymagają kontroli.
Bezpieczeństwo, magazynowanie i postępowanie
- Przechowywać w chłodnym, dobrze wentylowanym miejscu, z dala od źródeł ciepła i zapłonu oraz od utleniaczy.
- Opakowania uziemione i wyposażone w zabezpieczenia przeciwiskrowe; stosować środki zapobiegające samorzutnej polimeryzacji (inhibitory) podczas przechowywania.
- Stosować odpowiednie wyposażenie ochronne (rękawice odporne na rozpuszczalniki, okulary ochronne, odpowiednia maska lub respirator przy narażeniach powyżej dopuszczalnych wartości).
- Postępowanie w przypadku wycieku: ograniczyć rozlew, usunąć źródła zapłonu, użyć materiałów absorbujących, właściwie zutylizować odpady zgodnie z przepisami lokalnymi.
- W pierwszej pomocy: przy wdychaniu — zapewnić świeże powietrze; przy kontakcie ze skórą — zdjąć skażoną odzież i przemyć skórę wodą z mydłem; przy dostaniu się do oczu — płukać dużą ilością wody i zgłosić się do lekarza.
Analiza i identyfikacja
- Styren identyfikuje się i oznacza przy użyciu technik takich jak chromatografia gazowa (GC), GC‑MS, spektroskopia IR i NMR.
- W warunkach przemysłowych monitoruje się stężenia w powietrzu i emisje przy użyciu dedykowanych metod pomiarowych.
Uwagi końcowe
Styren jest kluczowym monomerem w przemyśle tworzyw sztucznych i chemicznym, ale ze względu na łatwopalność oraz ryzyko zdrowotne jego stosowanie wymaga przestrzegania zasad bezpieczeństwa i regulacji środowiskowych. W praktyce przemysłowej dba się o stabilizację monomeru inhibitorami, kontrolę emisji oraz monitorowanie narażenia pracowników.