Sulfotlenek to cząsteczka, która ma atom siarki połączony z dwoma węglami i jednym atomem tlenu. Powstaje w wyniku utleniania tioeterów, bez przechodzenia przez całą drogę do sulfonu. Jak wiele cząsteczek zawierających siarkę, sulfotlenek może czasami silnie pachnieć.
Budowa i właściwości
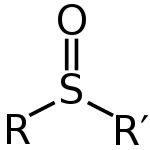
Sulfotlenki można zapisać wzorem ogólnym R–S(=O)–R'. Siarka tworzy formalne podwójne wiązanie z tlenem i pojedyncze wiązania z dwoma atomami węgla, przy czym na atomie siarki pozostaje jedna samotna para elektronowa. Elektronowa struktura powoduje, że środowisko przy siarce ma aproximatywnie tetraedryczny geometryczny układ. Obecność lone pair wpływa też na polarność wiązania S=O i całej cząsteczki — sulfotlenki są zazwyczaj polarne i dobrze rozpuszczają się w polarnych rozpuszczalnikach.
Sulfotlenki wykazują charakterystyczne właściwości chemiczne:
- Polaryzacja: silne dipolowe S=O nadaje im zdolność do stabilizowania jonów i koordynowania metali.
- Aktywność przy atomach α: atomy węgla bezpośrednio sąsiadujące z siarką (pozycje α) często mają zmniejszoną kwasowość i mogą ulegać alkilacji, kondensacjom lub epimeryzacji po odpowiedniej aktywacji.
- Zapach: wiele niskocząsteczkowych sulfotlenków ma silny, ostry zapach podobny do zapachu związków siarkowych.
Stereochemia — siarka jako centrum chiralne
Siarka w sulfotlenkach może być centrum chiralnym (sulfoxydy chiralne). Wynika to z faktu, że do siarki przyłączone są trzy różne "grupy" (dwa różne łańcuchy R i lone pair traktowany jako trzecia "grupa"), co daje możliwość istnienia enancjomerów. Bariera inwersji konfiguracji przy siarce bywa na tyle duża, że niektóre sulfoxydy są trwałymi enancjomerami i można je rozdzielać i stosować jako związki chirale w syntezach asymetrycznych.
Synteza i przemiany chemiczne
Typowa metoda otrzymywania sulfotlenków to selektywne utlenianie tioeterów (sulfidów) do odpowiedniego stopnia oksydacji. Najczęściej stosowane utleniacze to:
- nad-tlenki organiczne (np. mCPBA),
- nadtlenek wodoru (H2O2) w obecności katalizatorów,
- inne łagodne utleniacze pozwalające zatrzymać reakcję na etapie sulfoxidu (unikać nadmiaru, bo powstaje sulfon).
Sulfotlenki łatwo ulegają dalszym przemianom, m.in.:
- utlenianiu do sulfonów (R–S(=O)2–R'),
- reakcjom typu Pummerer — aktywacja sulfoxydów prowadzi do tworzenia intermediatów sulfoniowych, które mogą przekształcać się w produkty z przesunięciem grupy i tworzeniem nowych wiązań węgiel–węgiel i węgiel–heteroatom, co ma szerokie zastosowanie w syntezie organicznej,
- reakcjom α-alkilacji i kondensacji po odpowiedniej aktywacji.
Zastosowania i przykład DMSO
Sulfotlenki mają wiele zastosowań w chemii i przemyśle:
- Ligandy w kompleksach metali: sulfotlenki są dobrymi ligandami dla metali przejściowych, koordynując zwykle przez atom tlenu zespolonego w S=O. Kompleksy te stosuje się np. w katalizie i chemii materiałów.
- Intermediary w syntezie organicznej: sulfoxydy służą jako pośredniki w reakcjach Pummerera, w reakcjach eliminacji czy jako grupy opuszczające w specyficznych warunkach.
- Farmacja i chemia bio-org. niektóre sulfoxydy i ich pochodne mają znaczenie farmakologiczne lub są używane jako chirale pomocnicze w syntezach leków.
Przykładem najważniejszego sulfotlenku jest sulfotlenek dimetylu — dimetylosulfotlenek, znany szerzej jako DMSO. Jest on również nazywany DMSO. Jest on stosowany jako rozpuszczalnik w wielu reakcjach, zwłaszcza w biochemii. Główne cechy i zastosowania DMSO:
- Polarny, aprotyczny rozpuszczalnik: dobrze rozpuszcza zarówno związki polarne, jak i wiele substancji organicznych; często używany tam, gdzie inne rozpuszczalniki zawodzą.
- Właściwości fizyczne: DMSO jest miscible z wodą, ma stosunkowo wysoką temperaturę wrzenia i charakteryzuje się dobrą stabilnością termiczną (często stosowany jako rozpuszczalnik reakcji w umiarkowanych temperaturach).
- Zastosowania specjalistyczne: jako rozpuszczalnik do reakcji utleniania (np. w protokołach typu Swern po aktywacji DMSO), jako rozpuszczalnik do spektroskopii (DMSO‑d6 w NMR), jako nośnik związków w badaniach biologicznych, oraz jako składnik buforów i nośników w biotechnologii.
- Krioprotektant i przenikanie przez skórę: DMSO stosuje się jako krioprotektant w przechowywaniu komórek i tkanek; ma też zdolność zwiększać przepuszczalność skóry, co bywa wykorzystywane, ale także wymaga ostrożności (DMSO może przenosić rozpuszczone w nim substancje przez skórę).
Bezpieczeństwo i przechowywanie
Przy pracy z sulfotlenkami, a zwłaszcza z DMSO, należy pamiętać o kilku zasadach bezpieczeństwa:
- Używać rękawic i chronić skórę — DMSO łatwo przenika przez skórę i może przenosić rozpuszczone w nim toksyny do organizmu.
- Unikać przypadkowego kontaktu z silnymi utleniaczami — mieszaniny mogą być reaktywne, a DMSO w obecności silnych utleniaczy może ulec gwałtownym przemianom.
- Przechowywać w szczelnych pojemnikach, z dala od źródeł ognia i wysokich temperatur; zapewnić dobrą wentylację przy użyciu lotnych sulfoxydów o intensywnym zapachu.
- Przestrzegać odpowiednich procedur utylizacji i zasad BHP w laboratorium.
Podsumowując, sulfotlenki (sulfoxydy) to wszechstronna klasa związków siarki o specyficznej budowie, interesującej stereochemii i szerokim zastosowaniu — od katalizy i syntezy organicznej po rolę rozpuszczalników i reagentów w chemii biologicznej. DMSO pozostaje najbardziej znanym przedstawicielem tej grupy ze względu na unikalne właściwości rozpuszczalnikowe i praktyczne zastosowania.