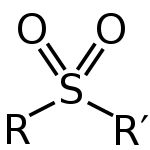
Sulfon to cząsteczka, która ma atom siarki z wiązaniami z dwoma atomami tlenu. Siarka ma dwa podwójne wiązania z dwoma atomami tlenu. Z pozostałymi dwiema grupami ma wiązanie pojedyncze. Zazwyczaj są one wytwarzane przez utlenianie tioeterów.
Są one wykorzystywane w wielu ważnych reakcjach chemicznych. Na przykład, olefinacja Julii wykorzystuje sulfon do wytworzenia alkenu z aldehydu. Są one również czasami używane jako rozpuszczalniki.
Budowa i właściwości
W sensie strukturalnym sulfon (często w literaturze anglojęzycznej określany jako sulfone) ma ogólny wzór R–S(=O)2–R', gdzie atom siarki jest związany dwiema grupami organicznymi (R, R') oraz dwoma atomami tlenu poprzez wiązania będące formalnie podwójnymi. Grupa sulfonowa jest silnie elektroujemna i nadaje cząsteczkom wyraźny moment dipolowy. W praktyce związki te występują jako bezbarwne ciecze lub ciała stałe, charakteryzują się wysokimi temperaturami wrzenia, dobrą stabilnością termiczną i chemiczną oraz często wysoką polarnością.
Warto rozróżnić sulfon od pokrewnych grup funkcyjnych: sulfonyl (–SO2–) to fragment występujący w większych cząsteczkach, kwasy sulfonowe (–SO3H) mają dodatkowy atom tlenu i właściwości silnie kwasowe, a sulfonamidy zawierają wiązanie S–N. Stopień utlenienia siarki w sulfonie odpowiada zwykle +4.
Synteza i typowe przemiany
Najczęstszą metodą otrzymywania sulfonów jest utlenianie tioeterów (tioeter = tioeter, ang. thioether) przez odpowiednie utleniacze. Utlenianie przebiega często etapowo: najpierw powstaje sulfoxyd (R–S(=O)–R'), a przy dalszym utlenianiu — sulfon (R–S(=O)2–R'). Typowe utleniacze stosowane w syntezie to nadtlenek wodoru (H2O2), perkwasy (np. mCPBA) lub sole typu oxone.
Inne drogi syntezy obejmują tworzenie sulfonów z użyciem chlorków sulfonylowych (R–SO2Cl) w reakcjach z nukleofilami oraz metodiki prowadzące przez pochodne siarki, np. oksydację tioli lub przekształcenia w reakcjach przebiegających przez addycję do wiązań wielokrotnych. Sulfony łatwo ulegają reakcjom, w których grupa –SO2– stabilizuje aniony sąsiednie (kwaśność wodorków α), co umożliwia alkilacje, kondensacje i przekształcenia prowadzące do złożonych struktur organicznych.
Zastosowania
- Synteza organiczna: Sulfony są kluczowymi substratami i pośrednikami w reakcjach takich jak olefinacja Julii, Ramberg–Bäcklund (przekształcenie sulfonu w alken) czy alkilacje z użyciem anionów α-sulfonowych. Grupa sulfonowa stabilizuje karboaniony, co ułatwia przeprowadzanie selektywnych reakcji C–C.
- Rozpuszczalniki i media reakcyjne: Niektóre sulfony, np. sulfolane (1,1-dioxid tetrahydrotiophenu), są używane jako polarne, aprotyczne rozpuszczalniki o wysokiej stabilności termicznej, praktyczne w procesach przemysłowych.
- Materiały i polimery: Polimery zawierające jednostki sulfonowe, jak polisulfony, wykazują wysoką odporność termiczną i mechaniczną i stosowane są w przemyśle motoryzacyjnym, lotniczym i elektrycznym.
- Farmacja i chemia biologiczna: Fragment –SO2– jest powszechnie spotykany w lekach (sulfonamidy, niektóre inhibitory enzymów) ze względu na swoją trwałość i właściwości elektronowe. Przykładem prostego i znanego związku jest dimetylosulfon (MSM, (CH3)2SO2), stosowany jako suplement i składnik kosmetyków.
- Rolnictwo i chemia specjalistyczna: Sulfony i pochodne sulfonowe są stosowane jako aktywne składniki w agrochemii oraz w syntezie związków funkcjonalnych.
Właściwości reakcyjne i praktyczne uwagi
W chemii syntetycznej sulfon pełni rolę grupy odciągającej elektrony, dzięki czemu aktywuje sąsiednie pozycje do tworzenia karboanionów. To czyni go użytecznym narzędziem do formowania wiązań C–C. Sulfony są zwykle stabilne wobec szerokiego zakresu warunków chemicznych, ale mogą być redukowane lub poddawane specyficznym przekształceniom (np. usuwanie grupy sulfonylowej w reakcjach redukcyjnych).
Pod względem bezpieczeństwa, wiele prostych sulfonów ma niską toksyczność, ale właściwości fizykochemiczne (wysokie temperatury wrzenia, lepkość, rozpuszczalność) wymagają uwagi przy gospodarowaniu odpadami i pracy w laboratorium. Zawsze należy stosować się do kart charakterystyki (MSDS) i zasad BHP.
Podsumowanie
Sulfony (sulfony/sulfon) to ważna grupa związków zawierających atom siarki z dwoma wiązaniami do tlenu i dwiema resztami organicznymi. Dzięki swojej stabilności, polarności i zdolności do stabilizowania karboanionów są szeroko stosowane zarówno w syntezach organicznych (np. olefinacja Julii), jak i w przemyśle jako rozpuszczalniki, komponenty polimerów czy składniki leków i produktów chemii specjalistycznej.