Reakcja chemiczna zachodzi, gdy jedna lub więcej substancji chemicznych zostaje przekształcona w jedną lub więcej innych substancji. W czasie reakcji zmienia się rozkład atomów i elektronów w cząsteczkach, a często także występuje wymiana energii.
Przykłady i typowe procesy
- Utlenianie: łączenie żelaza z tlenem, prowadzące do powstania rdzy.
- Reakcje kwas‑zasada: np. mieszanie octu z sodą oczyszczoną, dające octan sodu, dwutlenek węgla i wodę.
- Spalanie i wybuchy: szybkie reakcje utleniania, które wydzielają dużą ilość ciepła i często gazów.
- Reakcje biologiczne: setki przemian chemicznych zachodzących w organizmach żywych, umożliwiających metabolizm i przekazywanie informacji.
- Reakcje elektrochemiczne: procesy zachodzące podczas ładowania i rozładowywania akumulatorów, czyli reakcje elektrochemiczne w ogniwach, obserwowane np. w akumulatorach.
Szybkość reakcji i czynniki wpływające
Szybkość reakcji chemicznej może się znacznie różnić: niektóre zachodzą bardzo szybko (milisekundy), inne bardzo wolno (lata). Główne czynniki wpływające to:
- Temperatura — wzrost temperatury zwykle przyspiesza reakcje; przykład: drewno nie reaguje z powietrzem w niskiej temperaturze, lecz po osiągnięciu punktu zapłonu zaczyna się palić.
- Stężenia reagentów i ciśnienie (dla gazów).
- Powierzchnia kontaktu substancji oraz mieszanie.
- Katalizatory — substancje przyspieszające reakcję bez trwałej przemiany własnej.
Energia w reakcjach chemicznych
Reakcje mogą wiązać się z wymianą energii z otoczeniem:
- Reakcje wydzielające energię (ciepło, światło) nazywane są reakcjami egzotermicznymi. W trakcie takich przemian następuje uwolnienie energii.
- Reakcje pochłaniające energię to reakcje endotermiczne, które wymagają dopływu energii z zewnątrz.
Reakcje chemiczne a reakcje jądrowe
Reakcje jądrowe nie są reakcjami chemicznymi. Główna różnica polega na tym, że chemia obejmuje zmiany rozmieszczenia elektronów wokół atomów, natomiast w reakcjach jądrowych zachodzą przemiany jąder atomowych i uczestniczą w nich protony oraz neutrony w jądrach atomowych. Reakcje jądrowe wpływają na tożsamość pierwiastka, a reakcje chemiczne nie zmieniają liczby protonów w jądrze.
Podstawowe klasyfikacje reakcji
W nauce wyróżnia się kilka wygodnych kategorii reakcji, które pomagają opisywać i przewidywać przebieg przemian:
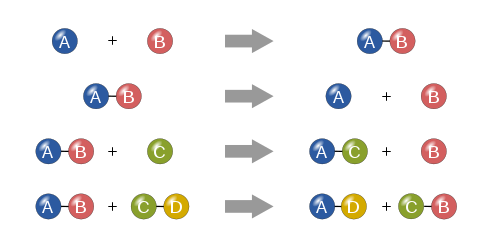
- Reakcje syntezy i analizy (łączenie lub rozkład substancji).
- Reakcje wymiany pojedynczej i podwójnej.
- Reakcje redoks — obejmujące utlenianie i redukcję.
- Reakcje kwas‑zasada oraz reakcje tworzenia osadów (precypitacja).
Znaczenie praktyczne
Reakcje chemiczne są podstawą wielu procesów technologicznych i życiowych: przemiany energetyczne w silnikach, synteza leków, przetwarzanie materiałów, fermentacja żywności czy fotosynteza w roślinach. Zrozumienie mechanizmów reakcji pozwala kontrolować ich przebieg, zwiększać wydajność i minimalizować skutki niepożądane.