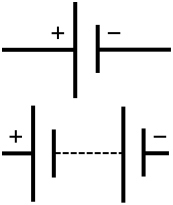Bateria przekształca energię chemiczną w energię elektryczną w wyniku reakcji chemicznej. Zazwyczaj substancje chemiczne (elektrody i elektrolit) są zamknięte wewnątrz obudowy baterii. Bateria dostarcza energię do obwodu, aby zasilić inne elementy lub komponenty. W praktyce bateria wytwarza prąd stały (DC) — prąd, który płynie w jednym kierunku i nie zmienia biegunowości.
Korzystanie z energii elektrycznej z gniazdka jest często tańsze i bardziej wydajne niż magazynowanie energii w bateriach, ale akumulator (bateria wtórna) jest niezbędny tam, gdzie nie ma dystrybucji energii elektrycznej lub gdy potrzebujemy zasilania w ruchu — na przykład w pojazdach elektrycznych czy w telefonach komórkowych. Baterie umożliwiają też pracę urządzeń przenośnych, zasilanie awaryjne i magazynowanie energii ze źródeł odnawialnych.
Baterie mogą być pierwotne lub wtórne. Pierwotne są jednorazowe — po wyczerpaniu ich nie można (lub jest to nieopłacalne) ponownie naładować i są wyrzucane. Wtórne (akumulatory) można ładować i używać wielokrotnie.
Ogniwo a bateria — jaka jest różnica?
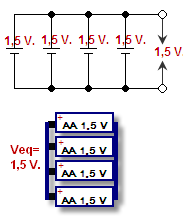
Ogniwo (elektrochemiczne) to podstawowy element, w którym zachodzi reakcja utleniania–redukcji i powstaje różnica potencjałów między dwiema elektrodami. Bateria w potocznym użyciu oznacza pojedyncze ogniwo (np. paluszka AA) lub zespół ogniw połączonych szeregowo lub równolegle w jedną całość (np. akumulator samochodowy składający się z kilku ogniw). W praktyce „bateria” może więc oznaczać pojedyncze ogniwo lub zestaw ogniw o określonej napięciowej i pojemnościowej konfiguracji.
Zasada działania
Bateria działa dzięki reakcji redoks pomiędzy dwiema elektrodami (anodą i katodą) oraz przewodzącemu jonowo elektrolitowi. Podstawowe elementy to:
- Anoda — elektroda, na której zachodzi utlenianie (oddawanie elektronów).
- Katoda — elektroda, na której zachodzi redukcja (pobieranie elektronów).
- Elektrolit — przewodnik jonowy, umożliwiający transport jonów pomiędzy elektrodami.
- Sekretor / separator — izolator elektryczny, który zapobiega zwarciu, pozwalając jednocześnie na przepływ jonów.
Gdy podłączymy obciążenie, elektrony przepływają z anody przez zewnętrzny obwód do katody, wykonując pracę (zasilając urządzenie), a jony w elektrolitcie przemieszczają się, aby zrównoważyć ładunki. Napięcie nominalne zależy od zastosowanych materiałów elektrody i elektrolitu.
Rodzaje baterii i ogniw
- Baterie pierwotne — np. ogniwa cynkowo-węglowe, alkaliczne (AA, AAA), baterie guzikowe (CR2032). Charakteryzują się wysoką gęstością energii i prostotą, ale nie dają się efektywnie ładować.
- Baterie wtórne (akumulatory) — np. ołowiowo-kwasowe (akumulator samochodowy), niklowo-wodorkowe (NiMH), niklowo-kadmowe (NiCd), litowo-jonowe (Li-ion) i litowo-polimerowe (LiPo). Mogą być wielokrotnie ładowane i rozładowywane, różnią się gęstością energii, żywotnością i wymaganiami ładowania.
- Specjalistyczne ogniwa — ogniwa przepływowe (flow batteries) do magazynowania dużej energii, ogniwa paliwowe do bezpośredniej konwersji paliwa na energię elektryczną.
Podstawowe parametry techniczne
- Napięcie nominalne — zależne od chemii: np. ogniwo alkaliczne ~1,5 V, NiMH ~1,2 V, ogniwo li-ion ~3,6–3,7 V, ogniwo ołowiowo-kwasowe ~2 V na ogniwo.
- Pojemność — podawana w mAh lub Ah; określa ilość ładunku, jaką ogniwo może oddać przy określonym prądzie rozładowania.
- Gęstość energii — energia na jednostkę masy lub objętości (ważne dla urządzeń przenośnych i pojazdów elektrycznych).
- Gęstość mocy — zdolność dostarczenia dużego prądu przez krótką chwilę (ważne dla rozruchu silnika, narzędzi elektrycznych).
- Opór wewnętrzny — wpływa na spadek napięcia pod obciążeniem i na wydzielanie ciepła.
- Cykl życia — liczba cykli ładowania/rozładowania, po których pojemność spada do określonego poziomu.
- Samoistne rozładowanie — utrata ładunku podczas przechowywania; różne chemie mają różne tempo samorozładowania.
Ładowanie i eksploatacja
Akumulatory wtórne wymagają odpowiednich metod ładowania. Najczęściej stosowane tryby to ładowanie prądem stałym (CC), ładowanie stałym napięciem (CV) oraz kombinacja CC–CV (np. dla Li‑ion). Parametry ładowania (prąd, napięcie, temperatura) muszą być dobrane do chemii ogniwa, aby uniknąć degradacji albo zagrożeń bezpieczeństwa. Ważne zasady eksploatacji:
- Unikać głębokiego rozładowania i przeładowania (szczególnie w niektórych chemiach).
- Przechowywać w umiarkowanej temperaturze; niskie i wysokie temperatury skracają żywotność.
- Dla akumulatorów NiCd mogą występować efekty „memory” — wymagają okresowego pełnego rozładowania (rzadsze w nowoczesnych NiMH i Li‑ion).
Zastosowania
Baterie i ogniwa znajdują zastosowanie w bardzo szerokim zakresie:
- Urządzenia przenośne: telefony, laptopy, tablety, aparaty fotograficzne.
- Transport: pojazdy elektryczne, hybrydowe, rowery elektryczne.
- Zasilanie awaryjne i UPS, magazynowanie energii w instalacjach PV.
- Systemy rozproszone i IoT — długowieczne baterie do czujników.
- Sprzęt medyczny, narzędzia bezprzewodowe, zabawki i wiele innych.
Bezpieczeństwo, środowisko i utylizacja
Nieodpowiednie obchodzenie się z bateriami może powodować zagrożenia: wyciek elektrolitu, zwarcie, przegrzewanie, a w przypadku niektórych baterii litowych — thermal runaway prowadzący do zapłonu lub wybuchu. Dlatego:
- Stosować oryginalne lub zalecane ładowarki i układy zabezpieczeń.
- Unikać mechanicznych uszkodzeń i przechowywania z metalowymi przedmiotami mogącymi spowodować zwarcie.
- Utylizować zużyte baterie zgodnie z lokalnymi przepisami — wiele typów (szczególnie zawierających metale ciężkie lub cenne materiały jak lit, kobalt, ołów) podlega recyklingowi.
Podsumowanie
Bateria (ogniwo lub zestaw ogniw) to podstawowe źródło energii w urządzeniach przenośnych i systemach awaryjnych. Wybór odpowiedniego typu zależy od wymagań dotyczących napięcia, pojemności, gęstości energii, bezpieczeństwa i kosztu. Znajomość zasady działania, parametrów oraz właściwego sposobu eksploatacji i utylizacji pozwala wydłużyć żywotność baterii i zmniejszyć wpływ na środowisko.