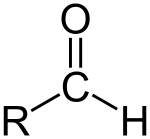
Aldehyd (/ˈældɪhaɪd/) jest związkiem organicznym zawierającym grupę formylową. Grupa ta jest częścią cząsteczki o ogólnej strukturze R‑CHO — atom węgla jest podwójnie związany z tlenem (C=O) i jednocześnie połączony z wodorem (C–H) oraz z łańcuchem bocznym R. Gdy zamiast łańcucha bocznego występuje tylko atom wodoru, mówimy o grupie aldehydowej lub formilowej. Aldehydy różnią się od ketonów tym, że grupa formylowa znajduje się na końcu cząsteczki — w ketonach grupę karbonylową łączy się z dwoma fragmentami węglowymi (R–CO–R).
Budowa i nazewnictwo
Generalny wzór aldehydu to R–CHO. Nazewnictwo systematyczne (IUPAC) kończy się sufiksem -al (np. metanal = formaldehyd, etanal = acetaldehyd). W praktyce często używa się także nazw zwyczajowych, np. formalina (roztwór formaldehydu), benzenaldehyd (benzaldehyd) — aromatyczny aldehyd odpowiedzialny za zapach migdałów.
Właściwości fizyczne
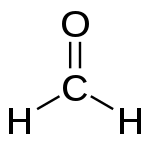
- Najprostszy aldehyd, metanal (H–CHO), jest gazem; aldehydy wyższe są cieczami lub ciałami stałymi o rosnących temperaturach wrzenia wraz ze wzrostem masy cząsteczkowej.
- Dzięki polarnej grupie karbonylowej mają zazwyczaj wyższą rozpuszczalność w wodzie niż węglowodory o podobnej masie (zwłaszcza niższe aldehydy).
- Wiele aldehydów ma intensywne zapachy — są składnikami perfum i aromatów (np. aldehydy alifatyczne i aromatyczne).
Właściwości chemiczne i reakcje charakterystyczne
Aldehydy są zazwyczaj bardziej reaktywne niż ketony ze względu na mniejszą steryczną ochronę karbonylu i mniejszy efekt elektronodonorowy ze strony podstawników R. Do najważniejszych reakcji należą:
- Nukleofilowe addycje do grupy karbonylowej — prowadzą do tworzenia hemiacetalów, hemiketali, alkoholi po redukcji itp.
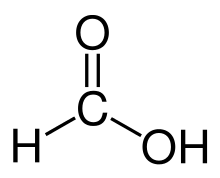
- Utlenianie — aldehydy łatwo utleniają się do kwasów karboksylowych (np. etanal → kwas octowy). To odróżnia je od większości ketonów (które są odporne na łagodne utlenianie).
- Redukcja — daje alkohole pierwszorzędowe (np. przy użyciu wodoru z katalizatorem lub reduktorów chemicznych jak NaBH4).
- Powstawanie imin (zasad Schiffa) — kondensacja z aminami pierwszorzędowymi tworzy iminę (C=N).
- Aldolizacja — aldehydy z alfa‑wodorem pod wpływem zasad tworzą produkty kondensacji aldolowej.
- Reakcja Cannizzaro — dysproporcjonowanie (utlenianie i redukcja) aldehydów bez wodoru alfa (np. benzaldehydu) w bardzo silnych zasadach, dające odpowiednio alkohol i kwas karboksylowy.
- Tworzenie acetali i hemiacetali — reakcje z alkoholami, ważne w ochronie grupy karbonylowej w syntezach organicznych.
Spektroskopia — jak rozpoznać aldehyd
- W widmie IR charakterystyczny pas w ok. 1720–1740 cm⁻¹ odpowiada grupie C=O; dodatkowo aldehydowy odcinek C–H daje słabe pasma około 2720–2820 cm⁻¹ (tzw. aldehydowe wibrujące C–H), co pomaga odróżnić aldehydy od ketonów.
- W 1H NMR proton aldehydowy występuje zwykle w obszarze 9–10 ppm jako singlet (lub nieco rozszczepiony), co jest bardzo charakterystyczne.
Otrzymywanie
Typowe metody przygotowania aldehydów to:
- Utlenianie odpowiednich alkoholów pierwszorzędowych (np. za pomocą PCC, K2Cr2O7, KMnO4 przy kontrolowanych warunkach) — w zależności od warunków można zatrzymać utlenianie na aldehydzie.
- Katalityczna dehydrogenacja alkoholi.
- Hydroformylacja (proces przemysłowy) — addycja CO i H2 do alkenów daje aldehydy (metodą Rohm‑Haas/oxo).
- Ozonoliza alkenów — rozszczepienie podwójnych wiązań może prowadzić do aldehydów (w zależności od stopnia utlenienia i warunków pracy).
- Specyficzne reakcje syntez: formylowanie, reakcje zylilowe i inne metody specjalistyczne w syntezie organicznej.
Zastosowania
Aldehydy mają szerokie zastosowanie w przemyśle chemicznym, farmaceutycznym i spożywczym:
- Składniki zapachów i aromatów — wiele aldehydów nadaje przyjemne nuty w perfumach i olejkach zapachowych.
- Produkcja żywic i tworzyw — np. formaldehyd używany do syntezy żywic fenolowych i mocznikowych (kleje, płyty wiórowe).
- Środki dezynfekcyjne i konserwanty — formaldehyd i jego pochodne były/ są stosowane jako środki bakteriostatyczne i utrwalające.
- Synteza leków i związków pośrednich — aldehydy są ważnymi reagentami w syntezach organicznych.
- Przemysł chemiczny jako surowce do dalszych przekształceń (np. tworzenie kwasów karboksylowych, alkoholi, amin).
Przykłady ważnych aldehydów
- Formaldehyd (metanal) — stosowany przemysłowo, jedna z najprostszych i najważniejszych substancji chemicznych.
- Acetaldehyd (etanal) — produkt utleniania etanolu, stosowany m.in. jako półprodukt syntez organicznych.
- Benzaldehyd — aromatyczny aldehyd o zapachu migdałów, wykorzystywany w aromatyce i syntezach.
Bezpieczeństwo i wpływ na zdrowie
Wiele aldehydów jest lotnych i drażniących dla dróg oddechowych. Szczególnie formaldehyd jest dobrze udokumentowanym czynnikiem toksycznym i klasyfikowany jest jako rakotwórczy dla ludzi; może powodować podrażnienia oczu, nosa, gardła oraz reakcje alergiczne. Przy pracy z aldehydami należy stosować odpowiednie środki ochrony (wentylacja, rękawice, okulary ochronne) i przestrzegać procedur postępowania z chemikaliami.
Podsumowanie
Aldehydy to grupa związków organicznych z charakterystyczną grupą formylową R–CHO. Są chemicznie aktywne i wszechstronne: łatwo ulegają reakcjom addycji i utleniania, mają istotne zastosowania przemysłowe (żywice, perfumy, syntezy chemiczne), ale wymagają ostrożnego obchodzenia się ze względu na właściwości toksyczne niektórych z nich (np. formaldehydu).