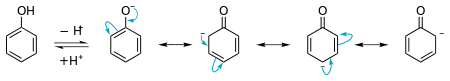Fenol jest związkiem organicznym o wzorze C6H5OH. Jest to zwykle białe, krystaliczne ciało stałe, które pod wpływem powietrza może zmieniać barwę na różową lub brązową wskutek utleniania. Posiada grupę OH (grupę hydroksylową) związaną z pierścieniem benzenowym. Fenol bywa klasyfikowany jako alkohol, jednak jego właściwości chemiczne różnią się od typowych alkoholi alifatycznych ze względu na sprzężenie z pierścieniem aromatycznym. Ponieważ grupa aromatyczna przyciąga elektrony i jednocześnie układ aromatyczny stabilizuje jon fenolanowy, związek ten jest stosunkowo kwaśny w porównaniu z alifatycznymi alkoholami. Fenol przemysłowo otrzymuje się głównie metodą kumenową z surowców naftowych, choć historycznie i nadal częściowo pozyskiwany jest z smoły węglowej; w produkcji wykorzystuje się surowce pochodzące z ropy naftowej. Jest to ważna cząsteczka, ponieważ stanowi surowiec do syntez wielu innych związków i materiałów. Stosowana jest również w detergentach i herbicydach, a także w produkcji tworzyw i produktów farmaceutycznych.
Wzór i budowa
Fenol ma wzór sumaryczny C6H5OH. Składa się z pierścienia benzenowego, do którego przyłączona jest grupa hydroksylowa. Elektrony układu aromatycznego współoddziałują z grupą –OH, co wpływa na właściwości kwasowo‑zasadowe i reaktywność pierścienia (np. ułatwiają podstawianie elektrofilowe w pozycjach orto i para).
Właściwości fizyczne
- Stan skupienia: białe, krystaliczne ciało stałe w temperaturze pokojowej (może przebarwiać się pod wpływem światła i powietrza).
- Temperatura topnienia: ~40,5 °C (stąd może być cieczą lekko powyżej tej temperatury).
- Temperatura wrzenia: ~181,7 °C.
- Gęstość: około 1,07 g/cm3 (w 20 °C).
- Rozpuszczalność: miesza się z wodą w ograniczonym stopniu; lepiej rozpuszcza się w rozpuszczalnikach organicznych. Tworzy stężone roztwory alkaliczne przy tworzeniu soli fenolanowych.
Właściwości chemiczne
- Kwasowość: fenol jest znacznie kwaśniejszy niż zwykłe alkohole; pKa ≈ 10 (w wodzie). Wynika to ze stabilizacji jonu fenolanowego przez rezonans.
- Reakcje podstawienia elektrofilowego: grupa –OH aktywuje pierścień i kieruje podstawianie głównie w pozycje orto i para (np. nitracja, bromowanie, sulfonowanie).
- Tworzenie soli i estrów: fenol reaguje z zasadami, tworząc fenolany (soli), oraz z kwasami (i ich pochodnymi) tworząc estry; z halogenkami alkilowymi powstają etery (alkilofenole).
- Utlenianie: fenole mogą być utleniane do chinonów lub innych produktów zależnie od warunków utleniania.
- Reakcje specyficzne: Kolbe‑Schmitt (karboksylacja fenolanów do kwasu salicylowego) jest ważną reakcją w syntezie związków farmaceutycznych (np. kwasu salicylowego).
Otrzymywanie
Główna metoda przemysłowa to proces kumenowy (Hocka): alkilacja benzenu propylem (powstaje kumen), który jest następnie utleniany do kumenowego nadtlenku i rozkładany do fenolu i acetonowego produktu ubocznego (aceton). W przeszłości fenol otrzymywano z smoły węglowej (produkt uboczny koksowania węgla). W warunkach laboratoryjnych można go otrzymać m.in. przez hydrolizę chlorku arylowego, oksydację cykloheksanolu/aminowania ze związków pochodnych czy przez wspomnianą reakcję Kolbe‑Schmitta z fenolanów.
Zastosowania
Fenol ma szeroki zakres zastosowań przemysłowych i laboratoryjnych. Najważniejsze z nich to:
- Produkcja żywic fenolowo‑formalnych (np. żywice fenolowe, znane jako bakelit) — stosowane do wyrobów izolacyjnych, elementów konstrukcyjnych i klejów.
- Synteza bisfenolu A (BPA) — surowiec do produkcji poliwęglanów i niektórych żywic epoksydowych.
- Produkcja prekursorów do tworzyw, barwników, dodatków do paliw, leków i pestycydów (m.in. niektóre herbicydy i intermedianty).
- Składnik niektórych detergentów (historycznie nonylofenole i pochodne), chociaż niektóre z nich są dziś ograniczane ze względu na toksyczność i działanie hormonalne.
- Użycie jako środek dezynfekujący i konserwujący w przeszłości (np. fenol był jednym z pierwszych środków antyseptycznych w chirurgii), choć ze względu na toksyczność stosowanie takie jest obecnie ograniczone.
Toksyczność i bezpieczeństwo
Fenol jest substancją toksyczną i żrącą. Może powodować oparzenia skóry i błon śluzowych, a wchłonięty przez skórę lub drogą pokarmową i oddechową wywoływać objawy ogólne (bóle głowy, zawroty, nudności, uszkodzenia wątroby i nerek, zaburzenia świadomości). Długotrwała ekspozycja oraz wdychanie oparów są niebezpieczne. Przy pracy z fenolem należy stosować odpowiednie środki ochrony osobistej: rękawice odporne na chemikalia, okulary ochronne, wentylację i odzież ochronną. W razie rozlania i kontaktu ze skórą zaleca się natychmiastowe spłukanie dużą ilością wody i usunięcie skażonej odzieży; w poważniejszych przypadkach konieczna jest pomoc medyczna.
Fenol jest również toksyczny dla organizmów wodnych — przed wprowadzeniem do środowiska przemysłowe odpady wymagają właściwej neutralizacji i oczyszczania.
Podsumowanie
Fenol (C6H5OH) to podstawowy surowiec chemiczny o licznych zastosowaniach przemysłowych, zwłaszcza w produkcji żywic, tworzyw i substancji pośrednich. Jego specyficzne właściwości wynikające z obecności grupy hydroksylowej sprzężonej z pierścieniem aromatycznym determinują zarówno przydatność w syntezach, jak i konieczność zachowania szczególnych środków ostrożności przy jego stosowaniu.