Węglowodory aromatyczne, często nazywane arenami, to grupa związków o charakterystycznej, pierścieniowej budowie. W sensie chemicznym są to związki węglowodorowe, w których atomy węgla łączą się w cykliczne układy z delokalizowanymi elektronami. Ich klasyczna reprezentacja pokazuje naprzemienne wiązania podwójne i pojedyncze, ale rzeczywisty rozkład elektronów jest lepiej opisany przez pojęcie aromatyczności i rezonansu, a nie prostą sekwencję wiązań wiązania. Nazwa „aromatyczne” historycznie wiązała się z wonią wielu wczesnych związków tej grupy.
Charakterystyka i zasada stabilizacji
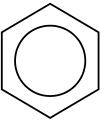
Podstawową cechą arenów jest stabilizacja aromatyczna związana z delokalizacją układu elektronów π nad pierścieniem. Typowy przykład to sześcioczłonowy pierścień benzenowy, reprezentowany przez benzen, którego szczególną własność opisuje reguła Hückla (liczba elektronów π odpowiada wzorowi 4n+2). Aromatyczność przejawia się w wyjątkowej trwałości związków, ich charakterystycznych widmach oraz w określonych przebiegach reakcji chemicznych.
Podziały i przykłady
- Monocykliczne areny — proste pierścienie, np. benzen, toluen.
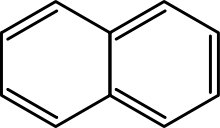
- Policykliczne węglowodory aromatyczne (PAH) — złożone układy pierścieniowe, np. naphalen, antracen.
- Heteroareny — pierścienie aromatyczne, w których co najmniej jeden atom węgla jest zastąpiony heteroatomem, na przykład tlen (tlen), azot (azot) lub siarka (siarka); przykłady to furan, pirydyna, tiofen.
Historia i rozwój pojęcia
Pojęcie aromatyczności wyrosło z badań nad związkami o wyraźnych zapachach, a struktura pierścienia benzenu została sformalizowana w XIX wieku. Rozwój teorii rezonansu i mechaniki kwantowej pozwolił na wyjaśnienie delokalizacji elektronów i sformułowanie kryteriów aromatyczności, co miało zasadnicze znaczenie dla rozwoju chemii organicznej i syntezy związków pochodnych.
Reakcje i zastosowania
Areny podlegają charakterystycznym przemianom, z których najważniejsze to substytucja elektrofilowa (np. nitrowanie, sulfonowanie, halogenowanie) oraz reakcje przyłączania w warunkach bardziej forsownych. W praktyce przemysłowej i laboratoryjnej związki aromatyczne służą jako rozpuszczalniki, surowce do produkcji tworzyw, barwników, leków i materiałów polimerowych. Policykliczne aromatyczne węglowodory występują także naturalnie w produktach spalania i w ropie naftowej.
Znaczenie środowiskowe i zdrowotne
Nie wszystkie areny są obojętne dla zdrowia: niektóre PAH są zanieczyszczeniami o właściwościach rakotwórczych i mogą być trwałe w środowisku. Z tego względu ważne są metody monitorowania emisji, oczyszczania środowiska i oceny narażenia. Jednocześnie wiele heteroarenów i pochodnych aromatycznych ma ogromne znaczenie farmaceutyczne oraz technologiczne, co sprawia, że zrozumienie ich właściwości pozostaje istotnym polem badań chemicznych.
Więcej informacji na temat podstawowego znaczenia i zastosowań można znaleźć w źródłach ogólnodostępnych oraz specjalistycznej literaturze chemicznej — dla ułatwienia odnośników umieszczono podstawowe linki tematyczne: definicje, budowa pierścieniowa, rodzaje wiązań, pierścień benzenowy, reguła Hückla, tlen, azot, siarka.