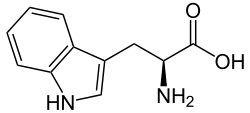
Tryptofan (Trp lub W) jest kodowany przez kodon UGG. Jest to α-aminokwas wykorzystywany w biosyntezie białek. Jest aminokwasem egzogennym dla ludzi — organizm nie potrafi go syntetyzować, dlatego musi być dostarczany z pożywieniem. W przeciwieństwie do ludzi, wiele bakterii, roślin i niektórych drożdży syntetyzuje tryptofan w szlaku szikimowym z pochodnych kwasu chorismowego.
Budowa i właściwości chemiczne
Tryptofan posiada grupę α-aminową (która w warunkach biologicznych występuje w formie -NH3+), oraz grupę α-karboksylową (która w warunkach biologicznych występuje w zdeprotonowanej formie -COO-). Posiada również łańcuch boczny indolowy, co czyni go niepolarnym aminokwasem aromatycznym. Boczne pierścienie indolowe nadają tryptofanowi właściwości hydrofobowe i umożliwiają uczestnictwo w oddziaływaniach π–π oraz strefach hydrofobowych białek. Z powodu obecności pierścienia indolowego tryptofan wykazuje silne fluorescencyjne właściwości (emisja przy ~320–350 nm), co jest wykorzystywane w badaniach struktury białek.
Wzór sumaryczny: C11H12N2O2; masa cząsteczkowa około 204,23 g/mol. Właściwości kwasowo-zasadowe (pKa) grup α decydują o jego jonizacji w pH fizjologicznym, w którym występuje w formie zjonizowanej.
Funkcje biologiczne
Tryptofan pełni kilka ważnych funkcji w organizmie:
- Składnik białek — wchodząc w skład łańcuchów polipeptydowych wpływa na strukturę i funkcję białek.
- Prekursor neurotransmiterów i hormonów: neuroprzekaźników: serotoniny i melatoniny. Synteza serotoniny odbywa się w dwóch etapach: hydroksylacja tryptofanu do 5-hydroksytryptofanu (5-HTP) przez tryptofan-hydroksylazę (enzym ograniczający tempo), a następnie dekarboksylacja do serotoniny przez aromatyczną L-aminokwasową dekarboksylazę (wymaga witaminy B6 jako kofaktora). Melatonina produkowana jest z serotoniny w szyszynce i reguluje rytmy okołodobowe.
- Szlak kinureninowy — większość spożytego tryptofanu metabolizowana jest do kinureniny i pochodnych. Z tego szlaku możliwa jest biosynteza niacyny (witamina B3), a także powstawanie metabolitów o działaniu neuroaktywnym (np. kwas kinureninowy o działaniu neuroprotekcyjnym i kwas chinolinowy/kwas quinolinowy o właściwościach neurotoksycznych). Aktywacja enzymów tego szlaku (np. indoloamina 2,3-dioksygenaza, IDO) może być indukowana przez stan zapalny i wpływa na dostępność tryptofanu do syntezy serotoniny.
- Regulacja układu odpornościowego — metabolity szlaku kinureninowego wpływają na odpowiedź immunologiczną i stan zapalny.
Transport do mózgu i znaczenie diety
Dostępność tryptofanu w mózgu zależy nie tylko od jego stężenia we krwi, lecz także od konkurencji o wspólny transporter przez barierę krew–mózg z innymi dużymi neutralnymi aminokwasami (LNAA: lizyna, leucyna, izoleucyna, walina, fenyloalanina, tyrozyna itd.). Dlatego spożycie posiłku bogatego w białko (z wieloma LNAA) może zmniejszać stosunek tryptofanu do pozostałych LNAA i ograniczać jego transport do mózgu. Spożycie węglowodanów stymuluje wydzielanie insuliny, co sprzyja wychwytowi konkurencyjnych aminokwasów przez mięśnie i względnemu wzrostowi stężenia wolnego tryptofanu we krwi — to wyjaśnia popularny mit o „uciążliwości po indyku”: zmęczenie po posiłkach bogatych w węglowodany powiązane jest raczej z metabolizmem glukozy i postprandialną sennością niż samym tryptofanem.
Źródła pokarmowe i zapotrzebowanie
Główne źródła tryptofanu w diecie to produkty białkowe: drób (np. indyk, kurczak), mięso czerwone, ryby, jaja, produkty mleczne, soja i jej przetwory, orzechy, nasiona (np. sezam, dynia), rośliny strączkowe, owies, czekolada i banany. Zrównoważona dieta bogata w białko zwykle dostarcza wystarczającą ilość tryptofanu.
Zalecane spożycie: dla dorosłych orientacyjne zapotrzebowanie wynosi około 4 mg tryptofanu na kg masy ciała dziennie (wartości orientacyjne — mogą się różnić w zależności od źródła i stanu fizjologicznego). Dla osoby ważącej 70 kg daje to w przybliżeniu 280 mg dziennie. W praktyce dostarczenie tej ilości jest zwykle możliwe w ramach typowej diety zawierającej odpowiednią ilość białka.
Niedobór, skutki i suplementacja
Niedobór tryptofanu może prowadzić do obniżonej syntezy serotoniny i melatoniny, co wiąże się z zaburzeniami nastroju, problemami ze snem i zmianami apetytu. Długotrwały i znaczny niedobór wpływa także na syntezę niacyny (witamina B3) i może przyczyniać się do wystąpienia objawów pelagry, zwłaszcza przy niedoborach współtowarzyszących witamin B6 i B2.
Suplementy tryptofanu (L-tryptofan) i prekursor 5-HTP są stosowane w celu wsparcia snu, nastroju lub łagodzenia objawów przedmiesiączkowych, ale dowody kliniczne są mieszane i wskazują na umiarkowany efekt w określonych sytuacjach. Należy pamiętać, że w przeszłości suplementy tryptofanu zostały powiązane z epidemią zespołu eozynofilii i bólu mięśniowego (EMS) na początku lat 90., co było związane z zanieczyszczeniem niektórych partii produktu — problem ten dotyczył głównie zanieczyszczeń produkcyjnych, nie samej substancji.
Interakcje i bezpieczeństwo
- Stosowanie tryptofanu lub 5-HTP jednocześnie z lekami zwiększającymi poziom serotoniny (np. SSRI, SNRI, trójpierścieniowymi antydepresantami, MAO inhibitorami) może zwiększać ryzyko zespołu serotoninowego — potencjalnie poważnego stanu. Dlatego łączenie suplementów z lekami przeciwdepresyjnymi powinno się odbywać wyłącznie pod kontrolą lekarza.
- Osoby w ciąży, karmiące piersią, z chorobami przewlekłymi lub przyjmujące leki powinny konsultować stosowanie suplementów z lekarzem.
- Umiarkowana suplementacja krótkotrwała bywa bezpieczna u zdrowych osób, ale nie zastępuje zrównoważonej diety. Przyjmowanie dużych dawek bez nadzoru może powodować działania niepożądane (nudności, zawroty głowy, senność) i wymaga ostrożności.
Zastosowania w badaniach i diagnostyce
Tryptofan i jego spektroskopowe właściwości (fluorescencja) są szeroko wykorzystywane w badaniach struktury i dynamiki białek. Analiza metabolitów tryptofanu (np. kinureniny) stosowana jest też w badaniach nad stanem zapalnym, zaburzeniami nastroju i chorobami neurologicznymi.
Podsumowując, tryptofan to kluczowy aminokwas niezbędny w diecie, ważny nie tylko jako składnik białek, lecz także jako prekursor serotoniny, melatoniny i niacyny oraz szeregu metabolitów o istotnych funkcjach biologicznych. Zrównoważona dieta i uwzględnienie potencjalnych interakcji lekowych są podstawą bezpiecznego korzystania z jego korzyści.