Ten artykuł jest tylko o chemii alkoholi.
Alkohol stosowany w drinkach to etanol; więcej informacji można znaleźć na stronie: picie alkoholu i alkoholizm.
W chemii, alkohol jest ogólnym terminem, który odnosi się do wielu związków organicznych stosowanych w przemyśle i nauce jako odczynniki, rozpuszczalniki i paliwa. Alkohole są węglowodanami, które składają się z grupy alkilowej z jedną lub więcej grup hydroksylowych (-OH) związanych z atomami węgla. Alkohol jest bezbarwny, a także przezroczysty.
Uwaga terminologiczna: w przytoczonym fragmencie pojawia się link węglowodanami, co może sugerować, że alkohole to to samo co węglowodany — to nieprecyzyjne. Alkohole to ogólna klasa związków organicznych zawierających grupę hydroksylową (-OH) związaną z atomem węgla. Węglowodany (cukry) również zawierają grupy –OH, ale stanowią odrębną klasę związków biologicznych.
Definicja i wzór ogólny
W chemii organicznej alkohol to związek zawierający jedną lub więcej grup hydroksylowych (-OH) bezpośrednio przyłączonych do atomu węgla alifatycznego lub benzylicznego. Ogólny wzór dla alkoholów alifatycznych monosubstytuowanych to R–OH, gdzie R oznacza grupę alkilową (np. CH3–, C2H5–).
Podział i rodzaje alkoholów
- Ze względu na rodzaj atomu węgla związanego z –OH:
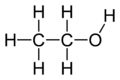
- Alkohole pierwszorzędowe (1°) – grupa –OH przy atomie węgla związanym z jednym innym atomem węgla (np. etanol, CH3CH2OH).
- Alkohole drugorzędowe (2°) – –OH przy atomie węgla związanym z dwoma atomami węgla (np. izopropanol, (CH3)2CHOH).
- Alkohole trzeciorzędowe (3°) – –OH przy atomie węgla związanym z trzema atomami węgla (np. tert-butanol).
- Ze względu na liczbę grup hydroksylowych:
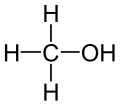
- Monohydroksylowe (jedna grupa –OH): np. metanol, etanol.
- Diole (glikole) – dwie grupy –OH: np. etylenoglikol (C2H6O2).
- Triole – trzy grupy –OH: np. glicerol (C3H8O3).
- Poliole (wiele grup –OH) – np. cukry zawierające liczne grupy hydroksylowe.
- Alkohole aromatyczne i fenole: jeśli grupa –OH jest przyłączona do pierścienia aromatycznego (np. fenol), związek wykazuje inne właściwości; fenole są zwykle klasyfikowane oddzielnie od alkoholi alifatycznych ze względu na zwiększoną kwasowość i specyficzne reakcje.
- Alkohole benzyliczne: –OH przy atomie węgla bezpośrednio związanym z pierścieniem benzenowym (np. benzylowy alkohol), mające często charakterystyczne właściwości reakcyjne.
Przykłady najważniejszych alkoholi
- Metanol (CH3OH) – rozpuszczalnik, surowiec chemiczny, paliwo; bardzo toksyczny po spożyciu.
- Ethanol (C2H5OH) – alkohol spożywczy, rozpuszczalnik, paliwo (etanolowy); umiarkowana toksyczność przy spożyciu.
- Propanol (n‑propanol, izopropanol) – rozpuszczalniki, środki dezynfekcyjne (izopropanol).
- Etylenoglikol (HO–CH2CH2–OH) – płyny chłodnicze/antyfryzy; toksyczny przy spożyciu.
- Glicerol (C3H8O3) – kosmetyki, farmaceutyki, środki przeciwzamrożeniowe, surowiec do syntez.
Właściwości fizyczne
- Więzi wodorowe: obecność grup –OH umożliwia powstawanie wiązań wodorowych, co podwyższa temperatury wrzenia i topnienia w porównaniu do węglowodorów o podobnej masie cząsteczkowej.
- Rozpuszczalność: małe alkohole (metanol, etanol) są dobrze rozpuszczalne w wodzie dzięki wiązaniom wodorowym; rozpuszczalność maleje wraz ze wzrostem łańcucha węglowego.
- Barwa i stan skupienia: wiele prostych alkoholi to bezbarwne, przezroczyste ciecze, chociaż cięższe alkohole mogą być oleiste lub stałe w 20 °C.
- Kwasowość: alkohole są słabymi kwasami (pKa typowych alifatycznych ok. 16–18); fenole są znacznie silniejszymi kwasami (pKa ok. 10).
Reakcje charakterystyczne
- Esterifikacja z kwasami karboksylowymi (np. tworzenie estrów w obecności kwasu brończącego).
- Oksydacja: alkohole 1° → aldehydy → kwasy karboksylowe; alkohole 2° → ketony; alkohole 3° są oporne na łatwą oksydację bez zerwania wiązania C–C.
- Dehydratacja (odwodnienie) do alkenów w obecności katalizatorów kwasowych.
- Substytucje nukleofilowe – przekształcanie alkoholi w lepsze grupy opuszczające (np. halogenki alkilowe) po aktywacji (np. przez protonację lub użycie reagentów typu SOCl2).
- Tworzenie eterów (reakcje Williamsona) – reakcja alkoksylu z halogenkiem alkilowym.
- Reakcje z reagentami alkalicznymi – utworzenie alkoksydów (RO–) po deprotonacji silnymi zasadami.
Metody otrzymywania
- Hydratacja alkenów (kataliza kwasowa lub hydroboracja‑oksydacja dla odwrotnej selektywności).
- Redukcja związków karbonylowych (aldehydów i ketonów) za pomocą reduktorów (NaBH4, LiAlH4).
- Reakcje Grignarda z formaldehydem, aldehydami i ketonami do otrzymywania alkoholów po hydroksylowaniu.
- Fermentacja bioorganiczna (etanol z cukrów przez drożdże).
- Hydroliza etyleno tlenków do glikolów (np. etylenoksyd → etylenoglikol).
Zastosowania
- Przemysł chemiczny: rozpuszczalniki (metanol, etanol, izopropanol), surowce do syntez (np. produkcja estrów, eterów, surfaktantów).
- Paliwa i dodatki: metanol i etanol jako paliwa lub dodatki do benzyny (bioetanol).
- Przemysł farmaceutyczny i kosmetyczny: glicerol jako emolient, alkohole jako rozpuszczalniki i składniki preparatów kosmetycznych.
- Środki dezynfekcyjne: etanol i izopropanol stosowane do dezynfekcji powierzchni i skóry.
- Antyfryzy i płyny chłodnicze: etylenoglikol, propylene glycol (mniej toksyczny odpowiednik) – dodatek do płynów chłodniczych.
- Przemysł spożywczy: etanol – napoje alkoholowe; ponadto alkohole jako rozpuszczalniki w ekstrakcji i aromatach.
Bezpieczeństwo i wpływ na zdrowie
- Alkohole są łatwopalne; przechowywać z dala od źródeł zapłonu.
- Toksyczność: metanol jest silnie toksyczny (uszkodzenie wzroku, śmierć) po spożyciu; etanol działa depresyjnie na ośrodkowy układ nerwowy; niektóre glikole są nefrotoksyczne.
- Wdychanie oparów i kontakt ze skórą wymaga odpowiednich środków ochrony osobistej – w miejscu pracy stosuje się wentylację i rękawice.
- Mieszaniny z wodą i innymi rozpuszczalnikami wymagają właściwego postępowania środowiskowego przy utylizacji.
Krótka notka nomenklaturowa
W nazewnictwie IUPAC końcówka „-ol” oznacza alkohol (np. etanol = ethan‑1‑ol). W nazwach zwyczajowych występują też nazwy powszechne (metanol = alkohol metylowy, etanol = alkohol etylowy).
Alkohole stanowią szeroką i ważną klasę związków organicznych — zarówno w syntezach chemicznych, jak i w zastosowaniach przemysłowych, farmaceutycznych i codziennych. Dla dalszego zgłębienia tematu warto zapoznać się z literaturą chemiczną dotyczącą mechanizmów reakcji, metod analitycznych i specyficznych zastosowań przemysłowych.