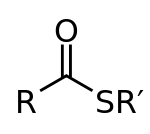
Tioester to cząsteczka z grupą C-S-CO-C. Są one podobne do estrów, ale z atomem siarki zamiast tlenu. Podobnie jak estry, można je otrzymać z kwasów karboksylowych. W syntezie zamiast alkoholu używany jest tiol.
Tioestry są bardzo ważne w biochemii. Są one wytwarzane w organizmie podczas reakcji, w których powstają kwasy tłuszczowe. Są one również ważnymi intermediatami w produkcji ATP, który jest cząsteczką dającą energię organizmowi.
W chemii, tioestry mogą być również używane jako elektrofil. Są one bardziej reaktywne niż estry i amidy. Mogą również przeprowadzać reakcje aldolowe.
Budowa i właściwości chemiczne
Tioestry mają ogólny wzór R–C(=O)–S–R'. W porównaniu z tlenowymi estrami mniejsza elektroujemność i większy promień atomu siarki powodują, że rezonansowe sprzężenie między grupą karbonylową a heteroatomem jest słabsze. W praktyce oznacza to, że w tioestrach wiązanie C=O jest bardziej elektrofilowe — łatwiej przyjmować nukleofile — dlatego tioestry są zazwyczaj bardziej reaktywne wobec podstawienia nukleofilowego niż odpowiednie estry.
Siarka jako heteroatom wpływa też na stabilność i właściwości fizykochemiczne: tioestry są zwykle mniej trwałe w wodzie niż estry, mają inne przesunięcia w widmach IR i NMR oraz różne właściwości rozpuszczalności.
Reaktywność i mechanizmy
- Nukleofilowe podstawienie acylowe: podobnie jak estry, tioestry ulegają nukleofilowej substytucji przy węglu karbonylowym. Dzięki słabszemu sprzężeniu siarki reakcje te przebiegają zwykle szybciej.
- Trans-tioestryfikacja: łatwe przenoszenie reszt acylowych między tiolami — reakcja wykorzystywana w syntezie i w enzymatycznych procesach przenoszenia acyli.
- Formowanie enolatów / kondensacje: tioestry mają aktywne protony alfa i mogą tworzyć enolaty, co czyni je dobrymi substratami do kondensacji typu Claisena oraz innych reakcji w syntezie węglowo-węglowej.
- Hydroliza: enzymatyczna (np. przez tioesterazy) lub chemiczna hydroliza prowadzi do kwasów karboksylowych i tioli; hydroliza tioestrów uwalnia zwykle więcej energii niż hydroliza odpowiednich estrów tlenu.
Przygotowanie tioestrów
W praktyce laboratoryjnej tioestry przygotowuje się na kilka sposobów:
- aktywacja kwasu (np. przekształcenie do chlorku kwasowego), a następnie reakcja z tiolem,
- użycie środków sprzęgających (DCC, EDC) do kondensacji kwasu z tiolem,
- transestryfikacja z innych tioestrów lub z aktywowanych pochodnych acylowych.
Rola w biochemii
Tioestry odgrywają kluczowe role w metabolizmie:
- Acetyl-CoA i inne acylo-CoA: Acetyl-CoA to tioester pomiędzy grupą acetylową a CoA; jest centralnym metabolitem łączącym szlaki kataboliczne i anaboliczne. Hydrolyza tioestru acetyl-CoA oraz przeniesienie reszty acetylowej na inne akceptory napędzają wiele reakcji biosyntetycznych.
- Synteza kwasów tłuszczowych: w łańcuchu syntezy kwasów tłuszczowych pośrednikami są tioestry związane z białkiem nośnikowym (ACP) lub CoA (np. malonyl-ACP, acetyl-ACP). Kondensacje enzymatyczne (dekarboksylacyjne kondensacje typu Claisena) korzystają z właściwości tioestrów jako dobrych donorów acylowych.
- Przenoszenie acyli w enzymach: wiele transferaz wykorzystuje pośrednie tworzenie tioestrów (np. podczas aktywacji kwasów przez acyl-CoA syntetazy).
- Modyfikacje białek: S-palmitoilacja (wiązanie kwasu palmitynowego do reszt cysteiny) zachodzi przez tworzenie thioestrów i jest ważna dla lokalizacji i funkcji białek w błonach.
- Mechanizmy aktywacji wewnątrz komórki: podczas aktywacji ubikwityny i innych procesów tworzą się przejściowe tioestry z resztami cysteiny enzymów (np. w enzymach E1 w szlaku ubikwityny).
Zastosowania w syntezie i biotechnologii
Tioestry są szeroko wykorzystywane w chemii organicznej i biorzemie:
- jako aktywne pochodne do przenoszenia grup acylowych,
- w syntezie peptydów — native chemical ligation wykorzystuje C-końcowe tioestry peptydów do tworzenia wiązań peptydowych w warunkach łagodnych,
- w syntezie naturalnych produktów i katalizie asymetrycznej jako aktywne substraty do kondensacji.
Enzymy rozkładające i przetwarzające tioestry
W komórkach istnieją specyficzne enzymy, które rozpoznają i rozkładają tioestry — tioesterazy i różne hydrolazy acylo-CoA. Enzymy te kontrolują przebieg syntez kwasów tłuszczowych, detoksykację i regulują dostępność wysokoenergetycznych acyli.
Podsumowanie
Tioestry to istotna klasa związków o specyficznej budowie i podwyższonej reaktywności w porównaniu z estrami tlenu. Ich właściwości wynikające z obecności siarki czynią je nieocenionymi w procesach biochemicznych (np. acylowanie, synteza i rozkład kwasów tłuszczowych, transport grup acylowych) oraz w zastosowaniach syntetycznych, zwłaszcza tam, gdzie potrzebne są aktywne i łatwo przekształcalne pochodne acylowe.