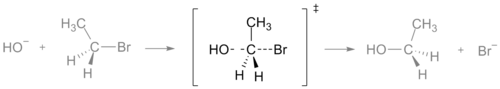W reakcji chemicznej stan przejściowy (ang. transition state) to punkt na ścieżce reakcji o maksymalnej energii — moment, gdy toczą się procesy jednoczesnego tworzenia i zrywania wiązań. Energia potrzebna, aby osiągnąć ten punkt, to energia aktywacji (najczęściej oznaczana jako E_a lub ΔG‡, gdy mówimy o energii swobodnej). Na wykresie energetycznym stanu przejściowego używa się często symbolu podwójnego sztyletu ‡.
Jak zachowuje się cząsteczka w stanie przejściowym
Gdy dwie lub więcej cząsteczek zostanie zmieszanych i zderzą się, muszą posiadać wystarczającą energię, aby „przeskoczyć” barierę energetyczną i przejść przez stan przejściowy — w przeciwnym razie zderzenie nie prowadzi do reakcji. W stanie przejściowym tworzą się częściowe (przejściowe) formy nowych wiązań i jednocześnie zrywają się stare wiązania. Jest to stan niestabilny i krótkotrwały: cząsteczki spędzają w nim zwykle czasy rzędu femtosekund (10^-15 s), dlatego stan przejściowy nie może być wyizolowany ani bezpośrednio „złapany”.
Różnica między stanem przejściowym a intermediatem
Ważne jest, aby nie mylić stanów przejściowych z intermediatami. Intermediaty (stany pośrednie) znajdują się w minimach energetycznych na ścieżce reakcji, mają względną stabilność i mogą istnieć przez znacznie dłuższy czas niż stany przejściowe — czasami są na tyle trwałe, że można je wykryć lub wyizolować. Obie formy leżą pomiędzy reagentami i produktami, ale różnią się pozycją na wykresie energetycznym oraz czasem trwania.
Znaczenie i zastosowania
Badanie stanów przejściowych jest kluczowe dla zrozumienia mechanizmów reakcji i przewidywania szybkości reakcji. Informacje o strukturze i energii stanu przejściowego pozwalają:
- obliczyć stałe szybkości reakcji (przez związki z teorią przejścia oraz równaniami Arrheniusa i Eyringa),
- projektować katalizatory — katalizatory przyspieszają reakcję głównie poprzez obniżenie energii aktywacji, czyli stabilizację stanu przejściowego,
- rozumieć efekty izotopowe i stereochemiczne (np. dlaczego niektóre ścieżki prowadzą do określonych produktów),
- optymalizować warunki procesu w syntezie chemicznej i w przemyśle.
Jak bada się stany przejściowe
Bezpośrednie obserwowanie stanu przejściowego jest trudne z powodu jego krótkotrwałości, ale istnieją eksperymentalne i obliczeniowe metody pozwalające poznać jego własności:
- Techniki eksperymentalne: spektroskopia femtosekundowa (femtochemia), pomiary szybkości reakcji i efektów izotopowych, przejściowe spektroskopy (time-resolved methods) — metody te pozwalają pośrednio badać dynamikę i wskazywać właściwości przejściowe.
- Metody obliczeniowe: obliczenia kwantowo-chemiczne (ab initio, DFT), optymalizacja struktur przejściowych, obliczenia energii i ścieżki reakcji (np. Intrinsic Reaction Coordinate, IRC). Programy komputerowe pozwalają wyznaczyć strukturę stanu przejściowego, jego energię oraz częstość drgań z jednym ujemnym kierunkiem (tzw. jedną „imaginary frequency”), co potwierdza, że znaleziono rzeczywiście punkt siodłowy.
Teorie i reguły pomocnicze
W opisie stanów przejściowych używa się kilku pojęć i przybliżeń, z których praktyczne znaczenie mają m.in.:
- Teoria przejścia (Transition State Theory) — matematyczna rama łącząca strukturę stanu przejściowego z szybkością reakcji.
- Postulat Hammonda — mówi, że struktura stanu przejściowego przypomina najbardziej tę stronę reakcji (reagentów lub produktów), do której jest bliżej energetycznie; pomaga to przewidywać kształt TS w reakcjach egzo- i endoenergetycznych.
Przykład
Typowym przykładem ilustrującym stan przejściowy jest reakcja SN2 (substytucja nukleofilowa jednoczynnikowa), gdzie w stanie przejściowym atom centralny ma częściowo utworzone wiązanie z nukleofilem i częściowo z odchodzącą grupą — tworzy się tzw. kompleks pentagonalny (w uproszczeniu: więź „przechodnia”). Taki TS ma symetrię i geometryczne cechy wynikające z jednoczesnego rozrywania i tworzenia wiązań.
Podsumowanie
Stan przejściowy to krótkotrwały punkt o najwyższej energii na ścieżce reakcji, kluczowy dla określenia szybkości i mechanizmu reakcji. Choć bezpośrednio nieuchwytny, jego właściwości można odtwarzać i analizować za pomocą zaawansowanych technik eksperymentalnych i obliczeniowych — wiedza ta jest fundamentem kinetyki chemicznej oraz projektowania katalizatorów i procesów syntez organicznych i przemysłowych. Zawiera on zarówno aspekty energetyczne (energia aktywacji), jak i strukturalne (cząstkowe tworzenie i zrywanie wiązania), a symbolicznie oznacza się go znakiem ‡.