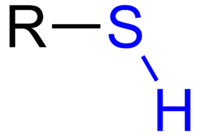
Tiol to cząsteczka, która posiada grupę R-SH. Tiole są jak alkohole z atomem tlenu zamienionym na atom siarki. Często mają one bardzo silny i nieprzyjemny zapach. Tiole są dodawane do gazu ziemnego, aby ludzie mogli go poczuć. Dzieje się tak dlatego, że metan nie ma zapachu, ale może bardzo łatwo eksplodować.
Tiole są bardzo łatwe do utlenienia. Są też dość kwaśne, bardziej niż alkohole. Gdy proton zostanie zabrany przez zasadę, tiol może stać się nukleofilem. Może przeprowadzać reakcje takie jak substytucja nukleofilowa.
Jeden z naturalnych aminokwasów, cysteina, posiada w swojej strukturze tiol.
Właściwości chemiczne
Kwaśność i zasadowość: Tiole są na ogół znacznie bardziej kwaśne niż odpowiadające im alkohole — typowe pKa alifatycznych tioli wynoszą około 10–11, podczas gdy alkohole mają pKa rzędu ~16–18. Oznacza to, że łatwiej tworzą aniony (tzw. tiolany lub tiolaty, R–S−) po oddaniu protonu.
Utlenianie i tworzenie disiarczków: Dwa cząsteczki tiolu łatwo ulegają utlenieniu do disiarczku (R–S–S–R). To proste utlenianie jest kluczowe w chemii i biologii — w białkach mostki dwusiarczkowe między dwiema grupami tiolowymi cysteiny stabilizują strukturę trzeciorzędową białek. Silniejsze utleniacze mogą dalej utleniać siarkę do form sulfenowych, sulfinowych i sulfonowych.
Nukleofilowość i reakcje: Aniony tiolanowe są silnymi i „miękkimi” nukleofilami (w kontekście teorii HSAB), co sprawia, że chętnie reagują z elektrofiliami miękkimi (np. związki siarki, niektóre halogenki alkilowe). Tiole biorą udział w reakcjach takich jak alkilacja (powstawanie tioeterów R–S–R'), substytucje nukleofilowe, reakcje addycji typu thiol–ene (radikalna addycja do wiązań C=C) oraz tworzenie kompleksów z metalami.
Zapach i zastosowania jako odoranty
Charakter zapachu: Wiele tioli ma bardzo intensywny, często opisany jako „gnilny”, „zgniłej kapusty” lub „sierści/papierosowy” zapach. Substancje te mają bardzo niskie progi wyczuwalności — wykrywane są już w bardzo niskich stężeniach (często na poziomie ppb), dlatego są używane do ostrzegania o wyciekach gazu.
Przykłady stosowanych odorantów: Do dodawania zapachu do gazu ziemnego i LPG używa się kilku związków siarkowych, np. etantiol (ethanethiol), tert-butylthiol (tzw. TBM) lub tetrahydrothiophene (THT). Dzięki bardzo niskim progom zapachowym nawet niewielkie ilości tych związków umożliwiają wykrycie nieszczelności.
Rola w biologii
Cysteina i glutathion: Grupa tiolowa cysteiny występuje w białkach i pełni kluczowe funkcje: tworzy mostki disiarczkowe, bierze udział w katalizie enzymatycznej (np. w enzymach z dwusiarczkiem reaktywnym), oraz w reakcjach redoks w komórce. Glutation (tripeptyd zawierający cysteinę) jest głównym wewnątrzkomórkowym antyoksydantem — redukuje disiarczki i chroni przed stresem oksydacyjnym.
Metal‑binding: Atomy siarki z grup tiolowych są efektywnymi donorami elektronów do jonów metali (np. Zn2+, Fe2+/Fe3+), co wykorzystują m.in. domeny „zinc finger”.
Zastosowania techniczne i laboratoryjne
- Przemysł petrochemiczny: odorowanie gazów, kontrola jakości zapachu.
- Chemia organiczna: tworzenie tioeterów, użycie tioli jako reagentów w syntezach, reakcjach typu thiol–ene, oraz jako ligandów w kompleksach metali.
- Biochemia i medycyna: badanie mostków disiarczkowych, redukcja/utlenianie białek, zastosowania w molekularnych sensorach i biokatalizie.
- Przemysł polimerowy i gumowy: związki siarkowe biorą udział w procesach utwardzania i modyfikacji polimerów.
Bezpieczeństwo i charakter użytkowania
Tiole są często palne, mogą być toksyczne i drażnią drogi oddechowe. Ze względu na silny zapach, niskie stężenia bywają bardzo uciążliwe. W pracy laboratoryjnej i przemysłowej zaleca się używanie odciągów, dobrej wentylacji, odpowiednich rękawic i przechowywanie w szczelnych pojemnikach. W przypadku silnego zapachu i podejrzenia wycieku gazu — stosuje się procedury awaryjne określone przez operatora sieci gazowej.
Przykłady związków i ciekawostki
Przykładowe tioli to metantiol (CH3SH, metylo‑mercaptan), etantiol (C2H5SH), benzylotiol (C6H5CH2SH). Metantiol powstaje m.in. podczas rozkładu niektórych amin i jest odpowiedzialny za zapach zgniłej kapusty lub zgnilizny w pewnych produktach spożywczych. Nazwa „merkaptan” (ang. mercaptan) historycznie wiąże się z dużym powinowactwem tych związków do soli rtęci (łac. mercurium captans = „chwytający rtęć”).
Podsumowując, tiol (grupa R–SH) to wszechstronna grupa funkcyjna: łatwo ulega utlenieniu, ma charakterystyczny silny zapach wykorzystywany praktycznie jako środek ostrzegawczy w gazach palnych, odgrywa kluczowe role w chemii organicznej i biologii oraz wymaga ostrożnego obchodzenia się ze względu na toksyczność i palność.