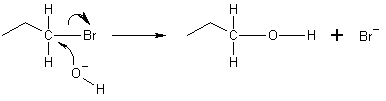
Nukleofil to gatunek, który oddaje parę elektronową elektrofilowi w celu utworzenia wiązania chemicznego w reakcji. Mogą to być jony ujemne (np. OH−, CN−, I−) lub związki neutralne posiadające parę elektronów (np. NH3, H2O). Taka para elektronów nazywana jest parą samotną. Ponieważ nukleofile oddają elektrony, pasują one do definicji zasad Lewisa — są to zatem typowe donory par elektronowych.
Czym jest nukleofilowość?
Nukleofilowość opisuje tendencję nukleofila do atakowania ośrodka elektronowo ubogiego (jądra atomowego lub atomu o częściowo dodatnim ładunku). Często określana jest także jako siła nukleofilu i służy do porównywania zdolności różnych substancji do oddawania pary elektronowej w warunkach kinetycznych (szybkość reakcji), niekoniecznie odpowiadając dokładnie ich zasadowości termodynamicznej.
Czynniki wpływające na nukleofilowość
- Ładunek: aniony zwykle są silniejszymi nukleofilami niż ich odpowiedniki neutralne (np. OH− > H2O).
- Elektroujemność: im niższa elektroujemność atomu donorowego, tym silniejszy nukleofil (przy podobnej polarności wiązania).
- Polarizowalność: duża polarizowalność (łatwość przesunięcia chmury elektronowej) zwiększa nukleofilowość, szczególnie w rozpuszczalnikach proticznych (np. I− jest lepszym nukleofilem niż F− w rozpuszczalnikach proticznych).
- Steryczne utrudnienie: duże podstawienie wokół atomu donorowego zmniejsza dostępność pary elektronowej i obniża nukleofilowość (tzw. efekt steryczny).
- Rozpuszczalnik: w rozpuszczalnikach aprotycznych małe, silnie naładowane aniony (np. F−) pozostają bardzo reaktywne, podczas gdy w rozpuszczalnikach proticznych są silnie solvowane i stają się słabszymi nukleofilami.
Mechanizmy reakcji nukleofilowych
Nukleofile biorą udział w różnych typach reakcji, z których najważniejsze to:
- Substytucja nukleofilowa bimolekularna (SN2) — jednoczesne atakowanie nukleofila i odłączenie grupy opuszczającej; kinetycznie zależna od stężeń substratu i nukleofila. Nukleofilowość ma duże znaczenie dla szybkości reakcji SN2.
- Substytucja nukleofilowa unimolekularna (SN1) — najpierw tworzy się karbokation (etap wolnorozpuszczalny), następnie następuje atak nukleofila; szybkość zależy głównie od tworzenia karbokationu, więc siła nukleofila ma mniejsze znaczenie.
- Solwoliza — to szczególny przypadek reakcji, gdy rozpuszczalnik (np. alkohole, woda) sam działa jako nukleofil; neutralne reakcje nukleofilowe z rozpuszczalnikami nazywane są solwolizą.
- Atak nukleofilowy na wiązania wielokrotne i układy koniugatowe — nukleofile mogą również reagować z wiązaniami pi (np. addycja do alkenów lub układów karbonylowych), a także uczestniczyć w reakcjach kondensacji i tworzeniu enoli/ enolanów.
Przykłady i rodzaje nukleofili
- Typowe anionowe nukleofile: OH−, OR−, CN−, RS−, I−, Br−.
- Typowe neutralne nukleofile: NH3, RNH2, H2O, alkohole.
- Nukleofile ambidentne: jony takie jak CN− (atak przez atom węgla lub azotu), enolaty (atak przez tlen lub węgiel) — wybór miejsca ataku zależy od warunków reakcji.
- Układy pi jako nukleofile: aromatyczne pierścienie i alkeny mogą działać jako nukleofile w reakcjach podstawienia elektrofilowego lub addycji.
Rozpuszczalnik i jego rola
Rozpuszczalnik wpływa silnie na nukleofilowość przez solvację jonów. W rozpuszczalnikach proticznych (np. alkohol, woda) małe, silnie naładowane aniony są mocno solvowane i osłabione jako nukleofile. W rozpuszczalnikach aprotycznych (np. DMSO, DMF) solvacja anionów jest słabsza, co zwykle zwiększa ich reaktywność nukleofilową.
Nukleofilowość a zasadowość
Choć nukleofilowość i zasadowość są powiązane (oba zależą od dostępności pary elektronowej), nie są pojęciami tożsamymi. Zasadowość odnosi się do termodynamicznej tendencji do przyjmowania protonu, podczas gdy nukleofilowość opisuje kinetyczną zdolność do ataku na centrum elektronowo ubogie. Przykładowo, F− jest silną zasadą, ale w rozpuszczalnikach proticznych może być słabszym nukleofilem niż I− ze względu na silną solvację.
Znaczenie grup opuszczających
W reakcjach substytucji nukleofilowej ważna jest obecność dobrej grupy opuszczającej (np. I−, Br−, TsO−). Słaba grupa opuszczająca utrudnia odłączenie i może zmieniać mechanizm reakcji (np. sprzyjać SN1 przez stabilizację karbokationu).
Praktyczne uwagi
- W planowaniu syntezy chemicznej dobór nukleofila, rozpuszczalnika i grupy opuszczającej jest kluczowy dla uzyskania pożądanego produktu i kontroli mechanizmu reakcji.
- Wybór nukleofila wpływa nie tylko na szybkość, ale i na regio- czy stereoizomerię produktu (np. SN2 prowadzi do inwersji konfiguracji przy centrum stereogenicznym).
- Ambidentne nukleofile i polifunkcyjne związki wymagają szczególnej uwagi — warunki reakcji (temperatura, rozpuszczalnik, kationy obecne) często decydują, które miejsce zaatakuje.
Nukleofile odgrywają kluczową rolę w chemii organicznej i nieorganicznej — zarówno w reakcjach laboratoryjnych, jak i procesach biologicznych. Zrozumienie czynników wpływających na ich zachowanie pozwala przewidywać przebieg reakcji i optymalizować warunki syntez.