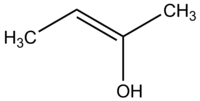
Enol jest alkenem, który ma grupę OH przyłączoną do jednego końca wiązania podwójnego. W postaci zasadowej, po odjęciu protonu z atomu tlenu, powstaje odpowiadający mu enolan (anion oksyglikolowy), często nazywany też enolanem metalicznym w obecności kationu metalu.
Tautomeria enol–keton (aldehyd)
Enole są tautomeriami ketonów lub aldehydów. Tautomery to cząsteczki, które różnią się jedynie położeniem atomu wodoru. Enole i odpowiadające im keto-formy tworzą zwykle dynamiczną równowagę, w której zazwyczaj preferowana jest forma keto, ponieważ wiązanie C=O jest energetycznie korzystniejsze niż wiązanie C=C z grupą OH. Wyjątki od tej reguły występują, gdy enol jest dodatkowo stabilizowany np. przez sprzężenie z układem aromatycznym lub przez silne wiązania wodorowe (przykład: enol acetylacetonu).
Powstawanie enoli i enolanów
Enole i enolany można otrzymać różnymi drogami:
- kataliza kwasowa — przemiana keto → enol przez protonowanie grupy karbonylowej i przeniesienie protonu na atom alfa,
- kataliza zasadowa — odjęcie protonu alfa przez zasadę tworzy enolan; typowe zasady to alkoksy, stericzne zasady niezbędne do kontroli selektywności,
- bezpośrednia deprotonacja silnymi, nieprotonującymi zasadami (np. LDA) daje izolowalne enolany metaloorganiczne,
- powstawanie enoli można także „zatrzymać” przez przemianę do imin lub enamin (przez reakcję z aminami) lub przez utworzenie enolowych pochodnych, np. sililowych eterów enolowych (silyl enol ethers).
Enole można bardzo łatwo otrzymać z ketonów lub aldehydów za pomocą zasady. W praktyce wybór metody i warunków decyduje o kierunku i selektywności enolizacji.
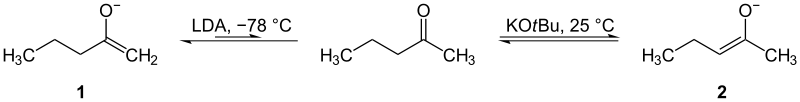
Enolan kinetyczny i termodynamiczny
Enole z ketonów mogą być wytwarzane z dwóch różnych stron (z dwóch różnych atomów węgla alfa). Ważne jest, aby umieć wybrać, która strona ma być poddana reakcji. Strona z mniejszą ilością podstawników (mniej podstawione centrum alfa) jest zwykle najłatwiejsza do deprotonacji i daje enolan kinetyczny. Może on być otrzymany w niskiej temperaturze (np. −78 °C) przy użyciu dużej, nieporęcznej zasady typu LDA, co zapobiega izomeryzacji. Druga strona, z większą ilością podstawników, prowadzi do enolanu termodynamicznego — bardziej podstawiona forma jest stabilniejsza energetycznie i wymaga zwykle wyższej temperaturze lub warunków umożliwiających odwracalną enolizację (np. słabsza zasada w warunkach równowagi).
Właściwości fizyczne i chemiczne
- Enole są zazwyczaj mniej stabilne niż odpowiadające im keto-formy, ale stabilność wzrasta przy sprzężeniu i możliwości tworzenia silnych wiązań wodorowych (przykład: β-diketonowe enole).
- Enole są nukleofilowe zarówno na atomie węgla alfa (C-reaktywność), jak i na atomie tlenu (O-reaktywność). Enolaty są z kolei ambidentnymi nukleofilami — przy odpowiednich warunkach reakcje alkilacji mogą zachodzić przez O- lub C-alkilację; wybór zależy od rodzaju metalu, rozpuszczalnika i temperatury.
- Enole wykazują charakterystyczne pasma w spektroskopii: w IR obecny jest pas OH (~3200–3600 cm−1) oraz sygnały C=C i C–O; w 1H NMR protony winylowe pojawiają się zwykle w obszarze 4–7 ppm, a sygnał OH może być szeroki i zależny od rozpuszczalnika.
- Typowe pKa wodnych dla protonów α przy karbonylach wynoszą około 17–25 (dla prostych ketonów ok. 19–21), dlatego potrzebne są stosunkowo mocne zasady do odwracalnej deprotonacji.
Typowe reakcje enoli/enolanów
- Reakcja aldolowa — łączenie dwóch jednostek karbonylowych przez nukleofilowy atak enolatu na karbonyl drugiego związku; to jedna z najważniejszych reakcji tworzących wiązania C–C (reakcja aldolowa).
- Alkilacja α — enolaty reagują z halogenowanymi elektrofilami prowadząc do alkilacji w pozycji α (C-alkilacja) lub, w innych warunkach, do O-alkilacji.
- Halogenacja α — enol/enolan ulega łatwo halogenowaniu w pozycji α (np. chlorowanie, bromowanie), często w obecności kwasu lub halogenu w kwasie.
- Claisen, Dieckmann — kondensacje prowadzące do acyloin i β‑ketoestrów; enolaty są kluczowymi reagentami w tych reakcjach.
- Michael — 1,4-donory enolanów w addycjach do α,β-nienasyconych układów karbonylowych.
- Tworzenie enamin i ich stosowanie jako „miękkich” ekwiwalentów enolów w katalizie aminowej (przykład: syntezy asymetryczne).
Praktyczne uwagi i przykłady
- Wybór zasady: do otrzymania enolanu kinetycznego używa się silnej, sterycznie utrudnionej zasady (np. LDA) w niskiej temperaturze; do otrzymania enolanu termodynamicznego często wystarcza alkoksyd (np. NaOEt) w temperaturze pokojowej.
- Niektóre układy preferują enol dzięki rezonansowi i wewnętrznym wiązaniom wodorowym — przykład: acetylaceton pokazuje silną tendencję do istnienia w formie enolowej.
- W syntezach często stosuje się pośredniki takie jak silyl enol ethers, które są bardziej selektywnymi i stabilnymi „odpowiednikami” enoli i pozwalają na kontrolowaną alkilację lub acylację.
Identyfikacja i analiza
Obecność enolu można potwierdzić przez spektroskopię IR (pasmo OH), 1H i 13C NMR (sygnały winylowe i chemiczne przesunięcia węgla α oraz sygnał OH), a także przez obserwację reakcji typowych dla enoli (np. reakcja z bromem dająca α‑bromoketon). W praktyce wiele enoli występuje jedynie w śladowych ilościach w równowadze z keto-formą i wykrywalnych jest jedynie przez szybkie śledzenie podczas reakcji lub przez zastosowanie pułapek (trapów) takich jak TMSCl dla wydajnego wychwycenia enolatu.
Enole i enolany odgrywają kluczową rolę w chemii organicznej, szczególnie w tworzeniu wiązań C–C i w syntezach budujących złożone cząsteczki. Znajomość mechanizmów enolizacji, czynników wpływających na stabilność oraz zasad kontroli selektywności (kinetycznej vs termodynamicznej) jest podstawą projektowania wielu reakcji w syntezie organicznej.