Co to są alkiny?
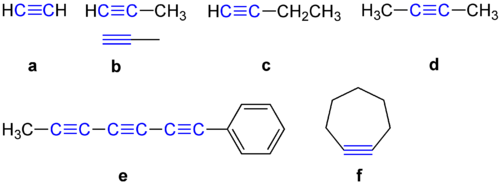
Alkiny to grupa węglowodorów, których cząsteczki zawierają atomy węgla połączone wiązaniem potrójnym C≡C. Ogólny wzór sumaryczny tych związków to CnH2n-2, a najprostszym przedstawicielem jest acetylen (etyn). Ze względu na obecność potrójnego wiązania alkiny nazywa się także acetylenami.
Charakterystyka i właściwości fizyczne
Alkiny są zwykle rozpuszczalne w rozpuszczalnikach organicznych i praktycznie nierozpuszczalne w wodzie. Struktura potrójnego wiązania powoduje liniową geometrię wokół atomów węgla, co wpływa na właściwości mechaniczne i polarność cząsteczki. W porównaniu z innymi węglowodorami alkiny wykazują wyższą reaktywność w reakcjach addycji i mogą uczestniczyć w wielu typach katalizowanych przemian.
Właściwości chemiczne i typowe reakcje
Potrójne wiązanie jest miejscem aktywnym: alkiny ulegają reakcjom addycji, redukcji oraz reakcjom perycyklicznym. Wiele przemian przebiega szybciej lub w inny sposób niż analogiczne reakcje z udziałem alkenów. Terminalne alkiny (z potrójnym wiązaniem na końcu łańcucha) mają słabiej sprzężoną protonową kwasowość i mogą być odbarczane przez silną zasadę, co pozwala na otrzymywanie anionów acetylidowych użytecznych w syntezie.
- Addycje: przyłączanie halogenów, wodoru lub halogenowodorów.
- Redukcja: selektywna redukcja daje alkeny bądź wiązania podwójne o konfiguracji cis lub trans, zależnie od warunków katalitycznych.
- Tworzenie wiązań C–C: aniony acetylidowe reagują z elektrofilami, co umożliwia wydłużanie łańcucha i sprzęganie z grupami karbonylowymi, jak ketony.
- Reakcje perycykliczne: alkiny biorą udział m.in. w cykloaddycjach i innych procesach perycyklicznych.
Synteza i chemia praktyczna
Alkiny można otrzymać na kilka sposobów: przez eliminację z odpowiednich halogenopochodnych, dehydrohalogenację lub przez reakcje sprzęgania. Gdy alkin występuje jako końcowy związek, łatwo go zdeprotonować i uzyskać nukleofil zdolny do przyłączania się do związków elektrofilowych. W laboratoriach i przemyśle stosuje się różne katalizatory i warunki, aby kontrolować stopień addycji i stereoizomerię powstających produktów.
Zastosowania i znaczenie
Alkiny, a zwłaszcza acetylen, mają szerokie zastosowanie: jako surowce w syntezie chemicznej, w produkcji tworzyw, przy wytwarzaniu leków i materiałów o specjalnych właściwościach. Acetylen był dawniej wykorzystywany jako paliwo do lamp i spawarek, a pośrednie produkty reakcji alkinów służą do budowy złożonych struktur organicznych. Ze względu na specyficzną reaktivność alkiny są też pożądane w chemii organicznej do tworzenia wiązań w nowych molekułach.
Różnice i uwagi bezpieczeństwa
Najważniejsze rozróżnienia: alkiny różnią się od alkenów i alkanów rodzajem wiązań i wynikającą z tego reaktywnością. Terminalne alkiny są bardziej kwasowe niż alkanowe wodorki, lecz znacznie mniej niż kwasy O–H czy N–H. Z praktycznego punktu widzenia: gazy takie jak acetylen mogą być wybuchowe i wymagają ostrożnego obchodzenia się oraz właściwego przechowywania. Dalsze informacje praktyczne i przykładowe procedury syntezy można znaleźć w materiałach źródłowych i podręcznikach chemii organicznej: źródło o redukcji, reakcje perycykliczne oraz ogólne kompendia (zob. także woda jako rozpuszczalnik w kontekście reakcji wodnych).
Podstawowe pojęcia i dalsze lektury: wiązanie potrójne, węglowodory, rozpuszczalniki organiczne, acetylen, atomy węgla, wzór ogólny, porównanie z alkenami, terminalne alkiny, silne zasady, addycje, reagowanie z ketonami, redukcje.