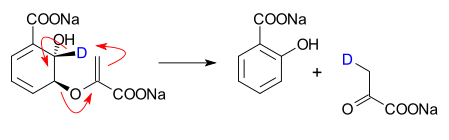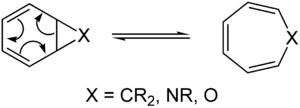
W chemii organicznej, reakcja perykliczna jest rodzajem reakcji chemicznej pomiędzy związkami organicznymi. W przypadku reakcji cyklicznych stan przejściowy cząsteczki jest pierścieniem (ma geometrię cykliczną), a reakcja przebiega w sposób skoordynowany. Reakcje cykliczne są zwykle reakcjami zmiany układu. Najważniejszymi grupami reakcji cyklicznych są:
- Reakcje elektrocykliczne
- Cyklodiady
- Reakcje Sigmatropic
- Reakcje przeniesienia grupy
- Reakcje cheletroptyczne
- Reakcje dyotropowe
Ogólnie rzecz biorąc, reakcje perykliczne są procesami równowagi. Możliwe jest jednak przesunięcie reakcji w jednym kierunku, jeśli produkt znajduje się na znacznie niższym poziomie energetycznym. Jest to zastosowanie zasady Le Chateliera do reakcji obejmującej pojedynczą cząsteczkę.
Wiele reakcji peryklicznych ma podobne stopniowe procesy radykalne z nimi związane. Chemicy nie zgadzają się, czy niektóre reakcje są reakcjami cyklicznymi. Na przykład, nie jest ostatecznie wiadomo, czy mechanizm [2+2] cykloaddycji jest zgodny (lub może zależeć od układu reaktywnego). Wiele reakcji peryklicznych ma podobne reakcje, które są skatalizowane metalami. Ale te reakcje skatalizowane metalami również nie są tak naprawdę perykliczne. Katalizatory metalowe stabilizują półprodukty reakcji. Tak więc reakcja nie jest skoordynowana, ale raczej stabilizowana metalicznie.
W syntezie korynowej wykonanej przez Alberta Eschenmosera, zawierającej układ 16π, wykorzystano duże fotoindukowane przesunięcie sigmatropowe wodoru.
Ze względu na zasadę odwracalności mikroskopowej, istnieje równoległy zestaw "retro" reakcji peryklicznych, które wykonują reakcję odwrotną.