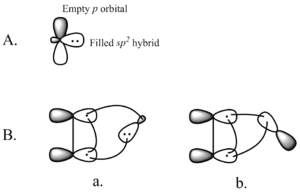
Reakcje cheletropowe są szczególną odmianą reakcji pericyklicznej, w której z jednej strony tworzy się jednocześnie dwoje nowych wiązań chemicznych do tego samego atomu. Reakcja pericykliczna przebiega przez stan przejściowy o cyklicznym układzie atomów i odpowiadającym mu cyklicznym układzie oddziałujących orbitali — w jego trakcie następuje jednoczesna reorganizacja wiązań σ i π. W reakcjach cheletropowych oba nowe wiązania są utworzone z tego samego atomu jednego z reagentów, co odróżnia je od innych typów cykloaddycji.
Charakterystyczne cechy
- Cheletropowe tworzenie/rozerwanie dwóch wiązań do jednego atomu reagentowego.
- Proces często przebiega w sposób skoordynowany (concerted), przez jednoczesne przesunięcie elektronów w zamkniętym cyklicznym stanie przejściowym.
- Wielu przykładom towarzyszy wydzielanie małej, stabilnej cząsteczki (np. CO, N2) — w takich przypadkach reakcję nazywa się czasem „wytrąceniem cheletropowym”. Siłą napędową jest często korzyść entropowa wynikająca z uwolnienia gazu.
- Stereochemia produktów jest zwykle ściśle kontrolowana przez mechanizm (stereospecyficzność), jeśli proces jest synchoronyczny i nie przebiega przez pośredniak rodnikowy.
Mechanizm orbitalny i reguły symetrii
Mechanizm cheletropowy mieści się w ramach teorii reakcji pericyklicznych. Kluczową rolę odgrywają tutaj wzajemne oddziaływania orbitali reagujących fragmentów (np. orbitali π układu wielokrotnego i orbitali karbenów, atomów z wolnymi parami itp.). Zastosowanie mają reguły symetrii Woodwarda–Hoffmanna: czy proces jest dozwolony termodynamicznie jako suprafacjalny czy wymaga przesunięć antarafacjalnych zależy od liczby elektronów biorących udział i układu orbitali. Dla prostych cheletropowych (np. dodawanie singletowych karbenów do alkenów) typowy jest skoncertowany, suprafacjalny przebieg, prowadzący do stereospecyficznych produktów.
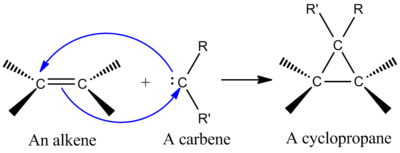
Przykładowo, w przypadku addycji singletowego karbenu (:CHR) do alkenu, orbital p karbenu i jego wolna para współdziałają z układem π węgiel–węgiel, tworząc jednocześnie dwa wiązania C–C i powstaje cyklopropan. Jeśli karben jest w stanie tripletowym, reakcja często przebiega dwuetapowo przez pośredniak rodnikowy, co zmniejsza stereospecyficzność.
Przykłady reakcji cheletropowych
- Cyklopropanacja alkenów przez karbeny — klasyczny przykład: dichlorokarben (:CCl2) lub meteń (:CH2) dodaje się do wiązania C=C, tworząc cyklopropan; oba nowe wiązania tworzone są z tego samego atomu karbenu.
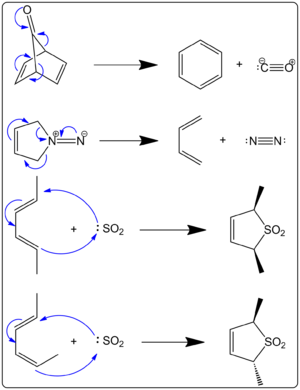
- Wytrącenia cheletropowe — reakcje, w których z układu odłączana jest mała cząsteczka, np. CO lub N2. W takich procesach zmiana entropii (uwolnienie gazu) jest często główną siłą napędową reakcji.
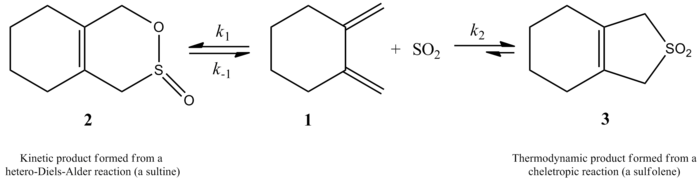
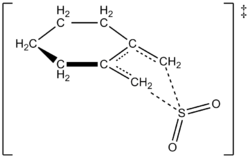
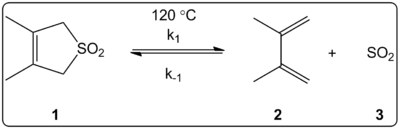
- Przykłady z tlenem i siarką — dodanie SO2 do dienów (prowadzące do związków typu sulfolenu) lub inne addycje, w których atom siarki/siarczanowy tworzy dwa nowe wiązania do jednego atomu reagentu, bywają klasyfikowane jako cheletropowe.
- Reakcje w chemii koordynacyjnej — tworzenie/rozerwanie wiązań między ligandami a metalami, gdzie jeden atom ligandu łączy się jednocześnie z dwoma centrami, może mieć charakter cheletropowy w sensie pericyklicznym.
Stereochemia i czynniki wpływające na przebieg
Główne czynniki decydujące o mechanizmie i stereochemii:
- Stan elektronowy reagentów (singlet vs triplet dla karbenów) — singlet sprzyja mechanizmowi skoordynowanemu, triplet — mechanizmowi dwuetapowemu przez rodniki.
- Symetria orbitali reagujących fragmentów — zgodność faz orbitali determinuje, czy przebieg jest dozwolony jako suprafacjalny lub wymagający antarafacjalności.
- Warunki termiczne — podwyższona temperatura sprzyja często procesom wytrącenia (eksergonicznym dzięki uwolnieniu gazu), natomiast niższe temperatury mogą faworyzować reakcje sterospecyficzne o niskiej energii aktywacji.
- Rozpuszczalnik i katalizatory — polarne rozpuszczalniki, katalizatory metaliczne lub fotochemia mogą zmieniać rodzaj karbenów/pośredników i tym samym mechanizm reakcji.
Znaczenie i zastosowania
Reakcje cheletropowe mają zastosowanie w syntezie organicznej (np. szybkie wprowadzanie trójczłonowych pierścieni przez cyklopropanację), w chemii materiałów oraz w procesach, gdzie kontrolowane wytrącenie małej cząsteczki jest wykorzystywane do napędu dalszych przemian. Rozumienie reguł orbitalnych pozwala chemikom projektować selektywne i stereospecyficzne warianty tych reakcji.
Podsumowanie
Reakcje cheletropowe to pericykliczne, często skoordynowane procesy, w których jeden atom jednego reagenta tworzy dwa wiązania z drugim reagentem. Mechanizm i stereochemia zależą od stanu elektronowego reagentów i symetrii orbitali; typowymi przykładami są cyklopropanacje karbenów i wytrącenia, w których uwalniany jest CO lub N2. Dzięki swojej specyfice i przewidywalnej stereochemii reakcje te są cennym narzędziem w syntezie organicznej.

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)