W chemii, orbital molekularny (lub MO) wyjaśnia, co dzieje się z elektronami, gdy atomy łączą się w cząsteczce. MO jest matematyczną funkcją, która opisuje falowe zachowanie elektronu w cząsteczce. Chemicy używają takich funkcji do przewidywania lub wyjaśniania właściwości chemicznych i fizycznych. Na przykład, funkcje te mogą określić prawdopodobieństwo znalezienia elektronu w dowolnym określonym obszarze.
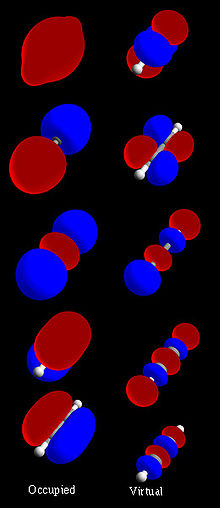
Chemicy zazwyczaj budują modele matematyczne orbit molekularnych poprzez łączenie orbit atomowych. Można również wykorzystać orbitały hybrydowe z każdego atomu cząsteczki, lub inne orbitały molekularne z grup atomów. Na tych funkcjach mogą pracować komputery. Orbitale molekularne pozwalają chemikom na zastosowanie mechaniki kwantowej do badania cząsteczek. MOs odpowiadają na pytania o to, jak atomy w cząsteczkach łączą się ze sobą. Różne zaokrąglone kształty na schemacie orbitalnym wskazują, gdzie najprawdopodobniej znajdowałyby się elektrony w atomie.
Jak powstają orbitale molekularne — metoda LCAO
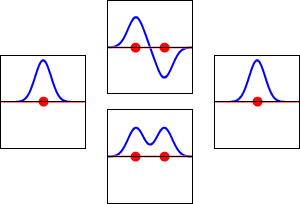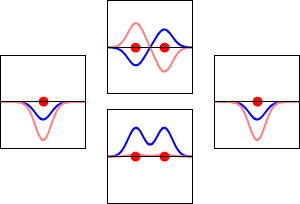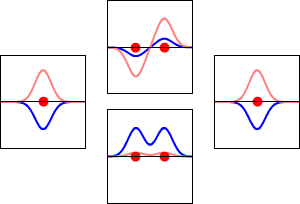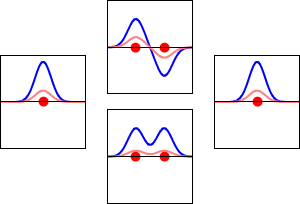
Najprostszy i najczęściej stosowany sposób konstrukcji orbitali molekularnych to metoda LCAO (Linear Combination of Atomic Orbitals) — liniowa kombinacja orbit atomowych. W tej koncepcji orbity atomowe poszczególnych atomów są ważone i sumowane, tworząc nowe funkcje rozciągające się na całą cząsteczkę. Sumy te dają dwa podstawowe typy orbitali:
- Orbital wiążący — powstaje przez konstruktywną interferencję falową (sumowanie faz zgodnych); ma niższą energię niż odpowiadające orbitale atomowe i prowadzi do stabilizacji wiązania.
- Orbital antywiążący — powstaje przez destruktywną interferencję (sumowanie faz przeciwnych); ma wyższą energię niż orbitale atomowe i osłabia wiązanie.
- Orbital niesparowany (wolna para / nonbonding) — orbita, która pozostaje w przybliżeniu na jednym atomie i nie przyczynia się istotnie do stabilizacji lub destabilizacji wiązania.
Symetria i reguły łączenia orbitali
Przy łączeniu orbitali ważna jest zgodność symetrii i energii. Orbital atomowy o pewnej symetrii może tworzyć z innym orbitale tylko wtedy, gdy mają zgodne właściwości symetryczne względem osi i płaszczyzn w cząsteczce. Różnice energii między orbitami atomowymi wpływają na stopień mieszania — im bliżej energetycznie, tym większe mieszanie i bardziej rozciągły orbital molekularny.
Diagramy orbitalne, obsada, HOMO i LUMO
Po zbudowaniu orbitali przypisuje się do nich obsadę elektronową zgodnie z zasadą zakazu Pauliego i regułą Hund'a. Kluczowe pojęcia to:
- HOMO (Highest Occupied Molecular Orbital) — najwyższy zajęty orbital molekularny; często determinuje zdolność do oddawania elektronu (kwasowość, reakcje utleniania).
- LUMO (Lowest Unoccupied Molecular Orbital) — najniższy niezajęty orbital molekularny; jest akceptorem elektronu w reakcjach — określa podatność na przyjmowanie elektronu (reaktywność elektrofilowa).
- Porządek wiązania — obliczany jako (liczba elektronów w orbitalach wiążących − liczba elektronów w orbitalach antywiążących) / 2; daje przybliżone pojęcie o sile wiązania.
Przykłady prostych cząsteczek
W najprostszych przypadkach, jak H2, dwa atomowe orbitale 1s łączą się tworząc jeden orbital wiążący σ(1s) i jeden antywiążący σ*(1s); wypełnienie orbitalu wiążącego dwoma elektronami daje trwałe wiązanie. W cząsteczce O2 teoria MO tłumaczy jej paramagnetyzm — dwa niesparowane elektrony zajmują orbitale π* antywiążące, co prowadzi do właściwości magnetycznych, których nie wytłumaczyłby prosty model wiązań kowalencyjnych.
Zastosowania w chemii i materiałach
Orbitalne opisywanie elektronów jest fundamentem wielu dziedzin chemii kwantowej i technologii:
- Wyjaśnianie i przewidywanie geometrii cząsteczek, długości i siły wiązań.
- Badanie reaktywności chemicznej — analiza HOMO/LUMO pozwala przewidywać miejsca ataku nukleofilowego i elektrofilowego.
- Spektroskopia — przejścia elektronowe między MO odpowiadają liniom w UV‑Vis, fotoemisji itp.
- Projektowanie materiałów przewodzących i półprzewodników — pasma energetyczne w ciałach stałych są rozszerzeniem pojęcia MO dla dużych układów.
- Kataliza i teoria reaktywności — orbity przejściowe i hybrydowe wyjaśniają mechanizmy katalityczne i wybiórczość reakcji.
Metody obliczeniowe i wizualizacja
Do obliczeń używa się wielu metod: przybliżonych (Hückel, ucząc się z prostych modeli) oraz bardziej zaawansowanych z zakresu mechaniki kwantowej, takich jak Hartree–Fock, metody post‑Hartree–Fock (MP2, CC) i funkcjonały gęstości (DFT). Wynikiem obliczeń są funkcje falowe i rozkłady gęstości elektronowej, które można wizualizować jako izopowierzchnie pokazujące kształt MW. Na tych wizualizacjach łatwiej jest zrozumieć rozkład ładunku, polaryzację i charakter wiązań.
Orbitały hybrydowe i lokalizacja
W wielu cząsteczkach wygodniej jest myśleć o orbitałach lokalnych lub hybrydowych (np. sp, sp2, sp3) — to transformacje liniowe MO, które ułatwiają interpretację geometrii i chemii wiązań (np. kątów i kierunkowości wiązań w związkach organicznych). Lokalizowane MO (np. orbitale Boys'a) pozwalają na oddzielenie wiązań kowalencyjnych i wolnych par w wygodny sposób do analizy chemicznej.
Ograniczenia i przybliżenia
Model MO jest potężny, ale opiera się na przybliżeniach: w praktyce używa się skończonych baz funkcji, zaniedbuje niektóre korelacje elektronowe lub stosuje przybliżone funkcjonały DFT. Dlatego wyniki powinny być interpretowane z uwzględnieniem błędów metodycznych oraz porównywane z danymi eksperymentalnymi tam, gdzie to możliwe.
Podsumowanie
Orbitale molekularne to centralne narzędzie chemii kwantowej: łącząc idee falowe z zasadami symetrii i regułami obsady, pozwalają chemikom przewidywać i wyjaśniać strukturę, właściwości i reaktywność cząsteczek. Dzięki komputerowym metodom obliczeniowym MO stały się praktycznym instrumentem w projektowaniu leków, katalizatorów, materiałów oraz w zrozumieniu procesów fotochemicznych i elektronowych.