Przegląd
Orbital atomowy to matematyczny opis przestrzeni wokół jądra, w której z największym prawdopodobieństwem występuje elektron. Formalnie orbital to wynik rozwiązania równania falowego (funkcji falowej) opisującej stan jednego lub pary elektronów w atomie; wartość bezwzględna kwadratu tej funkcji daje gęstość prawdopodobieństwa występowania elektronu (funkcja falowa, opis atomu). Termin "orbital" zastąpił starszy obraz elektronów krążących po sztywnych ścieżkach.
Cechy i klasyfikacja
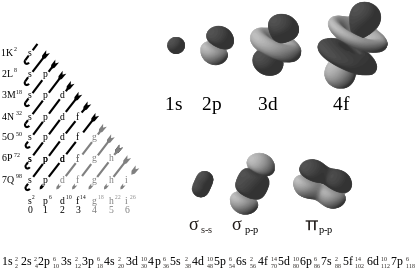
Orbital określają cztery liczby kwantowe: główna, poboczna, magnetyczna i spinowa — każda z nich wpływa na energię, kształt i orientację orbitalu. Orbital może pomieścić maksymalnie dwa elektrony o przeciwnych spinach (teoria atomowa, mechanika kwantowa). Najważniejsze typy orbitali to s, p, d i f, różniące się kształtem i symetrią; przykładowo orbital s jest kulisty, a orbitale p mają kształt hantli.
- Powłoka i podpowłoka: powłoka odpowiada głównej liczbie kwantowej, podpowłoka — pobocznej.
- Obsada: konfiguracja elektronowa informuje które orbitale są zajęte i ile elektronów jest na danym orbitalu (konfiguracje elektronowe).
- Przejścia: elektrony mogą przechodzić między orbitalami, emitując lub absorbując kwanty energii widoczne w spektroskopii.
Historia pojęcia
Początkowe modele atomu korzystały z analogii do Układu Słonecznego — jądro jak Słońce, elektrony jak planety — stąd nazwy i wyobrażenia (układ słoneczny). Z czasem obraz klasycznych orbit został zastąpiony przez mechanikę kwantową i równanie Schrödingera; pojęcie orbitalu wyłoniło się jako probabilistyczny opis rozkładu elektronu. Nazwy orbitali s, p, d, f mają historyczne korzenie w klasyfikacji linii spektroskopowych: sharp, principal, diffuse i fundamental, odkrytych podczas badań emisyjnych metali (spektroskopia, metale alkaliczne).
Znaczenie i zastosowania
Orbital jest centralnym pojęciem w chemii i fizyce atomowej: wyjaśnia wiązania chemiczne (poprzez nakładanie orbitali i tworzenie orbitali molekularnych), geometrię cząsteczek (hybrydyzacja), właściwości magnetyczne i widma elektronowe. Zrozumienie orbitali umożliwia przewidywanie reaktywności, stabilności stanów elektronowych oraz interpretację eksperymentalnych danych spektroskopowych. W teorii molekularnej orbitale atomowe służą jako baza do konstrukcji orbitali molekularnych, które opisują rozkład elektronów w cząsteczkach.
Różnice i uwagi terminologiczne
Należy rozróżnić orbital od klasycznej orbity: orbitale nie są ścieżkami ruchu, lecz funkcjami opisującymi prawdopodobieństwo. Terminy powłoka i podpowłoka odnoszą się do zbiorów orbitali o podobnej energii. Dla różnych pierwiastków liczba dostępnych orbitali zależy od ich konfiguracji i położenia w układzie okresowym — na przykład rozmieszczenie elektronów zmienia się z okresem (element, okres). W praktyce obliczeniowej i badawczej pojęcia te łączone są z narzędziami teoretycznymi i eksperymentalnymi (orbital — nazwa, jądro).
Więcej informacji o matematycznym opisie, wzorach i zastosowaniach można znaleźć w literaturze specjalistycznej oraz zasobach edukacyjnych (elektrony, atom, funkcja falowa). Zastosowania praktyczne obejmują chemię kwantową, spektroskopię i projektowanie materiałów, gdzie zrozumienie orbitali jest kluczowe dla przewidywania właściwości elektronowych.
Ważna jest także świadomość, że pojęcie orbitali rozwija się wraz z postępem teorii i metod obliczeniowych — opisy coraz bardziej złożonych układów wymagają rozszerzeń pojęciowych i numerycznych (mechanika kwantowa, teoria atomowa). Kompleksowe omówienia znajdują się w podręcznikach do chemii kwantowej oraz pracach przeglądowych.