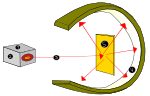
W 1850 r. Sir William Crookes skonstruował "lampę wyładowczą", czyli szklaną rurkę z usuniętym powietrzem i metalowymi elektrodami na jej końcach, podłączoną do źródła wysokiego napięcia. Kiedy w rurze wytwarza się próżnia, można zaobserwować wyładowanie świetlne, które przechodzi od katody (elektrody naładowanej ujemnie) do anody (elektrody naładowanej dodatnio). Crookes nazwał tę emisję "promieniami katodowymi".
Po eksperymentach z promieniami katodowymi Sir Joseph John Thomson ustalił, że emitowany promień tworzą ładunki ujemne, ponieważ są one przyciągane przez biegun dodatni. Thomson wiedział, że atomy są elektrycznie obojętne, ale ustalił, że aby tak było, atom powinien mieć taką samą ilość ładunków ujemnych i dodatnich. Ładunki ujemne nazwał elektronami (e-).
Zgodnie z przyjętymi założeniami o neutralnym ładunku atomów, Thomson zaproponował pierwszy model atomu, który został opisany jako dodatnio naładowana kula, w którą zostały włożone elektrony (o ładunku ujemnym). Znany jest on pod nazwą modelu budyniu śliwkowego.
W 1906 roku Robert Millikan ustalił, że elektrony mają ładunek Coulomba (C) równy -1,6 * 10-19, co pozwoliło obliczyć jego masę jako maleńką, równą 9,109 * 10-31 kg.
W tym samym czasie, eksperymenty Eugene Goldsteina w 1886 r. z lampami wyładowczymi katodowymi pozwoliły mu ustalić, że ładunki dodatnie miały masę 1,6726 * 10-27 kg i ładunek elektryczny +1,6 * 10 -19 C. Lord Ernest Rutherford nazwał później te dodatnio naładowane cząstki protonami