Atomy pierwiastka chemicznego mogą występować w różnych typach. Są one nazywane izotopami. Mają one tę samą liczbę protonów (i elektronów), ale różne liczby neutronów. Różne izotopy tego samego pierwiastka mają różne masy. Masa jest słowem określającym, ile substancji (lub materii) coś ma. Rzeczy o różnych masach mają różne ciężary. Ponieważ różne izotopy mają różne liczby neutronów, to nie wszystkie ważą tyle samo lub mają tę samą masę.
Różne izotopy tego samego pierwiastka mają tę samą liczbę atomową. Mają taką samą liczbę protonów. O liczbie atomowej decyduje liczba protonów. Izotopy mają jednak różne liczby masowe, ponieważ mają różne liczby neutronów.
Słowo izotop, oznaczające to samo miejsce, pochodzi z faktu, że izotopy znajdują się w tym samym miejscu układu okresowego.
W atomie neutralnym, liczba elektronów równa się liczbie protonów. Izotopy tego samego pierwiastka mają też tę samą liczbę elektronów i tę samą strukturę elektronową. Ponieważ o sposobie działania atomu decyduje jego elektroniczna struktura, izotopy są prawie takie same chemicznie, ale różnią się fizycznie od siebie.
Cięższe izotopy reagują chemicznie zwykle wolniej niż lżejsze izotopy tego samego pierwiastka. Ten „efekt masowy” jest szczególnie widoczny dla przyzębia (1H) i deuteru (2H), ponieważ deuter ma około dwukrotnie większą masę od przyzębia. W przypadku cięższych pierwiastków względny stosunek masy atomowej pomiędzy izotopami jest znacznie mniejszy, a efekt masowy jest zazwyczaj niewielki.
Notacja izotopowa i przykłady
Izotopy zwykle zapisuje się za pomocą notacji AZX, gdzie A to liczba masowa (suma protonów i neutronów), Z to liczba atomowa (liczba protonów), a X to symbol pierwiastka. Przykłady:
- 12C – stabilny izotop węgla używany jako podstawa skali mas atomowych;
- 14C – radioaktywny izotop węgla wykorzystywany w datowaniu (metoda radiowęglowa);
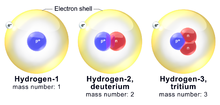
- 1H (znany też jako protium), 2H (deuter), 3H (tryt) – izotopy wodoru.
Rodzaje izotopów
- Stabilne – nie ulegają rozpadowi radioaktywnemu w skali czasowej obserwowalnej; wiele pierwiastków ma kilka stabilnych izotopów (np. tlen: 16O, 17O, 18O).
- Radioaktywne (promieniotwórcze) – mają niestabilne jądra i przemieniają się w inne nuklidy, emitując promieniowanie (rozpady α, β, γ). Każdy izotop promieniotwórczy ma określony czas połowicznego rozpadu (półokres).
Właściwości fizyczne i chemiczne
Chemicznie izotopy jednego pierwiastka zachowują się bardzo podobnie, ponieważ mają taką samą konfigurację elektronową. Różnice pojawiają się głównie w właściwościach fizycznych zależnych od masy: gęstości, temperatur topnienia/krzepnięcia, prędkości reakcji chemicznych (efekt izotopowy) czy kinetyce dyfuzji. W chemii kinetycznej mówimy o efekcie izotopowym kinetycznym (KIE), który opisuje różnicę szybkości reakcji między izotopami.
Stabilność jądrowa i rozpad
Stabilność jądrowa zależy od stosunku protonów do neutronów oraz od energetyki jądra. Niestabilne izotopy mogą ulegać:
- rozpadowi α (emisja cząstki α – jądra helu),
- rozpadowi β− lub β+ (emisja elektronu lub pozytonu przy przemianie neutronu w proton lub odwrotnie),
- emisji promieniowania γ (fotony wysokiej energii) po przejściach energetycznych jądra.
Zastosowania izotopów
- Datowanie – np. 14C do datowania materiałów organicznych, izotopy U/Pb, K/Ar do datowania geologicznego.
- Medycyna – izotopy promieniotwórcze jako znaczniki w diagnostyce obrazowej (np. 99mTc w scyntygrafii) i w terapii (np. 131I w leczeniu chorób tarczycy).
- Badania środowiskowe i klimatyczne – izotopy tlenu i węgla w analizach paleoklimatycznych, śledzenie źródeł zanieczyszczeń.
- Metody śledzenia i znaczniki – izotopy stabilne wykorzystywane jako znaczniki w badaniach metabolicznych, procesach chemicznych i biologicznych.
- Przemysł i energetyka – izotopy używane w kontroli korozji, badaniach nieniszczących, a także paliwa jądrowe (np. 235U).
- Badania naukowe – spektroskopia izotopowa, badania struktury materii, studia reakcji jądrowych.
Występowanie i produkcja
Niektóre izotopy występują w przyrodzie w stałych stosunkach izotopowych (np. stosunki 18O/16O w wodzie), inne powstają wtórnie wskutek promieniowania kosmicznego (14C) lub jako produkty rozpadu. Izotopy radioaktywne do zastosowań przemysłowych i medycznych często wytwarza się w reaktorach jądrowych lub akceleratorach poprzez bombardowanie jąder cząstkami.
Znaczenie w ustalaniu masy atomowej
Średnie wartości mas atomowych podane w tablicach uwzględniają naturalne występowanie wszystkich stabilnych izotopów danego pierwiastka i ich proporcje. Standard masy atomowej oparty jest na 12C (definiuje skalę mas atomowych).
Podsumowanie
Izotopy to odmiany tego samego pierwiastka różniące się liczbą neutronów i masą. Choć zachowują podobne właściwości chemiczne (ta sama struktura elektronowa), różnice masowe wpływają na właściwości fizyczne i szybkość reakcji. Znajomość izotopów i ich właściwości jest kluczowa w chemii, medycynie, geologii, ekologii i wielu dziedzinach techniki.