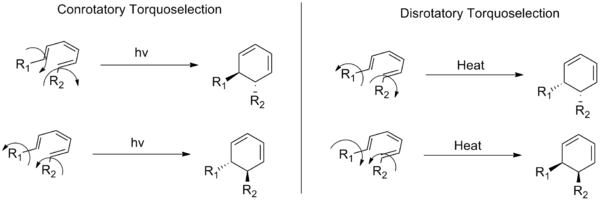
Konrotacyjny i dysrotacyjny to dwa podstawowe tryby przemian w reakcjach elektrocyklicznych — rodzaju reakcji elektrocyklicznej w chemii organicznej. W trybie konrotacyjnym podstawniki na końcach sprzężonego układu wiązań podwójnych obracają się w tym samym kierunku (oba zgodnie albo oba przeciw), natomiast w trybie dysrotacyjnym poruszają się w przeciwnych kierunkach (jeden zgodnie, drugi przeciwnie). Ta różnica kierunków rotacji decyduje o fazie końcowych orbitali p i w konsekwencji o dopuszczalności i stereochemii produktu reakcji.
Mechanika orbitalna (podejście FMO)
Decydującym czynnikiem jest symetria najwyżej zajmowanego orbitalu molekularnego (HOMO) w stanie, w którym zachodzi reakcja. Podczas zamykania pierścienia końcowe lobule orbitalu π muszą połączyć się tak, aby utworzyć nowe wiązanie σ z właściwą symetrią (taką, by fazy lobuli były zgodne). Jeśli aby uzyskać zgodność faz konieczne jest obrócenie końców w tę samą stronę, proces będzie konrotacyjny; jeśli konieczny jest obrót w przeciwnych kierunkach — dysrotacyjny.
Zasady Woodwarda–Hoffmanna
Zasady Woodwarda-Hoffmanna upraszczają wybór trybu na podstawie liczby elektronów π i rodzaju wzbudzenia (termicznie czy fotochemicznie). W skrócie:
- Dla reakcji termicznych: układy zawierające 4n + 2 elektronów π (n — liczba całkowita, np. 6π) przebiegają dysrotacyjnie, natomiast układy zawierające 4n elektronów π przebiegają konrotacyjnie.
- Dla procesów fotoindukowanych (pojedyncze wzbudzenie elektronowe zmienia obsadę orbitali): układy 4n + 2 elektronów π przebiegają konrotacyjnie, a układy 4n elektronów π przebiegają dysrotacyjnie.
Innymi słowy: tryb reakcji odwraca się po przejściu z warunków termicznych do fotochemicznych. To wynika z tego, że w stanie wzbudzonym zmienia się konfiguracja orbitalna (np. HOMO staje się innym orbitalem), a więc także warunki zachowania symetrii.
Przykłady i konsekwencje stereochemiczne
Typowym przykładem jest zamykanie 6π systemów (np. heksatrienów): przy warunkach termicznych (4n+2, n=1) zamknięcie przebiega dysrotacyjnie — końcowe p-lobule poruszają się w przeciwnych kierunkach, co prowadzi do określonej konfiguracji podstawników w produkcie. Dla tego samego układu, jeżeli reakcja jest fotoindukowana, tryb ulega odwróceniu i staje się konrotacyjny.
Stereospecyficzność elektrocyklicznych przemian oznacza, że konfiguracja wyjściowa (układ cis/trans podstawników przy końcach łańcucha) bezpośrednio determinuje konfigurację powstałego centrum chiralnego lub układu geometrycznego w produkcie — dlatego te reakcje są powszechnie wykorzystywane do stereoselektywnej syntezy związków cyklicznych.
Dlaczego to ma znaczenie?
- Przewidywanie produktów: znajomość liczby elektronów π i tego, czy reakcja jest termiczna czy fotochemiczna, pozwala przewidzieć, czy reakcja przebiegnie kon- czy dysrotacyjnie i jakie będą stereoizomery produktów.
- Projektowanie syntez: chemicy wykorzystują te zasady do planowania reakcji, tak aby uzyskać pożądane stereoizomery lub uniknąć niepożądanych układów konfiguracyjnych.
- Zrozumienie mechanizmu: podejście orbitalne (FMO) tłumaczy, dlaczego niektóre przemiany są „dozwolone” (szybkie) a inne „zabronione” (wolne lub wymagające wzbudzenia MS).
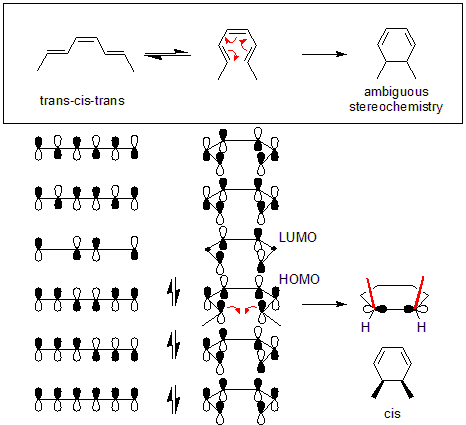
Na powyższym rysunku widać różnicę pomiędzy reakcjami konrotacyjnymi i dysrotacyjnymi: w pierwszym przypadku oba końce łańcucha obracają się w tym samym kierunku, w drugim — w przeciwnych. Ilustracja ta pomaga wizualizować, jak zmienia się faza lobuli orbitalnych p przy tworzeniu nowego wiązania σ.
Podsumowując: rozróżnienie konrotacyjny/dysrotacyjny oraz znajomość zasad Woodwarda–Hoffmanna i mechaniki orbitalnej pozwalają przewidzieć przebieg i stereochemię elektrocyklicznych reakcji pierścieniotwórczych i pierścieniotwórczych odwrotnych, co ma kluczowe znaczenie w chemii syntetycznej.