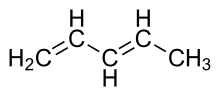
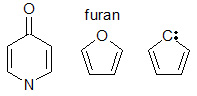
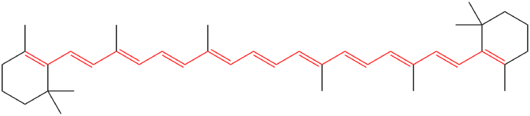
W chemii układ sprzężony jest układem połączonych p-orbitali z delokalizowanymi elektronami. Układy sprzężone są tworzone przez kilka wielokrotnych wiązań, z których każde jest oddzielone pojedynczym wiązaniem. Ogólnie rzecz biorąc, układy koniugowane mogą obniżać ogólną energię cząsteczki i zwiększać jej stabilność. Mogą one zawierać samotne pary, rodniki lub jony karbenu. Związek może być cykliczny, acykliczny, liniowy lub mieszany. W większości przypadków atomy w cząsteczce są trzymane razem przez pojedyncze wiązania (gdzie orbity z sąsiednich atomów nakładają się na siebie). Cząsteczki, które mają sprzężony układ, mają unikalne właściwości, różniące się od zwykłych związków tworzonych przez udział elektronów przeniesionych pomiędzy wieloma atomami.
Koniugacja jest nakładaniem się na siebie jednego p-orbitalu i drugiego w poprzek wiązania sigma (lub pojedynczego wiązania), które znajduje się pomiędzy nimi. (D-orbity większych atomów mogą również przyczyniać się do powstania układu sprzężonego).
System sprzężony ma region nakładających się na siebie p-orbity, pomijając pojedyncze wiązania, które są pomiędzy nimi. Pozwalają one na przeniesienie elektronów pi na wszystkie przylegające do siebie wyrównane p-orbity. Elektrony pi nie należą do pojedynczego wiązania lub atomu, ale do grupy atomów.
Największe sprzężone układy (o największej liczbie elektronów wspólnych) znajdują się w graficie, polimerach przewodzących i nanorurkach węglowych.