Cykloaddycja to reakcja chemiczna pomiędzy reagentami z wiązaniami podwójnymi, które zostają zastąpione przez strukturę pierścienia. Jest to perycykliczna reakcja chemiczna, w której "dwie lub więcej nienasyconych cząsteczek (lub części tej samej cząsteczki) łączy się ze sobą, tworząc cykliczny addukt, w którym następuje redukcja netto mnogości wiązań." Jest to reakcja cyklizacji: tworzy nowy pierścień z atomów.
Cykloaddycje są nazywane według podstawowego rozmiaru cząsteczek, które są łączone. W ten sposób reakcja Dielsa-Aldera jest [4 + 2]cykloaddycją, a 1,3-dipolarna cykloaddycja jest [3 + 2]cykloaddycją. Ten typ reakcji jest reakcją addycji niepolarnej.
Mechanizm i zasady orbitalne
Cykloaddycje perycykliczne typowo przebiegają w sposób koncertowany — wszystkie wiązania tworzą się i rozrywają jednocześnie w jednym stanie przejściowym. Kluczową rolę odgrywają tutaj interakcje między orbitami granicznymi reagentów (Frontier Molecular Orbitals, FMO): głównie HOMO jednej cząsteczki i LUMO drugiej. Zgodność fazowa i różnica energii tych orbitali decydują o szybkości i regio-/stereoselektywności reakcji.
Reguły Woodwarda–Hoffmanna przewidują, które cykloaddycje są termicznie dozwolone (najczęściej suprafacjalne przebiegi dla odpowiedniej parzystości elektronów) a które są zabronione i muszą być wymuszone fotochemicznie lub przebiegać przez mechanizmy krokowe (diradikalne lub jonowe).
Rodzaje i przykłady
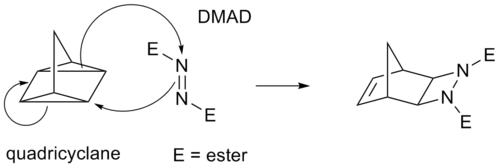
- [4+2] — reakcja Dielsa–Aldera: łączy dien w układzie 1,3-butadienu (4 atomy) z dienofilem (2 atomy). Przykład: cyklopentadien reagujący z maleinowym anyhydrydem daje adukt sześcioczłonowy. Reakcja jest stereospecyficzna (konfiguracja podwójnego wiązania dienofilu przenosi się na produkt) i często kieruje się regułą endo/exo (preferencja endo przy obecności akceptorów elektronowych w dienofilie).
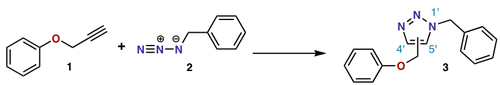
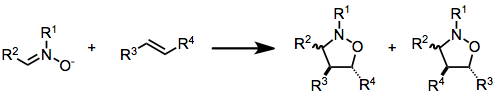
- [3+2] — 1,3-dipolarna cykloaddycja: łączy dipol 1,3 (np. azotyn, azid, nitrony) z alkenem lub alkinem, tworząc pięcioczłonowe heterocykliczne produkty (np. izoksazolidyny, izydyny). Przykładem technologicznie ważnej reakcji jest azydowo-alkinowa cykloaddycja katalizowana miedzią (CuAAC) — tzw. „click chemistry”.
- [2+2] — cykloaddycja: tworzy czteroczłonowe pierścienie; jest zwykle termicznie zabroniona dla suprafacjalnego przebiegu (z powodu zasad symetrii), ale możliwa fotochemicznie lub poprzez mechanizmy krokowe (diradikalne).
- Hetero-cykloaddycje: obejmują reagenty zawierające heteroatomy (O, N, S) i prowadzą do utworzenia heterocykli, szeroko wykorzystywanych w syntezie związków biologicznie aktywnych.
Stereochemia i selektywność
Cykloaddycje są zwykle stereospecyficzne — konfiguracja geometryczna reagujących multiplektywnych wiązań (cis/trans) jest często zachowywana w produkcie. Regioselektywność (które atomy łączą się ze sobą) przewiduje się na podstawie rozkładów gęstości HOMO i LUMO oraz efektów elektronowych podstawników. Wiele cykloaddycji wykazuje preferencję endo (np. w Diels–Alderze) ze względu na korzystne oddziaływania orbitalne w stanie przejściowym.
Kataliza i warunki reakcyjne
- Kwasy Lewisa (np. AlCl3, BF3, ZnCl2) obniżają energię LUMO dienofila i znacząco przyspieszają reakcje Diels–Aldera oraz poprawiają selektywność.
- Katalizatory chiralne umożliwiają asymetryczną wersję cykloaddycji, dając produkty z wysoką enancjoselektywnością — kluczowe w syntezie leków i naturalnych produktów.
- Fotochemia — używana do uruchamiania cykloaddycji zabronionych termicznie (np. [2+2]).
- Rozpuszczalniki, temperatura i ciśnienie mogą silnie wpływać na przebieg i szybkość reakcji; niekiedy stosuje się wysokie ciśnienia, by przyspieszyć procesy cyklizacji.
Mechanizmy alternatywne
Choć wiele cykloaddycji przebiega koncertowanie, istnieją przypadki mechanizmów krokowych przez pośredniki diradikalne lub jonowe — szczególnie gdy obecne są silnie polarne podstawnikii lub gdy reakcję katalizuje metal. Takie mechanizmy mogą zmieniać stereochemię i selektywność produktów.
Zastosowania
- Budowa pierścieni w syntezach naturalnych produktów i leków — szybkie zwiększanie złożoności strukturalnej.
- W syntezie materiałów i polimerów — tworzenie cyklicznych segmentów o specyficznych właściwościach.
- „Click chemistry” (np. CuAAC) — szybkie i wydajne łączenie fragmentów molekularnych w chemii biologicznej i medycznej.
- Reakcje odwrotne (retrocycloaddycje) — używane retrosyntaktycznie lub do fragmentacji złożonych cząsteczek.
Podsumowanie
Cykloaddycje to uniwersalna i potężna klasa reakcji w chemii organicznej, umożliwiająca szybkie tworzenie pierścieni i złożonych struktur przy zachowaniu stereochemii reagentów. Znajomość mechanizmu orbitalnego, reguł Woodwarda–Hoffmanna, wpływu katalizatorów i warunków reakcji pozwala przewidywać wynik i optymalizować przebieg procesu, co czyni cykloaddycje fundamentem nowoczesnej syntezy organicznej.
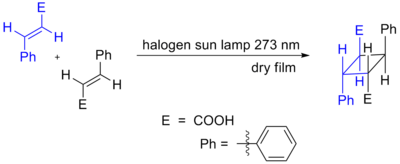
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)