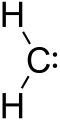Karben to cząsteczka zawierająca atom węgla, który jest połączony dwoma wiązaniami do sąsiednich grup (R i R') i ma dwa dodatkowe elektrony, które nie biorą udziału wwiązaniach. W praktyce węgiel taki ma 6 elektronów walencyjnych (zamiast pełnych 8), co sprawia, że karbeny są zwykle bardzo reaktywne. Ogólny wzór można zapisać jako R-(C:)-R'. Karben można traktować jako połączenie donora elektronów (para wolna) i centrum elektronowopozbawionego (puste orbitalne) — to determinujące właściwości chemiczne tej klasy związków.
Budowa elektronowa i stany spinowe: singlet i tryplet
Karbeny występują w dwóch podstawowych stanach elektronowych:
- Singlet — oba niesparowane elektrony tworzą parę elektronową (podobną do samotnej pary) i zajmują ten sam orbital (zwykle hybrydowy sp2), podczas gdy prostopadły orbital p jest pusty. Singlety są stanami zamkniętoskorupkowymi i zwykle zachowują się jako elektrofile (mają tendencję do przyjmowania elektronów).
- Tryplet — dwa elektrony znajdują się na różnych orbitalach i mają równoległe spiny (ten sam spin), co daje stan rodnikowy z dwoma niesparowanymi elektronami. Tryplety często wykazują reactivity typową dla rodników (np. dodawanie jednoelektronowe).
Różnica energetyczna między tymi stanami (tzw. singlet–tryplet gap) zależy od podstawników przy węglu karbenowym. Na przykład karbeny z atomami heteroatomów posiadającymi pary elektronowe (np. OR, NR2, a także halogeny z możliwością n→p sprzężenia) zwykle stabilizują stan singletowy, gdyż mogą donować gęstość elektronową do pustego orbitalu p. Z kolei podstawnikialkilowe stabilizują częściej stan trypletowy przez hyperkonjugację i brak efektywnego sprzężenia z pustym p-orbitalem.
Powstawanie karbenów
Karbeny można wytwarzać kilkoma powszechnymi metodami:
- Termiczna lub fotochemiczna dekompozycja związków diazowych (R2C=N2) — jedna z najczęściej używanych dróg, prowadząca do wydzielenia N2 i powstania karbenów wolnych.
- α-Eliminacja halogenopochodnych (np. reakcje prowadzące do :CCl2) lub termoliza diaziryn/ketenów.
- Generowanie karbenów „karbenoidowych” przy użyciu reagentów metalicznych, np. w reakcji Simmons–Smith (reagent iodometyleno-cynkowy) — daje pośredniki o właściwościach zbliżonych do karbenów, ale związane z metalem.
- Kompleksy metal–karben (np. w katalizie przejściowometalicznej) — tutaj karben jest związany z metalem i wykazuje inne właściwości niż wolny karben (patrz: karbeny typu Fischer i Schrock).
Typowe reakcje chemiczne
Karbeny biorą udział w wielu typach przemian, zarówno jako elektrofile, jak i nukleofile, w zależności od ich natury (singlet/tryplet) i podstawników. Do najważniejszych reakcji należą:
- Cyklopropanacja — addycja do wiązań podwójnych (np. alkenów), prowadząca do powstania pierścieni cyklopropanowych; typowa reakcja karbenów singletowych.
- Wstawianie — wstawianie do wiązań C–H, O–H, N–H i innych (tworzenie nowych wiązań C–X).
- Dimeryzacja — dwa karbeny mogą połączyć się, tworząc alkeny (w zależności od warunków i natury karbenu).
- Tworzenie ylides — reakcje z heteroatomowymi donorami (np. z tiolami, fosfinami, karbonylami) prowadzące do powstawania ylidu (ważne w wielu przemianach syntetycznych).
- Reakcje cheletropowe i przemieszczenia — karbeny uczestniczą też w reakcjach pericyklicznych (reakcje cheletropowe) oraz w przebudowach strukturalnych, jak np. przemiana Wolffa (α-diazoketony → keteny).
Stabilność karbenów — od bardzo reaktywnych do trwałych
Większość wolnych karbenów jest krótkożyjąca i trudno jest je zestalnić w warunkach standardowych. Niemniej jednak istnieją wyjątki:
- Karbeny trwałe — przykładem są karbeny heterocykliczne nienasycone (N-heterocyclic carbenes, NHC), takie jak IMes czy IPr, które dzięki silnemu efektowi stabilizującemu od atomów azotu i odpowiedniej steryce mogą istnieć jako izolowane związki w temperaturze pokojowej. NHC są powszechnie używane jako ligandy i jako organokatalizatory.
- Karbeny metaliczne — w wielu reakcjach katalitycznych karben jest związany z metalem (np. kompleksy Ru w katalizatorze Grubbsa). Warto tu podkreślić, że katalizator Grubbsa zawiera kompleks metal–karben, a nie wolny karben; takie kompleksy są kluczowe w reakcji metatezy wiązań podwójnych.
- Klasyfikacja Fischer vs Schrock — w chemii kompleksów karbenowych rozróżnia się karbeny typu Fischer (zwykle na metalach z wyższymi stanami utlenienia i z ligandami π-akceptorowymi; karbon karbonowy ma charakter elektrofilowy) oraz karbeny typu Schrock (na metalach w niskich stopniach utlenienia, często bardziej nukleofilowe i rodnikowe).
Zastosowania
Karbeny i ich pochodne mają szerokie zastosowania w syntezie organicznej i katalizie:
- Synteza cyklopropanów (budowa trzechpierścieniowych fragmentów), ważna w chemii leków i materiałów.
- Kataliza metatezy olefin (kompleksy typu Grubbs) wykorzystywane w tworzeniu węglowodorów i makrocząsteczek.
- NHC jako stabilne ligandy i katalizatory w reakcjach tworzenia wiązań C–C i C–heteroatomowych.
- Reakcje selektywnych wstawień i przekształceń, przydatne w konstrukcji złożonych cząsteczek organicznych.
Podsumowując, karbeny to jedne z najbardziej interesujących i użytecznych pośredników w chemii organicznej — od bardzo reaktywnych, krótkotrwałych wolnych karbenów po stabilne karbeny związane z metalami lub izolowane NHC, wykorzystywane w licznych reakcjach syntetycznych i katalitycznych.