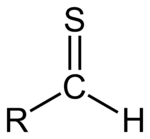
Tial lub tioaldehyd to dowolna cząsteczka z grupą RC(S)H. Jest on podobny do aldehydu, w którym atom tlenu zamieniony jest na siarkę. Siarka tworzy z węglem podwójne wiązanie C=S i zachowuje dwie samotne pary, co istotnie wpływa na własności elektronowe i geometryczne tych związków.
Właściwości fizyczne i chemiczne
Tiale mają charakterystyczne właściwości różniące je od zwykłych aldehydów. Wiązanie C=S jest na ogół dłuższe i słabsze niż C=O, a rozkład ładunku i polarność grupy tiokarbonylowej różnią się od grupy karbonylowej. Z punktu widzenia chemii są one zazwyczaj silnymi elektrofilami, ponieważ atom węgla wiązany z siarką łatwo przyciąga elektrony nukleofilów. Wiele tioaldehydów ma dużą reaktywność i krótkotrwałą żywotność w standardowych warunkach; często łatwo ulegają dimerom, oligomeryzacji lub dalszym przemianom.
Reaktywność i typowe reakcje
- Adicje nukleofilowe — podobnie jak inne grupy C=Y, tiale reagują z nukleofilami (np. tioaddycje), prowadząc do produktów addycji przy atomie węgla.
- Cykloadycje — grupy C=S są bardzo dobrymi dienofilami, dlatego tioaldehydy i inne tiokarbonylowe pochodne często biorą udział w reakcjach typu Dielsa–Aldera i innych cykloaddycjach, co bywa wykorzystywane w syntezie złożonych układów pierścieniowych.
- Dimerizacja i polimeryzacja — wiele tiali szybko reaguje samych ze sobą, tworząc dimery lub wyższe oligomery, co utrudnia ich izolację.
- Przemiany redoks i dalsze przekształcenia — tioaldehydy mogą być utleniane, redukowane lub przekształcane dalej do pochodnych siarkowych; mechanizmy zależą od warunków reakcji i zastosowanych reagentów.
Ogólnie tiale są więc bardzo reaktywne i często wykorzystywane jako krótkożyjące intermediates w reakcjach syntetycznych. Ich aktywność sprawia, że są cennymi reagentami w badaniach metodologicznych, ale rzadko spotyka się je jako trwałe związki użytkowe.
Synteza i metody przygotowania
Ze względu na dużą reaktywność tioaldehydów, często przygotowuje się je in situ (bez izolowania) i natychmiast zużywa w kolejnych etapach syntezy. Do przemiany grupy karbonylowej (C=O) w tiokarbonylową (C=S) stosuje się powszechnie reagenty tiolujące, takie jak Lawesson's reagent lub siarczek fosforu (P4S10). Te odczynniki przekształcają aldehydy i ketony w odpowiednie związki tiokarbonylowe; jednak izolacja wolnych tiali jest możliwa tylko dla wybranych, sterycznie utrudnionych lub specjalnie stabilizowanych związków.
Inne techniki stosowane przy badaniach tiali obejmują niskotemperaturowe warunki, izolację matrycową (matrix isolation) lub użycie bardzo nieporęcznych, objętościowych podstawników R, które zapobiegają samorzutnej dimeryzacji.
Stabilizacja i czynniki wpływające na trwałość
- Steryka — duże, nieporęczne grupy R hamują zbliżanie się cząsteczek i zmniejszają skłonność do dimerów; to jedna z najskuteczniejszych strategii stabilizacji.
- Efekty elektronowe — podstawienie elektronodonorowe lub -akceptorowe może modyfikować elektrofilowość atomu węgla i wpływać na stabilność; w praktyce stabilniejsze bywają niektóre tioketony i tioestry niż proste tiale.
- Warunki przechowywania — przechowywanie w niskiej temperaturze i w atmosferze obojętnej (np. azot, argon) oraz unikanie wilgoci i światła przedłuża żywotność wrażliwych tiozwiązków.
Porównanie z tioketonami
Jeśli atom wodoru (H) przy grupie C(S)H zostanie zastąpiony przez inną grupę organiczną R, powstaje tioketon. Tioketony są na ogół bardziej stabilne niż tioaldehydy, ponieważ brak protonu aldehydowego ogranicza możliwość wielu rodzajów niepożądanych reakcji (np. kondensacji czy łatwej oligomeryzacji).
Zastosowania i znaczenie
Tioaldehydy mają przede wszystkim znaczenie w badaniach organicznych i fizykochemicznych jako bardzo reaktywne intermediates w syntezach złożonych cząsteczek, w badaniach cykloaddycji oraz przy wprowadzaniu jednostek siarkowych do struktur organicznych. Ze względu na trudności z izolacją, wiele zastosowań opiera się na ich generowaniu in situ i natychmiastowym wykorzystaniu w kolejnych etapach syntez.
Podsumowując: tiale (tioaldehydy) to analogi aldehydów z siarką zamiast tlenu przy funkcji karbonylowej; cechują się wysoką reaktywnością (zwłaszcza jako elektrofile i dienofile), łatwo ulegają dimeryzacji i wymagają specjalnych technik syntezy i przechowywania. Przy zastąpieniu wodoru grupą R powstają tioketony, które są zwykle bardziej stabilne.