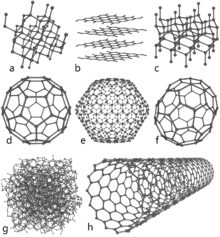
Istnieje kilka alotropów węgla. Diament i grafit są najbardziej znane. Grafit jest przewodnikiem, semimetalem (pierwiastkiem, który jest częściowo metalem i niemetalem, jak czarny fosfor i szary selen). Może być stosowany np. jako materiał w elektrodach lampy łukowej. Grafit jest najbardziej stabilną formą stałego węgla, jaką kiedykolwiek odkryto. Poniżej opisano te i inne formy, ich strukturę, właściwości oraz typowe zastosowania.
Co to jest alotropia?
Allotropy są różnymi formami tego samego pierwiastka chemicznego. Wszystkie pierwiastki składają się w unikalny sposób z własnych atomów. Wszelkie różnice fizyczne wynikają z tego, jak atomy są ze sobą połączone. Wiele pierwiastków wykazuje alotropię, ponieważ istnieje wiele sposobów, w jaki atomy mogą być ze sobą połączone. Istnieją również różne sposoby ułożenia cząsteczek w celu uzyskania większych struktur. Zmiana hybrydyzacji atomów węgla (sp3, sp2, sp) wpływa bezpośrednio na twardość, przewodnictwo elektryczne, przewodnictwo cieplne i właściwości optyczne materiału.
Główne formy alotropowe węgla
- Diament (Diament) – sieć krystaliczna oparta na hybrydyzacji sp3. Atomy węgla tworzą tetraedryczne wiązania, co daje wyjątkową twardość i wysoką przewodność cieplną. Diament jest najtwardszym znanym naturalnym minerałem, dzięki czemu sprawdza się jako materiał ścierny i narzędziowy. Jego wysoka dyspersja światła i połysk czynią go cenionym w biżuterii. Diament ma bardzo wysoką temperaturę topnienia (w praktyce sublimacji) i dobrze zachowuje swój blask.
- Grafit (grafit) – warstwowa struktura oparta na hybrydyzacji sp2. Pojedyncza warstwa to grafen; warstwy są słabo związane siłami van der Waalsa, co pozwala na łatwe ścieranie i smarowanie. Grafit przewodzi prąd elektryczny w płaszczyźnie warstw i jest odporny na wysokie temperatury, dlatego znajduje zastosowanie jako elektrody czy materiały ogniotrwałe.
- Grafen – pojedyncza warstwa atomów węgla ułożonych w sześciokąty (siatka heksagonalna). Ma wyjątkową wytrzymałość mechaniczną, wysokie przewodnictwo elektryczne i cieplne oraz unikatowe właściwości optyczne. Grafen jest wykorzystywany w badaniach nad elektroniką, czujnikami, kompozytami i magazynowaniem energii.
- Fullereny (np. C60) – molekularne struktury w kształcie kulistym lub elipsoidalnym. Mają zastosowania w chemii materiałowej, medycynie (badania nad dostarczaniem leków) i elektronice ze względu na unikatowe właściwości elektronowe.
- Nanorurki węglowe (CNT) – cylindryczne struktury zbudowane z nawijającego się grafenu. Wyróżniają się ogromną wytrzymałością na rozciąganie, niską masą oraz dobrym przewodnictwem elektrycznym i cieplnym. Stosowane są w kompozytach, elektronice i nanotechnologii.
- Węgiel amorficzny – obejmuje sadzę, węgiel aktywny, koks i węgiel drzewny. Nie posiada regularnej struktury krystalicznej. Węgiel aktywny wykorzystywany jest m.in. do oczyszczania wody i gazów oraz w adsorpcji zanieczyszczeń.
- Lonsdaleit (heksagonalny diament) – rzadki alotrop powstający m.in. w skałach meteorytowych. Ma strukturę heksagonalną i według badań może być równie twardy lub twardszy od diamentu.
Właściwości wynikające ze struktury
- Hybrydyzacja – sp3 (diament) daje twardość i izolację elektryczną; sp2 (grafit, grafen) zapewnia przewodnictwo i plastyczność warstw; sp (nieliczne formy liniowe) prowadzi do innych specyficznych właściwości.
- Przewodnictwo – grafen i grafit przewodzą prąd wzdłuż warstw; diament jest izolatorem elektrycznym, ale domieszkowany może przewodzić.
- Przewodność cieplna – diament ma jedno z najwyższych przewodnictw cieplnych spośród materiałów naturalnych; grafen również wykazuje doskonałe przewodnictwo cieplne w płaszczyźnie.
- Wytrzymałość mechaniczna – diament i nanomateriałowe formy (grafen, CNT) charakteryzują się wyjątkową twardością i wytrzymałością na rozciąganie.
- Stabilność termodynamiczna – w normalnych warunkach grafit jest termodynamicznie stabilniejszy niż diament; diament może przekształcić się w grafit w ekstremalnych warunkach długotrwałego ogrzewania przy niskim ciśnieniu.
Zastosowania praktyczne
- Diament – biżuteria, narzędzia skrawające i ścierne, końcówki wiertnicze, elementy optyczne w zastosowaniach przemysłowych, wysokoprzewodzące podłoża cieplne w elektronice.
- Grafit – elektrody (np. w lampach łukowych i piecach elektrycznych), smary suche, materiały ogniotrwałe, elemnty w bateriach i ogniwach paliwowych, czarny pigment i składnik kompozytów.
- Grafen i nanorurki – zaawansowane kompozyty, elastyczna elektronika, czujniki, materiały przewodzące, magazynowanie energii (superkondensatory, baterie), potencjalne zastosowania w medycynie i filtracji.
- Fullereny – badania w nanomedycynie, elektronice molekularnej, materiałach optoelektronicznych oraz katalizie.
- Węgiel aktywny – oczyszczanie powietrza i wody, adsorpcja toksyn, filtracja przemysłowa.
Tworzenie i pozyskiwanie
Różne alotropy powstają w różny sposób: diament naturalny tworzy się pod bardzo wysokim ciśnieniem i temperaturą w głębi Ziemi, natomiast syntetyczne diamenty produkuje się metodami takimi jak wysokie ciśnienie–wysoka temperatura (HPHT) oraz chemiczne osadzanie z fazy gazowej (CVD). Grafen uzyskuje się m.in. poprzez eksfoliację mechaniczna grafitu, syntezę CVD lub chemiczną redukcję tlenku grafenu. Fullereny i nanorurki powstają m.in. w procesach wyładowań łukowych, ablacji laserowej czy metodach CVD.
Podsumowanie
Alotropia węgla pokazuje, jak jedna liczba protonów i elektronów w atomie może dać bardzo różnorodne materiały o skrajnie odmiennych właściwościach — od najtwardszego naturalnego minerału (diamentu), przez miękki, przewodzący grafit, po nanostruktury o obiecujących zastosowaniach w zaawansowanej technologii. Zrozumienie zależności między strukturą a właściwościami pozwala wykorzystać te formy w przemyśle, elektronice, medycynie i ochronie środowiska.