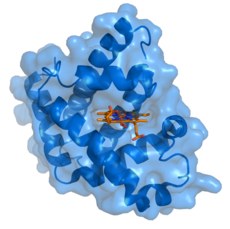
Ligand jest substancją biochemiczną. Jego zadaniem jest związanie się z cząsteczką biologiczną i sprawienie, by ta cząsteczka spełniała jakąś funkcję. Wiązanie ligandu zmienia kształt białka receptora. Zmienia to zachowanie białka.
W węższym znaczeniu jest to cząsteczka wyzwalająca sygnał, wiążąca się z miejscem na docelowym białku.
Wiązanie zachodzi dzięki siłom międzycząsteczkowym, takim jak wiązania jonowe, wiązania wodorowe i siły van der Waalsa. Dokowanie (asocjacja) jest zazwyczaj odwracalne (dysocjacja).
Ligandy to substraty, inhibitory, aktywatory i neuroprzekaźniki. Tendencja lub siła wiązania nazywana jest powinowactwem.
Co to jest ligand — rozszerzona definicja
W szerszym ujęciu ligand to dowolna cząsteczka (lub jon, atom) zdolna do specyficznego wiązania z większą cząsteczką biologiczną, najczęściej białkiem (receptorem, enzymem), ale także z kwasem nukleinowym lub z membraną. Ligand może wywoływać efekt funkcjonalny (np. aktywować receptor) albo go blokować. Mogą to być związki endogenne (np. hormony, neuroprzekaźniki, jony) albo związki egzogenne (leki, trucizny).
Rodzaje ligandów
- Agoniści — wiążą się z receptorem i aktywują jego funkcję.
- Antagoniści — wiążą się z receptorem, blokując dostęp agonisty i zapobiegając aktywacji.
- Inhibitory — hamują aktywność enzymów (mogą być konkurencyjne, niekonkurencyjne lub allosteryczne).
- Aktywatory — zwiększają aktywność białka lub enzymu.
- Substraty — cząsteczki, na których działają enzymy (są przemieszczane lub modyfikowane).
- Ligandy allosteryczne — wiążą się w miejscu odległym od miejsca aktywnego i modulują funkcję białka.
- Ligandy kowalencyjne — wiążą się trwale (np. niektóre inhibitory enzymów); większość ligandów oddziałuje niekowalencyjnie przy użyciu sił międzycząsteczkowych.
Mechanizm działania
Wiązanie ligandu do miejsca na białku (np. do miejsca aktywnego enzymu lub do domeny receptora) zmienia konformację białka. Ta zmiana struktury może:
- bezpośrednio uruchomić kaskadę sygnałową (np. receptor metabotropowy);
- zmienić aktywność enzymatyczną (przyspieszyć lub zahamować reakcję);
- umożliwić lub blokować interakcje z innymi białkami.
Wiązanie odbywa się dzięki kombinacji sił: wiązaniom jonowym, wiązaniom wodorowym, oddziaływaniom hydrofobowym i siłom van der Waalsa. Dokowanie (asocjacja) bywa odwracalne — ligand może się dysocjować. W przypadku wiązań kowalencyjnych dysocjacja jest rzadko możliwa i takie interakcje są zwykle nieodwracalne.
Powinowactwo i kinetyka wiązania
Powinowactwo opisuje, jak silnie ligand wiąże się z receptorem. Często używaną miarą jest stała dysocjacji Kd (im mniejsza Kd, tym wyższe powinowactwo). W kategoriach kinetycznych Kd = k_off / k_on, gdzie k_on to szybkość asocjacji, a k_off — szybkość dysocjacji. Ligand o niskim k_off pozostaje dłużej związany z receptorem.
Specyficzność odnosi się do tego, jak selektywnie ligand wiąże się z jednym typem miejsca względem innych możliwości wiązania. Wysoka specyficzność zmniejsza ryzyko efektów ubocznych w kontekście leków.
Kowariancja i kooperatywność: w oligomerycznych białkach (np. hemoglobinie) wiązanie jednego ligandu może zmieniać powinowactwo pozostałych miejsc — to zjawisko nazywamy kooperatywnością.
Przykłady ligandów i znaczenie biologiczne
- Neuroprzekaźniki (np. dopamina, serotonina) — ligandy receptorów synaptycznych.
- Hormony (np. adrenalina, insulina) — ligandy receptorów komórkowych regulujących metabolizm i odpowiedzi fizjologiczne.
- Leki (np. beta-blokery, inhibitory ACE) — ligandy terapeutyczne projektowane do modulacji funkcji białek.
- Substraty enzymatyczne i kofaktory (np. ATP, NAD+) — niezbędne do reakcji enzymatycznych.
- Jony metali (np. Ca2+, Zn2+) — ligandy ważne dla struktury i funkcji wielu białek.
Metody badania interakcji ligand–receptor
Do analizy wiązania ligandów używa się technik takich jak:
- SPR (Surface Plasmon Resonance) — badanie kinetyki (k_on, k_off) i powinowactwa;
- ITC (calorimetria izotermiczna) — pomiar energii wiązania i stechiometrii;
- Badania wiązania radioligandów lub fluorescencyjne assay — określanie Kd i liczby miejsc wiązania;
- Strukturalne metody — krystalografia rentgenowska, NMR, cryo-EM — pozwalają zobaczyć miejsce wiązania i konformację białka;
- Medycyna i farmakologia — testy komórkowe, modele in vivo do oceny efektów biologicznych.
Znaczenie w farmakologii i biotechnologii
Ligandy stanowią podstawę terapii farmakologicznej — leki są projektowane jako ligandy o odpowiednim powinowactwie i selektywności. Rozumienie mechanizmów wiązania pomaga w optymalizacji skuteczności leku i ograniczaniu działań niepożądanych. W biotechnologii ligandy służą też jako znaczniki, inhibitory enzymów, czy narzędzia do modulacji aktywności białek.
Kluczowe podsumowanie: ligand to cząsteczka wiążąca się specyficznie z inną cząsteczką biologiczną, wpływająca na jej funkcję. Istotne cechy to rodzaj oddziaływania (agonista/antagonista), powinowactwo i kinetyka wiązania oraz specyficzność — wszystkie te parametry mają decydujące znaczenie w biologii i projektowaniu leków.