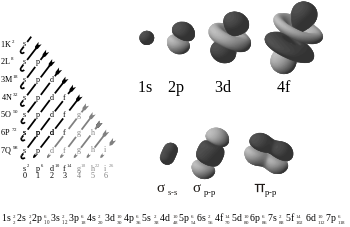
W chemii wiązania pi (wiązania π) są kowalentnymi wiązaniami chemicznymi, powstającymi wskutek bocznego nakładania się orbitali. Zwykle bierze w nich udział orbital typu p — ściana orbitalna jednego elektronu (czyli orbital jednego atomu) nakłada się równolegle na orbital drugiego atomu, tworząc dwa obszary nakładania się: nad i pod osią łączącą jądra. Tylko jedna z węzłowych płaszczyzn orbitala przechodzi przez oba zaangażowane jądra, co odróżnia wiązanie π od wiązania σ (sigma).
Symetria i udział orbitali
Grecka litera π w nazwie odnosi się do udziału orbitali p. Symetria wiązania π odpowiada symetrii orbitalu p przy patrzeniu wzdłuż osi wiązania — elektronowa chmura ma dwa przeciwległe płaty, a wzdłuż osi między jądrami znajduje się płaszczyzna węzłowa o zerowej gęstości elektronowej. Orbital p najczęściej tworzy wiązania π, jednak także orbity d mogą uczestniczyć w tworzeniu wiązań π (szczególnie w związkach metali przejściowych); takie efekty są istotne przy opisie hiperwalencji i sprzężeń π (np. π-backbonding).
Budowa i typy wiązań wielokrotnych
Wiązanie π występuje zwykle jako uzupełnienie wiązania σ w wiązaniach wielokrotnych:
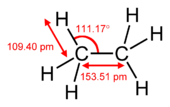
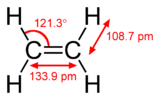
- wiązanie podwójne: jedno σ + jedno π (np. etylen, C2H4),
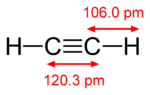
- wiązanie potrójne: jedno σ + dwa π (np. acetylen, C2H2).
Właściwości i konsekwencje chemiczne
Wiązania π są zwykle słabsze od obligacji sigma, ponieważ zakres nakładania orbitalnego jest mniejszy — orbitaly p są ustawione równolegle, więc ich nakładanie boczne jest mniej efektywne niż nakładanie czołowe orbitalów tworzących wiązanie σ. Mechanika kwantowa opisuje to jako mniejszą integralną wartość nakładania orbitali, co skutkuje mniejszym obniżeniem energii przy tworzeniu wiązania π.
Jednocześnie dodanie wiązania π do pojedynczego wiązania zwiększa całkowitą siłę i skraca długość wiązania między atomami (więcej wiązań = wyższy rząd wiązania), mimo że każdy komponent π jest słabszy niż σ. Elektrony uczestniczące w wiązaniu π są często nazywane elektronami pi i mają istotne znaczenie dla właściwości elektronowych związków.
Rotacja i izomeria
Fragmenty molekularne połączone przez wiązanie π nie mogą swobodnie obracać się wokół tego wiązania bez jego zerwania. Obrót niszczy równoległe ułożenie dwóch orbitali p i przerywa nakładanie boczne, dlatego wiązanie π ogranicza rotację — stąd możliwa jest izomeria geometryczna (np. cis–trans) przy wiązaniach podwójnych.
Delokalizacja i znaczenie w chemii organicznej
W systemach sprzężonych (ciągłych nakładających się orbitalach p) elektrony π mogą ulegać delokalizacji na kilka atomów, co prowadzi do stabilizacji przez rezonans i powstawania układów aromatycznych (np. benzen). Delokalizowane elektrony π wpływają na barwę związków (absorpcja w UV‑Vis), reaktywność (preferencje dla podstawień elektrofilowych zamiast addycji w pierścieniach aromatycznych) i właściwości przewodzące w materiałach organicznych.
Podsumowując, wiązania π są kluczowym elementem budowy i reaktywności wielu związków chemicznych — chociaż pojedyncze π wiązanie jest słabsze niż σ, to w połączeniu z innymi wiązaniami wpływa znacząco na geometrię, stabilność i właściwości elektronowe cząsteczek.