Chromatografia gazowa - spektrometria mas
Chromatografia gazowa - spektrometria mas (GC-MS) łączy w sobie cechy chromatografii gazowo-cieczowej (GC) i spektrometrii mas (MS). Pozwala to na identyfikację różnych substancji w badanej próbce. GC-MS ma wiele zastosowań, w tym wykrywanie narkotyków, badania przeciwpożarowe, analizy środowiskowe i badania materiałów wybuchowych. Może być również wykorzystywana do identyfikacji nieznanych próbek. GC-MS może być również wykorzystywany w ochronie lotniska do wykrywania substancji w bagażu lub na ludziach. Dodatkowo, GC-MS może zidentyfikować pierwiastki śladowe w zniszczonych materiałach, nawet po tym jak próbka rozpadnie się na tyle, że inne testy nie będą mogły zadziałać.
GC-MS jest najlepszym sposobem dla ekspertów kryminalistycznych na identyfikację substancji, ponieważ jest to specyficzny test. Specyficzne badanie pozytywnie identyfikuje rzeczywistą obecność danej substancji w danej próbce. W badaniu niespecyficznym stwierdza się jedynie, że w próbce znajdują się kategorie substancji. Chociaż niespecyficzne badanie może statystycznie sugerować tożsamość substancji, może to prowadzić do fałszywej identyfikacji pozytywnej.

Przykład urządzenia GC-MS
Historia
Pierwsze prace badawcze z zakresu chromatografii gazowo-cieczowej zostały opublikowane w 1950 roku. Chemicy używali różnych detektorów, aby stwierdzić, że związki wypływają z końca chromatografu. Większość detektorów niszczyła te związki, ponieważ je spalały lub jonizowały. Detektory te pozostawiły chemików, odgadując dokładną tożsamość każdego związku w próbce. W latach 50-tych, Roland Gohlke i Fred McLafferty opracowali nową, połączoną maszynę. Użyli spektrometru masowego jako detektora w chromatografii gazowej. Te wczesne urządzenia były duże, kruche i początkowo ograniczone do ustawień laboratoryjnych.
Projekt był skomplikowany. Odstęp czasowy pomiędzy różnymi związkami wypływającymi z chromatografu był trudny do kontrolowania. Tak więc spektrometr masowy musiał zakończyć pracę nad jednym związkiem, zanim kolejny wypłynął z chromatografu. We wczesnych modelach, pomiary ze spektrometru masowego były rejestrowane na papierze graficznym. Wysoko wykwalifikowani chemicy badali wzorce pików w celu identyfikacji każdego związku. Do lat siedemdziesiątych XX wieku do spektrometrów masowych dodawano przetworniki analogowo-cyfrowe. Pozwoliło to komputerom na przechowywanie i interpretację wyników. W miarę jak komputery stawały się coraz mniejsze, GC-MS stawał się coraz szybszy i rozprzestrzeniał się z laboratoriów na codzienne życie. Obecnie skomputeryzowane przyrządy GC-MS są szeroko stosowane w monitoringu środowiskowym wody, powietrza i gleby. Jest on również wykorzystywany w regulacji rolnictwa, bezpieczeństwa żywności oraz w odkrywaniu i produkcji leków.
Rozwój małych komputerów przyczynił się do uproszczenia maszyn GC-MS. Znacznie skrócił również czas potrzebny na analizę próbki. Electronic Associates, Inc. (EAI) była wiodącym amerykańskim dostawcą komputerów analogowych. W 1964 roku EAI rozpoczęło prace nad komputerowo sterowanym spektrometrem masowym pod kierownictwem Roberta E. Finnigana. Do 1966 r. sprzedano ponad 500 przyrządów do analizatorów gazowych. W 1967 roku utworzono Finnigan Instrument Corporation (FIC). Na początku 1968 roku dostarczono pierwsze prototypowe czworokątne instrumenty GC-MS do Stanford i Purdue University. Ostatecznie FIC zmienił nazwę na Finnigan Corporation i stał się światowym liderem w dziedzinie systemów GC-MS.
Podstawowe działanie
GC-MS może znaleźć wszystkie związki zmieszane razem w obiekcie próbki. Operator rozpuszcza próbkę w cieczy. Następnie operator wtryskuje ciecz do strumienia gazu. (Najczęściej używany jest hel, wodór lub azot.) Gaz przepływa przez rurkę ze specjalną powłoką. Ponieważ każdy związek zawarty w próbce przykleja się do powłoki w inny sposób, każdy związek wychodzi z rurki w innym czasie. Tak więc powłoka jest używana do oddzielenia każdego związku, który został zmieszany w próbce. Ponieważ każdy związek wychodzi na końcu rurki, jest on zjonizowany i otrzymuje ładunek elektryczny. Większość związków rozpada się, gdy są one zjonizowane. Poszczególne elementy lecą pod magnesem, który oddziela je na podstawie ich wagi i ładunku. Następnie komputer mierzy wszystkie kawałki każdego związku. Porównując pomiary z komputerową biblioteką znanych związków, komputer sporządza listę nazw wszystkich związków w próbce. Komputer może również określić, ile każdego ze związków było w próbce.
Oprzyrządowanie
GC-MS składa się z dwóch głównych elementów konstrukcyjnych: chromatografu gazowego i spektrometru masowego. W chromatografie gazowym wykorzystuje się kolumnę kapilarną, która zależy od jej wymiarów (długość, średnica, grubość warstwy) oraz właściwości fazowych (np. 5% polisiloksan fenylu). Różnica we właściwościach chemicznych pomiędzy różnymi cząsteczkami w mieszaninie będzie rozdzielać cząsteczki w miarę przemieszczania się próbki po długości kolumny. Cząsteczki te potrzebują różnej ilości czasu (zwanego czasem retencji), aby wyjść z (eluować z) chromatografu gazowego. Dzięki temu spektrometr masowy znajdujący się za nim może wychwytywać, jonizować, przyspieszać, odbijać i wykrywać zjonizowane cząsteczki oddzielnie. Spektrometr masowy robi to poprzez rozbijanie każdej cząsteczki na zjonizowane fragmenty i wykrywanie tych fragmentów przy użyciu ich stosunku masy do ładunku.
Te dwie maszyny, używane razem, pozwalają na znacznie większą precyzję identyfikacji substancji niż każda z nich używana osobno. Nie jest możliwa dokładna identyfikacja konkretnej molekuły wyłącznie za pomocą chromatografii gazowej lub spektrometrii mas. Proces spektrometrii masowej wymaga zazwyczaj bardzo czystej próbki. W przeszłości w chromatografii gazowej stosowano inne detektory, takie jak detektor jonizacji płomieniowej. Detektory te nie są w stanie rozdzielić różnych molekuł, które w tym samym czasie przechodzą przez kolumnę. (Gdy dwie różne molekuły mają ten sam czas retencji, mówi się o nich "co-elute"). Co-elute molekuły będą mylić programy komputerowe, które odczytują pojedyncze spektrum masy dla obu cząsteczek.
Czasami dwie różne molekuły mogą mieć również podobny wzór zjonizowanych fragmentów w spektrometrze masowym (widmo masowe). Połączenie tych dwóch procesów zmniejsza możliwość popełnienia błędu. Jest bardzo mało prawdopodobne, aby dwie różne molekuły zachowywały się w ten sam sposób zarówno w chromatografie gazowym jak i spektrometrze masowym. Dlatego, jeżeli widmo masowe pasuje do badanego analitu, czas retencji tego widma można sprawdzić w odniesieniu do charakterystycznego czasu retencji GC w celu zwiększenia pewności, że analit znajduje się w próbce.
Rodzaje detektorów spektrometrów masowych
Najczęstszym typem MS związanym z GC jest kwadrupolowy spektrometr masowy. Hewlett-Packard (obecnie Agilent) sprzedaje go pod nazwą handlową "Mass Selective Detector" (MSD). Innym stosunkowo popularnym detektorem jest spektrometr masowy z pułapką jonową. Dodatkowo można znaleźć spektrometr masowy w sektorze magnetycznym. Jednak te konkretne przyrządy są drogie i nieporęczne i zazwyczaj nie są spotykane w wysokowydajnych laboratoriach serwisowych. Inne detektory są używane, takie jak czas lotu (TOF), kwadrupony tandemowe (MS-MS) (patrz poniżej), lub w przypadku pułapki jonowej MSn. Litera n oznacza liczbę etapów spektrometrii masowej.

Wewnątrz GC-MS, z kolumną chromatografu gazowego w piecu po prawej stronie.
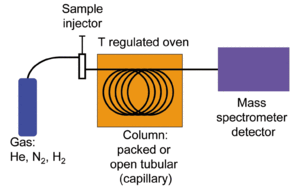
Schemat GC-MS
Analiza
Spektrometr masowy jest zwykle używany na jeden z dwóch sposobów: Pełne skanowanie lub selektywne monitorowanie jonów (SIM). Typowy GC-MS może pracować zarówno samodzielnie, jak i jednocześnie.
Pełny skan MS
Podczas zbierania danych w trybie pełnego skanowania wybiera się docelowy zakres fragmentów masy i wprowadza do metody urządzenia. Przykładem typowego szerokiego zakresu fragmentów masy do monitorowania jest m/z 50 do m/z 400. Określenie, jaki zakres ma być użyty, jest w dużej mierze uzależnione od tego, czego oczekuje się od obecności w próbce, mając jednocześnie świadomość istnienia rozpuszczalnika i innych możliwych zakłóceń. Jeżeli państwo członkowskie poszukuje fragmentów masy o bardzo niskiej wartości m/z, może ono wykryć powietrze lub inne możliwe czynniki zakłócające. Użycie dużego zakresu skanowania zmniejsza czułość urządzenia. Urządzenie będzie wykonywać mniej skanów na sekundę, ponieważ każde skanowanie zajmie więcej czasu na wykrycie szerszego zakresu fragmentów masy.
Pełny skan jest przydatny przy oznaczaniu nieznanych związków w próbce. Dostarcza on więcej informacji niż SIM, jeśli chodzi o potwierdzanie lub rozdzielanie związków w próbce. Większość instrumentów jest sterowana przez komputer, który obsługuje program komputerowy zwany "metodą instrumentalną". Metoda instrumentalna kontroluje temperaturę w GC, szybkość skanowania MS i zakres wykrytych wielkości fragmentów. Kiedy chemik opracowuje metodę instrumentalną, wysyła roztwory testowe przez GS-MS w trybie pełnego skanowania. Sprawdza to czas retencji GC i masowy odcisk palca fragmentu przed przejściem na metodę przyrządu SIM. Specjalistyczne przyrządy GC-MS, takie jak detektory materiałów wybuchowych, posiadają fabrycznie załadowaną metodę przyrządu.
Wybrane monitorowanie jonów
W wybranym monitoringu jonowym (SIM), metoda instrumentu skupia się na pewnych fragmentach jonów. Tylko te fragmenty masy są wykrywane przez spektrometr masowy. Zaletą SIM jest to, że granica wykrywalności jest niższa, ponieważ podczas każdego skanowania przyrząd patrzy tylko na niewielką liczbę fragmentów (np. trzy fragmenty). W każdej sekundzie może nastąpić więcej skanów. Ponieważ monitorowanych jest tylko kilka interesujących fragmentów masowych, zakłócenia matrycowe są zazwyczaj mniejsze. Aby zwiększyć szanse na prawidłowy odczyt pozytywnego wyniku, proporcje jonów różnych fragmentów masowych są porównywalne ze znanym standardem odniesienia.
Rodzaje jonizacji
Po przejściu przez kolumnę cząsteczek, przechodzą one przez linię transferową i wchodzą do spektrometru masowego, są jonizowane różnymi metodami. Zazwyczaj w danym momencie stosuje się tylko jedną metodę jonizacji. Po rozdrobnieniu próbki jest ona wykrywana, zwykle przez diodę mnożnika elektronów. Dioda ta traktuje zjonizowany fragment masy jak sygnał elektryczny, który jest następnie wykrywany.
Chemicy wybierają technikę jonizacji oddzielnie od wyboru Full Scan lub monitoringu SIM.
Jonizacja elektronów
Najczęstszym rodzajem jonizacji jest jonizacja elektronowa (EI). Cząsteczki wchodzą do MS (źródłem jest kwadrupol lub sama pułapka jonowa w MS pułapki jonowej), gdzie są uderzane swobodnymi elektronami emitowanymi z włókna. Jest to żarnik, który można by znaleźć w standardowej żarówce. Elektrony uderzają w cząsteczki, powodując ich fragmentację w charakterystyczny sposób, który może być powtarzany. Ta technika "twardej jonizacji" powoduje powstawanie większej ilości fragmentów o niskim stosunku masy do ładunku (m/z). EI ma niewiele, jeśli w ogóle, fragmentów o masie zbliżonej do masy pierwotnej cząsteczki. Chemicy uważają, że twarda jonizacja to strzelanie elektronami w cząsteczki próbki. Natomiast "jonizacja miękka" polega na umieszczeniu ładunku na cząsteczce próbki poprzez uderzenie w nią wprowadzonym gazem. Wzorzec fragmentacji molekularnej zależy od energii elektronów przyłożonej do układu, zazwyczaj 70 eV (elektronowoltów). Zastosowanie 70 eV pomaga porównać widma generowane z badanej próbki ze znanymi widmami bibliotecznymi. (Widma biblioteczne mogą pochodzić z oprogramowania dostarczonego przez producenta lub oprogramowania opracowanego przez National Institute of Standards (NIST-USA)). Oprogramowanie przeszukuje widma biblioteki za pomocą algorytmu dopasowującego, takiego jak Probability Based Matching lub dot-product matching. Wiele agencji zajmujących się standaryzacją metod kontroluje obecnie te algorytmy i metody, aby zapewnić ich obiektywność.
Jonizacja chemiczna
W chemicznej jonizacji (CI) do spektrometru masowego wprowadza się gaz odczynnikowy, zwykle metan lub amoniak. Istnieją dwa rodzaje CI: CI dodatni lub ujemny CI. W obu przypadkach gaz odczynnikowy wchodzi w interakcję z elektronami i analitem i powoduje "miękką" jonizację interesującej go cząsteczki. Miękka jonizacja fragmentów molekuły w mniejszym stopniu niż twarda jonizacja EI. Chemicy wolą CI niż EI. Dzieje się tak, ponieważ CI wytwarza co najmniej jeden masowy fragment o masie, która jest prawie taka sama jak masa cząsteczkowa analizowanego analitu.
Pozytywna jonizacja chemiczna
W dodatniej jonizacji chemicznej (PCI) gaz odczynnikowy wchodzi w interakcję z cząsteczką docelową, najczęściej z wymianą protonów. W ten sposób gatunek jonu wytwarza stosunkowo duże ilości.
Negatywna jonizacja chemiczna
W Negatywnej Jonizacji Chemicznej (NCI) gaz odczynnikowy zmniejsza wpływ wolnych elektronów na docelowy analit. Ta zmniejszona energia zazwyczaj pozostawia fragment w dużej ilości. (Fragmenty nie rozpadają się dalej).
Tłumaczenie ustne
Podstawowym celem analizy instrumentów jest pomiar ilości substancji. Dokonuje się tego poprzez porównanie względnych stężeń pomiędzy masami atomowymi w wytworzonym spektrum masowym. Możliwe są dwa rodzaje analizy, porównawcza i oryginalna. Analiza porównawcza zasadniczo porównuje dane widmo do biblioteki widm, aby sprawdzić czy jego charakterystyka jest obecna dla jakiejś znanej próbki w bibliotece. Analizę tę najlepiej przeprowadzić na komputerze, ponieważ istnieje wiele zniekształceń wizualnych, które mogą wystąpić w związku z różnicami w skali. Komputery mogą również skorelować więcej danych (takich jak czas retencji określony przez GC), aby dokładniej powiązać pewne dane.
Inna metoda analizy mierzy wartości szczytowe w stosunku do siebie. W tej metodzie najwyższy pik jest ustawiony na 100%. Pozostałym pikom nadano wartość równą stosunkowi wysokości piku do wysokości najwyższego piku. Wszystkie wartości powyżej 3% są przypisane. Całkowita masa nieznanego związku jest zazwyczaj wskazywana przez pik macierzysty. Wartość tego piku macierzystego może być użyta w celu dopasowania do wzoru chemicznego zawierającego różne pierwiastki, które są uważane za wchodzące w skład związku. Wzór izotopowy w spektrum jest unikalny dla pierwiastków, które mają wiele izotopów. Tak więc, może on być również używany do identyfikacji różnych pierwiastków obecnych. To mówi ogólny wzór chemiczny nieznanej cząsteczki. Ponieważ struktura cząsteczki i wiązania rozrywają się w charakterystyczny sposób, można je zidentyfikować na podstawie różnicy w masie piku. Zidentyfikowana struktura molekuły musi być zgodna z charakterystyką zarejestrowaną przez GC-MS. Zazwyczaj identyfikacja ta jest wykonywana automatycznie przez programy komputerowe, które są dostarczane z urządzeniem. Programy te dopasowują widma do biblioteki znanych związków, które mają tę samą listę pierwiastków, które mogą być obecne w próbce.
Analiza "pełnego spektrum" uwzględnia wszystkie "szczyty" w ramach danego spektrum. Ale selektywne monitorowanie jonów (SIM) monitoruje tylko wybrane szczyty związane z konkretną substancją. Chemicy zakładają, że w danym czasie retencji, zestaw jonów jest charakterystyczny dla danego związku. SIM to szybka i skuteczna analiza. SIM działa najlepiej, gdy analityk ma wcześniejszą informację o próbce lub szuka tylko kilku konkretnych substancji. Gdy ilość informacji zebranych o jonach w danym piku chromatografii gazowej zmniejsza się, wzrasta czułość analizy. Tak więc, analiza SIM pozwala na wykrycie i pomiar mniejszej ilości związku. Zmniejsza się jednak stopień pewności co do tożsamości tego związku.
GC-tandem MS
Gdy dodana jest druga faza fragmentacji masy, na przykład przy użyciu drugiego kwadrupolu w przyrządzie kwadrupolowym, nazywa się to tandem MS (MS/MS). MS/MS są dobre w mierzeniu niskich poziomów związków docelowych w próbce z matrycą związków tła, które nie są przedmiotem zainteresowania.
Pierwszy kwadrupol (Q1) jest połączony z komórką zderzeniową (q2) i kolejnym kwadrupolami (Q3). Oba kwadrupole mogą być używane w trybie skanowania lub statycznym, w zależności od rodzaju stosowanej analizy MS/MS. Typy analiz obejmują skanowanie jonów produktu, skanowanie jonów prekursorów, monitorowanie wybranych reakcji (SRM) oraz skanowanie strat neutralnych. Na przykład: Gdy Q1 znajduje się w trybie statycznym (patrząc tylko na jedną masę jak w SIM), a Q3 w trybie skanowania, uzyskuje się tzw. widmo jonów produktowych (zwane również "widmem pochodnym"). Z tego widma można wybrać wybitny jon iloczynowy, który może być jonem iloczynowym dla wybranego jonu prekursora. Para ta nazywana jest "przejściem" i stanowi podstawę dla SRM. SRM jest wysoce specyficzny i prawie całkowicie eliminuje tło matrycy.
Aplikacje
Monitorowanie i oczyszczanie środowiska
Wielu chemików uważa, że GC-MS jest najlepszym narzędziem do monitorowania zanieczyszczeń organicznych w środowisku. Koszt urządzeń GC-MS znacznie się obniżył. Jednocześnie wzrosła niezawodność GC-MS. Oba ulepszenia zwiększyły wykorzystanie w badaniach środowiskowych. Niektóre związki, takie jak niektóre pestycydy i herbicydy, nie mogą być zidentyfikowane przez GS-MS. Są one zbyt podobne do innych związków pokrewnych. Jednak w przypadku większości organicznych analiz próbek środowiskowych, w tym wielu głównych klas pestycydów, GC-MS jest bardzo czuły i skuteczny.
Kryminalistycy sądowi
GC-MS może analizować cząsteczki z ludzkiego ciała, aby pomóc powiązać przestępcę z przestępstwem. Prawo dopuszcza wykorzystanie GC-MS do analizy szczątków pożarowych. Amerykańskie Stowarzyszenie Badań Materiałów Palnych (ASTM) posiada normę dotyczącą analizy odpadów pożarowych. GCMS/MS jest tu szczególnie przydatny, ponieważ próbki często zawierają bardzo złożone matryce, a wyniki, stosowane w sądzie, muszą być bardzo dokładne.
Egzekwowanie prawa
GC-MS jest używany do wykrywania nielegalnych narkotyków i może ostatecznie zastąpić psy węszące narkotyki. Jest również powszechnie stosowany w toksykologii kryminalistycznej. Pomaga znaleźć narkotyki i/lub trucizny w próbkach biologicznych pobranych od podejrzanych, ofiar lub martwych ciał.
Bezpieczeństwo
Po atakach terrorystycznych z 11 września 2001 r. systemy wykrywania materiałów wybuchowych stały się częścią wszystkich amerykańskich lotnisk. Systemy te działają w oparciu o wiele technologii, wiele z nich opartych jest na GC-MS. Istnieje tylko trzech producentów certyfikowanych przez FAA jako dostawcy tych systemów. Pierwszym z nich jest Thermo Detection (dawniej Thermedics), który produkuje EGIS, linię detektorów materiałów wybuchowych opartych na GC-MS. Drugi to Barringer Technologies, który jest obecnie własnością Smith's Detection Systems. Trzecia to Ion Track Instruments (część General Electric Infrastructure Security Systems).
Analiza żywności, napojów i perfum
Żywność i napoje zawierają wiele związków aromatycznych, niektóre z nich są naturalnie obecne w surowcach, a niektóre tworzą się podczas przetwarzania. GC-MS jest szeroko stosowany do analizy tych związków, w tym estrów, kwasów tłuszczowych, alkoholi, aldehydów, terpenów itp. Stosuje się go również do wykrywania i pomiaru zanieczyszczeń pochodzących z psucia się lub zafałszowania, które mogą być szkodliwe. Zanieczyszczenia te są często kontrolowane przez agencje rządowe, na przykład pestycydy.
Astrochemia
Kilka GC-MS-ów opuściło ziemię. Dwa poszły na Marsa w programie Wikingów. Wenera 11 i 12 oraz Pioneer Venus analizowały atmosferę Wenus z GC-MS. Sonda Huygens z misji Cassini-Huygens wylądowała jeden GC-MS na największym księżycu Saturna, Tytanie. Materiał w komecie 67P/Churyumov-Gerasimenko będzie analizowany przez misję Rosetta z chiralnym GC-MS w 2014 roku.
Medycyna
GC-MS są stosowane w badaniach przesiewowych noworodków. W testach tych można wykryć dziesiątki wrodzonych chorób metabolicznych (tzw. wrodzonych błędów w przemianie materii). GC-MS może oznaczać związki w moczu nawet w bardzo małych ilościach. Związki te zazwyczaj nie są obecne, ale pojawiają się u osób z zaburzeniami metabolicznymi. Staje się to powszechnym sposobem diagnozowania IEM dla wcześniejszej diagnozy i rozpoczęcia leczenia. Prowadzi to w końcu do lepszego wyniku. Obecnie możliwe jest przebadanie noworodka na ponad 100 genetycznych zaburzeń metabolicznych za pomocą testu moczu w momencie urodzenia na podstawie GC-MS.
W połączeniu z izotopowym oznaczaniem związków metabolicznych, GC-MS jest wykorzystywany do określania aktywności metabolicznej. Większość zastosowań opiera się na wykorzystaniu 13C do znakowania i pomiaru stosunku 13C-12C za pomocą spektrometru masowego stosunku izotopowego (IRMS). IRMS jest spektrometrem masowym z detektorem przeznaczonym do pomiaru kilku wybranych jonów i wartości powrotnych jako stosunków.
Pytania i odpowiedzi
P: Co to jest chromatografia gazowa ze spektrometrią mas (GC-MS)?
O: Chromatografia gazowa ze spektrometrią mas (GC-MS) to technika łącząca chromatografię gazowo-cieczową (GC) i spektrometrię mas (MS) w celu identyfikacji różnych substancji w badanej próbce.
P: Jakie są niektóre zastosowania GC-MS?
GC-MS ma wiele zastosowań, w tym wykrywanie narkotyków, badanie pożarów, analiza środowiska i badanie materiałów wybuchowych. Może być również używany do identyfikacji nieznanych próbek.
P: Czy GC-MS może być stosowany w ochronie lotniska?
O: Tak, GC-MS może być stosowany w ochronie lotniska do wykrywania substancji w bagażu lub na ludziach.
P: Jakie są korzyści ze stosowania GC-MS w kryminalistyce?
GC-MS to najlepszy sposób identyfikacji substancji przez ekspertów medycyny sądowej, ponieważ jest to test specyficzny. Konkretny test pozytywnie identyfikuje rzeczywistą obecność określonej substancji w danej próbce.
P: Jaka jest różnica między testem specyficznym a niespecyficznym?
O: Test specyficzny pozytywnie identyfikuje rzeczywistą obecność konkretnej substancji w danej próbce, podczas gdy test niespecyficzny mówi tylko, że w próbce znajdują się kategorie substancji.
P: Czy GC-MS może zidentyfikować pierwiastki śladowe w zniszczonych materiałach?
O: Tak, GC-MS może zidentyfikować pierwiastki śladowe w zniszczonych materiałach, nawet po tym, jak próbka rozpadła się tak bardzo, że inne testy nie mogą działać.
P: Jakie jest ryzyko użycia niespecyficznego testu do identyfikacji substancji?
O: Chociaż niespecyficzny test może statystycznie sugerować tożsamość substancji, może to prowadzić do fałszywie pozytywnej identyfikacji.
Przeszukaj encyklopedię