Enzymy to cząsteczki białka w komórkach, które działają jak biologiczne katalizatory. Enzymy przyspieszają reakcje chemiczne w organizmie, ale nie zużywają się w tym procesie, dlatego mogą być wielokrotnie wykorzystywane. Dzięki swojej budowie i właściwościom obniżają energię aktywacji reakcji, co pozwala na przebieg procesów biochemicznych w warunkach panujących w komórkach.
Prawie wszystkie reakcje biochemiczne w organizmach żywych wymagają enzymów. Dzięki enzymowi reakcje chemiczne przebiegają znacznie szybciej niż bez niego. p39 Innymi biokatalizatorami są katalityczne cząsteczki RNA, zwane rybozymami.
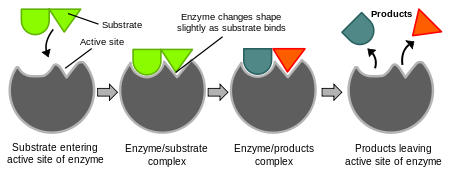
Substancje znajdujące się na początku reakcji nazywamy substratami. Substancje znajdujące się na końcu reakcji to produkty. Enzymy wiążą substraty w tzw. miejscu aktywnym i przekształcają je w produkty, po czym mogą ponownie uczestniczyć w kolejnych cyklach katalizy. Nauka o enzymach nazywana jest enzymologią.
Budowa enzymów i specyficzność
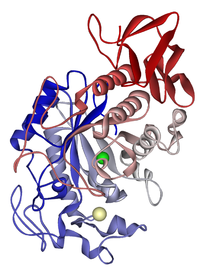
Większość enzymów jest zbudowana z jednego lub więcej łańcuchów polipeptydowych, których przestrzenne ułożenie tworzy miejsce aktywne — miejsce wiązania substratu. Do prawidłowego działania niektórych enzymów potrzebne są dodatkowe elementy zwane kofaktorami. Mogą to być jony metali (np. Zn2+, Mg2+) lub organiczne cząsteczki zwane koenzymami (np. NAD+, FAD). Jeśli kofaktor jest trwale związany z enzymem, nazywa się on grupą prostetyczną.
Specyficzność enzymu oznacza, że dany enzym rozpoznaje określony substrat lub grupę substratów — mówi się o specyficzności substratowej. Klasyczne modele wyjaśniające wiązanie enzym–substrat to model „klucza i zamka” oraz model „indukowanego dopasowania”, w którym enzym zmienia konformację przy wiązaniu substratu, optymalizując katalizę.
Mechanizm działania
Enzymy przyspieszają reakcje poprzez obniżenie energii aktywacji i stabilizację stanu przejściowego. Mechanizmy, które to umożliwiają, obejmują:
- zmniejszenie odległości pomiędzy substratami,
- odpowiednie ułożenie substratów względem siebie,
- tworzenie środowiska chemicznego sprzyjającego reakcji (np. przenoszenie protonów),
- tymczasowe tworzenie i rozrywanie wiązań między enzymem a substratem.
W biochemii często używa się opisu kinetycznego reakcji enzymatycznych, w tym równań Michaelisa–Menten, które wprowadzają parametry takie jak Vmax (maksymalna prędkość reakcji) i Km (stała Michaelisa, miara powinowactwa enzymu do substratu).
Czynniki wpływające na aktywność enzymów
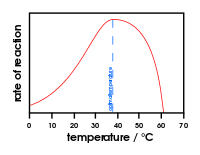
- Temperatura: wzrost temperatury zwykle zwiększa szybkość reakcji do czasu, gdy białko nie ulegnie denaturacji; większość enzymów ma optymalne zakresy temperaturowe.
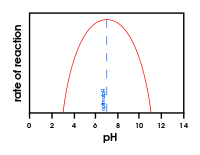
- pH: zmiany pH wpływają na jonizację grup funkcyjnych reszt aminokwasowych, co może prowadzić do utraty aktywności. Enzymy mają różne optimum pH (np. pepsyna w żołądku działa najlepiej w kwaśnym środowisku).
- Stężenie substratu: wzrost stężenia substratu zwiększa szybkość reakcji aż do osiągnięcia nasycenia enzymu.
- Inhibitory: substancje hamujące aktywność enzymów — mogą być odwracalne (konkurencyjne, niekonkurencyjne, niezależne) lub nieodwracalne (trwale modyfikujące enzym).
Regulacja aktywności enzymatycznej
Organizmy regulują aktywność enzymów na wiele sposobów, aby kontrolować szlaki metaboliczne:
- Regulacja allosteryczna: modulatory (aktywatory lub inhibitory) wiążą się w miejscach innych niż aktywne, zmieniając konformację enzymu.
- Modyfikacje kowalencyjne: np. fosforylacja/dezfosforylacja, które włączają lub wyłączają aktywność enzymu.
- Kontrola ekspresji genów: zmiana ilości syntetyzowanego enzymu przez regulację transkrypcji i translacji.
- Sprzężenie zwrotne (feedback): końcowy produkt szlaku metabolicznego może hamować enzymy na wczesnym etapie tego szlaku.
Przykłady i znaczenie
Przykładowe enzymy to amylaza (rozkłada skrobię), pepsyna (trawi białka w żołądku), lipazy (rozkładają tłuszcze), kinazy i dehydrogenazy (uczestniczą w przenoszeniu grup i elektronów w metabolizmie). Enzymy są kluczowe w:
- metabolizmie komórkowym i produkcji energii (np. enzymy oddychania komórkowego),
- trawieniu i wchłanianiu składników odżywczych,
- replikacji i naprawie DNA (polimerazy, ligazy),
- przemysłowych zastosowaniach: w przemyśle spożywczym, detergentowym, farmaceutycznym i biotechnologii (np. enzymy w produkcji serów, wytwarzaniu bioetanolu, enzymy stosowane w diagnostyce).
Znaczenie medyczne
Zaburzenia aktywności enzymów mogą prowadzić do chorób metabolicznych (np. fenyloketonuria — brak enzymu przekształcającego fenyloalaninę). Enzymy są także istotnymi celami leków — wiele leków działa jako inhibitory specyficznych enzymów patogenu lub szlaku metabolicznego gospodarza. W diagnostyce oznaczanie aktywności enzymów (np. enzymów wątrobowych) pomaga w wykrywaniu uszkodzeń narządów.
Nazewnictwo i klasyfikacja
Większość enzymów nosi nazwy zakończone przyrostkiem „-aza” (np. laktoza → laktaza), a Międzynarodowa Komisja Enzymatyczna nadaje numery klasyfikacyjne (EC) według typu katalizowanej reakcji.
Pierwszy enzym został odkryty w 1833 roku przez Anselme Payena.
Oprócz enzymów białkowych, jak wspomniano wcześniej, istnieją również enzymatyczne cząsteczki RNA — rybozymy — które pełnią ważne funkcje katalityczne w komórkach. Badania nad enzymami wciąż rozwijają się, dostarczając nowych narzędzi w medycynie, biotechnologii i ochronie środowiska.