Reakcja SN1 jest reakcją substytucji w chemii organicznej. "SN" oznacza substytucję nukleofilową, a "1" oznacza fakt, że etap determinujący szybkość reakcji obejmuje tylko jedną cząsteczkę (jednocząsteczkowy). Reakcja obejmuje pośredni związek karbokationowy. Niektóre powszechne reakcje SN1 dotyczą drugorzędowych lub trzeciorzędowych halogenków alkilowych w warunkach silnie zasadowych lub, w warunkach silnie kwasowych, drugorzędowych lub trzeciorzędowych alkoholi. W przypadku pierwszorzędowych halogenków alkilowych zachodzi alternatywna reakcjaSN2. Wśród chemików nieorganicznych, reakcja SN1 jest często znana jako mechanizm dysocjacyjny. Christopher Ingold et al. po raz pierwszy zaproponował mechanizm reakcji w 1940 roku.
Mechanizm — krok po kroku
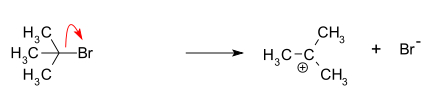
- Krok I: jonizacja (tworzenie karbokationu) — etap wolniejszy i determinujący szybkość; wiąże się z odejściem grupy opuszczającej (np. halogenu) i powstaniem karbokationu oraz anionu. To jednocząsteczkowe rozpadanie decyduje o tym, że szybkość zależy tylko od stężenia substratu: v = k[substrat].
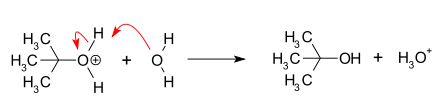
- Krok II: atak nukleofila — szybki etap, w którym nukleofil przyłącza się do płaskiego karbokationu, tworząc produkt substytucji.
- Dodatkowe etapy — w zależności od warunków mogą wystąpić przemieszczenia (np. przesunięcie hydridowe lub alkilowe), protonacje/deprotonacje lub tworzenie związków pośrednich (np. jonów sprzężonych z rozpuszczalnikiem).
Czynniki wpływające na przebieg i szybkość reakcji
- Stabilność karbokationu: reakcja preferuje substraty tworzące stabilne karbokationy (trzeciorzędowe > drugorzędowe > pierwszorzędowe; także efekty rezonansowe zwiększają stabilizację).
- Grupa opuszczająca: dobra grupa opuszczająca (np. I−, Br−, tosylat) ułatwia etap jonizacji.
- Rozpuszczalnik: polarne, proticzne rozpuszczalniki (np. H2O, alkohole) stabilizują karbokation i anion, sprzyjając mechanizmowi SN1.
- Siła nukleofila: w SN1 szybkość zależy słabo od nukleofila — nawet słabe nukleofile mogą efektywnie reagować, ponieważ etap ograniczający szybkość to jonizacja.
- Temperatura: wyższa temperatura sprzyja zazwyczaj eliminacji (E1) kosztem substytucji; warunki kinetyczne i termodynamiczne decydują o udziale poszczególnych ścieżek.
Stereochemia i przesunięcia
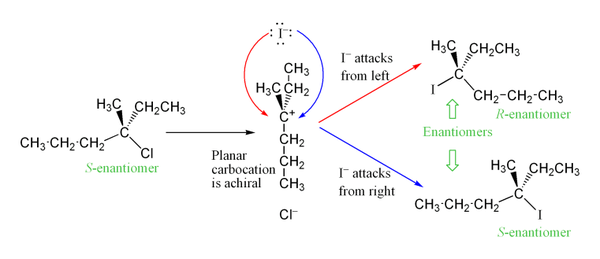
- Racemizacja: jeśli centrum stereogeniczne ulega karbokationowi, jego planarna struktura prowadzi zazwyczaj do mieszaniny enancjomeryczną (racemizacja). Często jednak obserwuje się częściową retencję lub inwersję z powodu tzw. par jonowych (ion pairs) i udziału ukierunkowanego ataku nukleofila.
- Przemieszczenia: karbokationy mogą ulegać przesunięciom (hydrydowym lub alkilowym), prowadząc do produktów, które wynikają z bardziej stabilnego karbokationu — ważne przy przewidywaniu struktury produktu.
- Udział grup sąsiednich: tzw. neighboring group participation (anchimeric assistance) może przyspieszać reakcję i wpływać na stereochemię produktu.
Konkurencyjne procesy i typowe przykłady
- Konkurencja z E1: w podobnych warunkach często zachodzi Eliminacja E1; wyższa temperatura i słabe nukleofile sprzyjają E1.
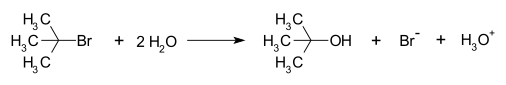
- Typowe substraty: trzeciorzędowe halogenki alkilowe i protonowane alkohole (w warunkach kwasowych, gdy OH staje się dobrą grupą opuszczającą) — dla alkoholi etap inicjujący to protonacja OH, a następnie odejście wody i powstanie karbokationu.
- Przykład reakcji: solvoliza tert-bromku izopropylu w wodzie prowadzi do tert-butanolu (przez pośredni karbokation i atak rozpuszczalnika).
Podsumowanie
Reakcja SN1 to dwustopniowy mechanizm nukleofilowej substytucji, którego kluczową cechą jest jednocząsteczkowy etap determinujący szybkość — tworzenie karbokationu. Jej przebieg zależy głównie od stabilności karbokationu, jakości grupy opuszczającej oraz od właściwości rozpuszczalnika; siła nukleofila odgrywa mniejszą rolę niż w mechanizmie SN2. Ze względu na możliwe przemieszczenia i racemizację, przewidywanie produktów wymaga uwzględnienia zarówno kinetyki, jak i termodynamiki oraz efektów stereochemicznych.