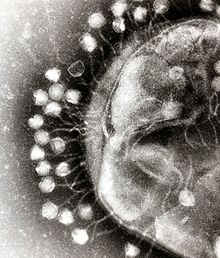
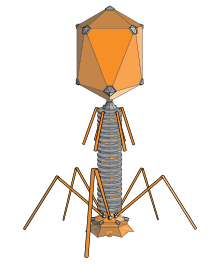
Bakteriofag to wirus, który infekuje bakterie. Termin ten jest powszechnie skracany do fagów. Fagi występują w ogromnej różnorodności morfologicznej i genetycznej — niektóre przypominają „bakteriofiltry” z główką i ogonem, inne mają kształt kulisty lub filamentowy.
Budowa i genom
Fagi są zazwyczaj zbudowane z zewnętrznego kadłuba białkowego (tzw. kapsydu), który chroni materiał genetyczny znajdujący się w środku. W przypadku wielu fagów (szczególnie z rodziny Myoviridae, Siphoviridae i Podoviridae) kapsyd jest połączony z ogonem, kończącym się płytką podstawową i włókienkami, które rozpoznają receptory na powierzchni komórek bakteryjnych.
Materiał genetyczny fagów może być jedno‑ lub dwuniciowy: ssRNA, ssDNA, dsRNA lub dsDNA. Genomy mogą mieć układ liniowy lub kolisty i obejmować różne rozmiary — najczęściej od kilku do kilkuset kilobaz par nukleotydów. Typowo Genomy fagowe mogą kodować od kilku do nawet setek genów, w zależności od rodzaju faga. Fagi mają zwykle rozmiary od 20 do 200 nanometrów.
Cykl życia
Typowy przebieg zakażenia polega na przyłączeniu do powierzchni bakterii, a następnie wstrzyknięciu genomu w bakterię. Po wprowadzeniu genomu fagi wykorzystują mechanizmy gospodarza do replikacji i produkcji nowych cząstek wirusowych.
- Cykl lityczny: fag szybko replikuje swój genom, produkuje kapsydy i białka ogona oraz powoduje lizę (rozpad) komórki bakteryjnej, uwalniając potomne cząstki.
- Cykl lizogeniczny (temperatny): fag włącza swój genom do chromosomu bakterii jako profag (provirus) i replikuje się wraz z komórką gospodarza; pod wpływem określonych czynników profag może się aktywować i przejść w cykl lityczny.
- Inne strategie: istnieją również cykle przewlekłe (bez lizy, ciągłe uwalnianie wirionów) oraz stany pseudolizogenne.
Rola ekologiczna i występowanie
Fagi są wszędzie tam, gdzie są bakterie — w glebie, w osadach, w układzie pokarmowym organizmów oraz w wodach: słodkich i morskich. Są one bardzo powszechne w wodzie morskiej: w gęstych skupiskach mikroorganizmów, np. w matach mikrobiologicznych na powierzchni, stwierdzono do 9×10^8 wirusów na mililitr, a do 70% bakterii morskich może być zakażonych przez fagi. Dzięki niszczeniu i przemianie organizmów bakterii fagi odgrywają istotną rolę w obiegu materii — uwalniają związki organiczne do kolistego obiegu w ekosystemie, wpływając na cykle biogeochemiczne i dynamikę populacji bakteryjnych.
Poprzez mechanizmy takie jak transdukcja fagi uczestniczą w poziomym transferze genów, co może prowadzić do rozpowszechniania genów oporności czy czynników wirulencji w populacjach bakterii.
Zastosowania i znaczenie dla medycyny i biotechnologii
Od ponad 90 lat są one stosowane jako alternatywa dla antybiotyków w byłym Związku Radzieckim i Europie Środkowej, a także we Francji. Początki terapii fagowej sięgają prac Felixa d'Herelle z początku XX wieku; udało się też już w 1939 r. potwierdzić strukturalną naturę fagów dzięki obserwacjom pod mikroskopem elektronowym autorstwa Helmuta Ruski.
Współcześnie fagi zyskują na znaczeniu jako potencjalna terapia przeciwko odpornym na antybiotyki szczepom bakterii. Zastosowania obejmują:
- Terapia fagowa — stosowanie pojedynczych fagów lub koktajli fagowych do leczenia zakażeń bakteryjnych (w tym przypadków, gdzie antybiotyki zawodzą); prowadzonych jest coraz więcej badań klinicznych i przypadków ratunkowego użycia.
- Usuwanie biofilmów — wiele fagów może rozkładać macierz biofilmu i zabijać komórki bakteryjne, co ma znaczenie w medycynie i przemyśle (np. dezynfekcja urządzeń). Jednocześnie niektóre fagi mogą modyfikować biofilmy lub przenosić geny, co w niektórych warunkach może komplikować zakażenia (patrz niżej).
- Biotechnologia — systemy takie jak phage display pozwalają na selekcję białek o pożądanych właściwościach; fagi są też wykorzystywane do wykrywania szczepów bakteryjnych, do dekontaminacji żywności oraz jako nośniki w inżynierii genetycznej bakterii.
- Nauka o odporności — odkrycie systemu CRISPR jako bakteryjnego mechanizmu obronnego przeciw fagom miało ogromne znaczenie dla biologii molekularnej i technologii edycji genomu.
Zalety i ograniczenia terapii fagowej
- Zalety: wysoka selektywność wobec patogenów (nie zabijają komórek eukariotycznych ani korzystnej mikroflory poza wąskim spektrum gospodarza), możliwość dopasowania koktajli fagowych, potencjalna efektywność wobec szczepów opornych na antybiotyki.
- Ograniczenia i ryzyka: wąskie spektrum hostowe (konieczność identyfikacji odpowiedniego faga), możliwy transfer genów przez fagową transdukcję (w tym genów oporności i czynników wirulencji), reakcje immunologiczne organizmu pacjenta, uwalnianie endotoksyn po masowej lizie bakterii. Ponadto standaryzacja, produkcja, testy bezpieczeństwa i regulacje prawne są nadal w trakcie rozwoju w wielu krajach.
Fagi a biofilmy i choroby
Fagi mają złożony wpływ na biofilmy: wiele fagów produkuje enzymy rozkładające polisacharydy macierzy biofilmu, co ułatwia penetrację i eliminację bakterii. Z drugiej strony, niektóre fagowe interakcje mogą wzmacniać odporność bakterii w biofilmie lub przenosić geny, które zwiększają przyleganie i przeżywalność — tak dzieje się m.in. w niektórych zakażeniach dróg oddechowych i u pacjentów z mukowiscydozą, gdzie biofilm Pseudomonas aeruginosa jest istotnym czynnikiem przewlekłego zapalenia płuc (zapaleniem płuc).
Metody badawcze i wykrywanie fagów
Do izolacji i identyfikacji fagów używa się klasycznych technik mikrobiologicznych (np. testu stref zahamowania wzrostu — plaque assay), mikroskopii elektronowej, sekwencjonowania genomów oraz badań proteomicznych. Określanie zakresu gospodarzy, analiza genomowa pod kątem genów potencjalnie szkodliwych i testy bezpieczeństwa są kluczowe przed zastosowaniem terapeutycznym.
Perspektywy i wnioski
Fagi są istotnym elementem biosfery i mają duży potencjał w medycynie oraz biotechnologii. W miarę narastania problemu oporności na antybiotyki rośnie zainteresowanie fagoterapią i fagami jako narzędziami diagnostycznymi i leczniczymi. Jednocześnie konieczne są dalsze badania nad bezpieczeństwem, standardami produkcji, mechanizmami interakcji fag–gospodarz oraz nad sposobami minimalizacji ryzyka przenoszenia niepożądanych genów.