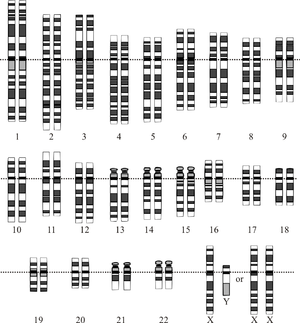
Ludzki genom zapisany jest na 23 parach chromosomów w jądrze komórkowym oraz w małym mitochondrialnym DNA. Wiele wiadomo już o sekwencjach DNA, które znajdują się na naszych chromosomach. Częściowo wiadomo też, co tak naprawdę robi DNA. Zastosowanie tej wiedzy w praktyce dopiero się zaczyna.
Budowa i podstawowe informacje
Genom człowieka to kompletna informacja genetyczna zapisane w postaci sekwencji nukleotydów (A, T, C, G). W przybliżeniu haploidalny genom ludzkiego dorosłego człowieka zawiera około 3–3,2 miliarda par zasad. Chromosomy występują w komórkach somatycznych w postaci 23 par: 22 par autosomów oraz para płciowa (XX u kobiet, XY u mężczyzn). Dodatkowo komórki zawierają mitochondrialne DNA — małą, kolistą cząsteczkę (~16,6 kb), która koduje kilka niezbędnych białek łańcucha oddechowego oraz RNA.
- Około 20–25 tysięcy genów koduje białka; są to tzw. geny kodujące białka. Jednak całkowita liczba transkryptów (RNA) jest większa dzięki istnieniu wielu ncRNA (niekodujących RNA), alternatywnemu składaniu eksonów i innym zjawiskom.
- Jedynie niewielka część genomu — rzędu 1–2% — bezpośrednio koduje sekwencje białek. Reszta to introny, sekwencje regulatorowe, powtórzenia i elementy niekodujące, które mogą mieć funkcję strukturalną lub regulacyjną.
- Pojawiają się liczne elementy powtarzalne i ruchome (np. LINE, SINE, transpozony), które razem stanowią znaczną część genomu (blisko 40–50%).
Regulacja i organizacja funkcjonalna
Funkcja genów zależy od złożonego systemu regulacji: promotory, enhancery, czynniki transkrypcyjne, modyfikacje histonów i metylacja DNA wpływają na to, które geny są włączone w danym typie komórki i w danym czasie. Trójwymiarowa organizacja chromatyny (np. domeny TAD — topologically associating domains) umożliwia kontakt między odległymi elementami regulatorowymi a genami, co ma kluczowe znaczenie dla prawidłowej ekspresji genów.
Human Genome Project (HGP) — sekwencja referencyjna
W ramach projektu Human Genome Project opracowano sekwencję referencyjną, która jest wykorzystywana na całym świecie w biologii i medycynie. Nature opublikowało raport z projektu finansowanego ze środków publicznych, a Science opublikowało pracę firmy Celera. Prace te opisywały, w jaki sposób powstał projekt sekwencji i przedstawiały jej analizę.
HGP rozpoczął się na początku lat 90. XX w.; pierwszy roboczy szkic referencyjny genomu człowieka ogłoszono w 2001 r. (dalsze poprawki i uzupełnienia doprowadziły w latach 2003 i 2005 do wersji roboczych obejmujących do ≈92% sekwencji). Publiczne i prywatne podejścia nieco się różniły — publiczny konsorcjum stosowało mapowanie klonów i sekwencjonowanie, podczas gdy firma Celera wykorzystała metodę shotgun. Efektem prac HGP są m.in. znormalizowane odniesienia (kolejne wersje referencyjnych genomów, np. GRCh37, GRCh38), które służą jako „mapa” dla badań genetycznych i medycznych.
W kolejnych dekadach społeczność naukowa uzupełniała luki: istotnym osiągnięciem jest praca konsorcjum Telomere-to-Telomere (T2T), które w 2022 r. przedstawiło praktycznie kompletną sekwencję ludzkiego genomu (T2T-CHM13), wypełniając wiele wcześniej nieodczytanych regionów, takich jak centromery i długie powtórzenia.
Równolegle HGP zainicjował program ELSI (ethical, legal and social implications) — badania i dyskusje nad konsekwencjami społecznymi sekwencjonowania genomu, prywatnością, dostępem do danych oraz możliwą dyskryminacją genetyczną.
Projekt ENCODE — co to bada i dlaczego jest ważny
Najnowszy projekt ENCODE (Encyclopedia of DNA Elements) ma na celu zidentyfikowanie i zmapowanie elementów funkcjonalnych w ludzkim genomie — nie tylko genów kodujących białka, lecz też regulatorów, miejsc wiązania czynników transkrypcyjnych, modyfikacji chromatyny, transkryptów niekodujących i innych „elementów” wykazujących aktywność biochemiczną.
ENCODE wykorzystuje metody wysokoprzepustowe, m.in.:
- RNA-seq do wykrywania transkryptów (również niedawno odkrytych długich ncRNA i krótkich RNA),
- ChIP-seq do mapowania miejsc wiązania białek i modyfikacji histonów,
- DNase-seq / ATAC-seq do identyfikacji regionów otwartej chromatyny (potencjalnie aktywnych regulatorowo),
- techniki 3D (np. Hi-C) do badania przestrzennej organizacji genomu.
Jednym z najbardziej dyskutowanych wyników pierwszych odsłon ENCODE (2012) była deklaracja, że znacząca część genomu wykazuje "aktywność biochemiczną" — co media przedstawiły jako stwierdzenie, że 80% genomu ma funkcję. To wywołało debatę naukową: krytycy zwracali uwagę, że aktywność biochemiczna (np. chwilowe wiązanie białka lub jednorazowy transkrypt) nie musi oznaczać biologicznie istotnej, wyewoluowanej funkcji. Późniejsze analizy i kolejne wydania ENCODE lepiej rozróżniły pojęcia „biochemiczna aktywność” od „funkcji biologicznej” rozumianej przez selekcję ewolucyjną.
Zastosowania praktyczne i dalsze kierunki
Mapa referencyjna genomu i zasoby tworzone przez projekty typu ENCODE mają wiele praktycznych zastosowań:
- interpretacja wariantów związanych z chorobami — wiele wariantów wykrywanych w badaniach GWAS znajduje się nie w genach, lecz w regionach regulatorowych; mapy ENCODE pomagają określić, które warianty mogą wpływać na ekspresję genów,
- onkologia — sekwencjonowanie nowotworów i analiza zmian regulacyjnych pomagają odnaleźć kierunki terapii celowanej,
- medycyna spersonalizowana i farmakogenomika — lepsze zrozumienie funkcji genów i regulatorów umożliwia dostosowanie terapii do pacjenta,
- biotechnologia i inżynieria genetyczna — znajomość sekwencji i regulatorów ułatwia projektowanie konstrukcji genetycznych i terapii opartych na CRISPR.
Wyzwania i etyka
Mimo postępów wiele zagadnień pozostaje otwartych: pełne zrozumienie funkcji większości regionów genomu, interpretacja wariantów rzadkich, znaczenie epigenetyki i interakcji gen‑środowisko. Równocześnie rozwój technologii wymusza stałą dyskusję o ochronie prywatności danych genetycznych, odpowiedzialnym udostępnianiu wyników oraz zapobieganiu dyskryminacji na tle genetycznym.
Podsumowując: sekwencja ludzkiego genomu oraz badania takie jak ENCODE przekształciły biologię i medycynę, dostarczając ramy do zrozumienia, jak zapis genetyczny jest wykorzystywany i regulowany w komórkach. Praca nad pełnym zrozumieniem genomu trwa nadal — kolejne technologie i analizy danych wciąż odsłaniają nowe poziomy złożoności.