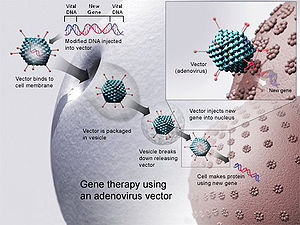
Terapia genowa to metoda leczenia polegająca na wprowadzeniu działającego genu do organizmu osoby, która ma uszkodzony lub brakujący gen. Celem jest przywrócenie prawidłowej funkcji komórek przez dostarczenie poprawnej kopii genu albo modyfikację aktywności istniejącego genu. Metoda ta może dotyczyć pojedynczych komórek, tkanek lub narządów i jest stosowana przede wszystkim w chorobach o uwarunkowaniu genetycznym.
Jak to działa?
W najprostszym ujęciu terapia genowa polega na dostarczeniu do komórek pacjenta materiału genetycznego, który zostanie odczytany i przetłumaczony na działający białkowy produkt. Do przeniesienia genu używa się nośników nazywanych wektorami; najczęściej są to zmodyfikowane wirusy, które utraciły zdolność do wywoływania choroby, ale nadal potrafią wprowadzić materiał genetyczny do komórek. W leczeniu produktem Glybera wykorzystuje się wirusa do zainfekowania komórek mięśniowych działającą kopią genu.
W zależności od techniki, proces może wyglądać tak:
- przygotowanie wektora niosącego "poprawny" gen,
- dostarczenie wektora do organizmu (in vivo) lub poza organizmem — do komórek pobranych od pacjenta (ex vivo), które następnie się wszczepia z powrotem,
- ekspresja dostarczonego genu w komórkach docelowych i uzyskanie terapeutycznego efektu.
Rodzaje wektorów i technik
Najczęściej stosowane wektory to:
- wektory oparte na wirusach AAV (adeno‑associated virus) — często wykorzystywane ze względu na niską immunogenność i względne bezpieczeństwo,
- wektory adenowirusowe — dają silną, ale zwykle przejściową ekspresję, mogą wywoływać reakcje immunologiczne,
- wektory lentivirusowe — integrują się z genomem gospodarza, co zapewnia dłuższą ekspresję, ale wiąże się z ryzykiem insercji w niepożądane miejsce,
- metody bezwirusowe: liposomy, nanopartikty, bezpośrednie wprowadzenie DNA/RNA — używane tam, gdzie wymagana jest niższa immunogenność lub prostsza produkcja.
Używany w ten sposób wirus jest wektorem. Oznacza to, że jest nośnikiem; gen został wprowadzony do wirusowego genomu, a wirus wprowadza go do ludzkich komórek. Technika ta nosi nazwę transfekcji. Technika ta różni się od techniki nokautu genowego, która nie wykorzystuje wektora wirusowego i polega na bezpośredniej edycji genomu (np. z użyciem narzędzi typu CRISPR/Cas).
Przykład: Glybera
Jednym z najszerzej znanych przykładów terapii genowej jest Glybera (alipogene tiparvovec) — terapia opracowana dla rzadkiej choroby genetycznej niedoboru lipazy lipoproteinowej (LPL). Jedna na milion osób ma uszkodzone kopie genu lipazy potrzebnego do rozkładania tłuszczów. W rezultacie tłuszcz gromadzi się we krwi, co prowadzi do nawracających, zagrażających życiu epizodów zapalenia trzustki. Do czasu wprowadzenia terapii genowej podstawowym sposobem leczenia była dieta o bardzo niskiej zawartości tłuszczu.
W preparacie Glybera zastosowano wektor AAV, który przenosił funkcjonalną kopię genu LPL do mięśni pacjenta, gdzie gen ten był następnie ekspresowany. Komisja Europejska zatwierdziła dopuszczenie Glybery do obrotu jako pierwszej terapii genowej w Unii Europejskiej (decyzja ta miała duże znaczenie symboliczne). W praktyce jednak terapia ta była rzadko stosowana, a producent ostatecznie wycofał preparat z rynku z powodów komercyjnych.
Inne przykłady i obszary zastosowań
W ostatnich latach zatwierdzono kolejne terapie genowe i pokrewne terapie komórkowe, m.in.:
- terapie lecznicze dla dziedzicznych chorób siatkówki (np. voretigene neparvovec, znany jako Luxturna),
- terapie systemowe dla rdzeniowego zaniku mięśni (np. onasemnogene abeparvovec, znany jako Zolgensma),
- terapie CAR‑T, czyli modyfikowane genetycznie limfocyty T (np. Kymriah, Yescarta) stosowane w niektórych nowotworach — są to przykłady terapii ex vivo.
Korzyści, zagrożenia i ograniczenia
Terapia genowa oferuje potencjał do leczenia chorób wcześniej nieuleczalnych, a w niektórych przypadkach może dawać długotrwałą lub nawet jednorazową kurację. Jednak wiąże się też z ryzykami i ograniczeniami:
- odpowiedź immunologiczna — organizm może rozpoznać wektor jako obce i zniszczyć go lub zainicjować stan zapalny,
- insercja w niepożądane miejsce (insertional mutagenesis) — integrujące wektory mogą aktywować onkogeny lub inaktywować geny supresorowe,
- przejściowość efektu — niektóre terapie nie integrują genu z genomem, więc efekt może być tymczasowy i wymagać ponownego podania,
- wysokie koszty — produkcja i opracowanie terapii genowych są kosztowne, co przekłada się na bardzo wysoką cenę leczenia,
- ograniczona dostępność i wskazania — wiele terapii jest przeznaczonych dla małych grup pacjentów z konkretnymi mutacjami, co utrudnia szerokie zastosowanie.
Regulacje i aspekty etyczne
Terapie genowe podlegają ścisłym regulacjom i wymagają wieloetapowych badań klinicznych. W większości krajów dozwolone są interwencje w komórkach somatycznych (zmiany nie przekazywane potomstwu), natomiast edycja germinalna (zmiany w komórkach rozrodczych) jest powszechnie zabroniona lub bardzo ograniczona ze względów etycznych.
Podsumowanie
Terapia genowa to rosnący i obiecujący obszar medycyny, który już przyniósł pierwsze zatwierdzone terapie i zmienił sposób leczenia niektórych chorób genetycznych. Jednocześnie wiąże się z wyzwaniami naukowymi, bezpieczeństwa i kosztów. Rozwój technologii wektorowych oraz metod edycji genów (np. CRISPR) nadal przyspiesza postęp, ale każda nowa metoda wymaga dokładnej oceny ryzyka i korzyści.