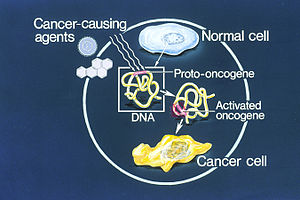
Onkogen jest genem, który ma potencjał do wywoływania raka. Innymi słowy, onkogen to gen, którego aktywacja prowadzi do niekontrolowanego podziału komórek i zaburzeń kontroli cyklu komórkowego. W normalnych warunkach odpowiedniki onkogenów — proto-onkogeny — regulują wzrost, różnicowanie i przeżycie komórek; stają się onkogenami po zmianach, które zwiększają ich aktywność lub ilość białka, które kodują.
W komórkach nowotworowych onkogeny są często zmutowane, wzmocnione przez amplifikację lub ulegają ekspresji na wysokim poziomie. Aktywowane onkogeny mogą zakłócać mechanizmy kontrolujące śmierć komórki — większość normalnych komórek ulega zaprogramowanej formie śmierci (apoptozie). Dzięki onkogenom komórki, które powinny zginąć, przeżywają i zamiast tego się rozmnażają. Jednak w praktyce większość onkogenów wymaga dodatkowych zmian, takich jak mutacje w genach supresorowych czy czynniki środowiskowe (np. infekcja wirusowa), aby doprowadzić do pełnoobjawowego raka. Ten wieloetapowy model karcynogenezy tłumaczy, dlaczego jedna zmiana genetyczna rzadko wystarcza do transformacji nowotworowej.
Mechanizmy aktywacji onkogenów
- Mutacje punktowe — zmiana pojedynczych nukleotydów może prowadzić do stałej aktywacji białka (np. mutacje w RAS lub BRAF).
- Amplifikacja genów — zwiększenie liczby kopii genu powoduje nadprodukcję onkogennych białek (np. MYC, ERBB2/HER2).
- Translokacje chromosomalne — reasocjacja fragmentów chromosomów może tworzyć fuzje genowe z właściwościami onkogennymi (np. fuzja BCR-ABL w białaczce).
- Wstawienie wirusowe — integracja materiału wirusowego w pobliżu proto-onkogenu może zwiększyć jego ekspresję (przykłady w onkogenicznych wirusach ludzkich).
- Nadmierna ekspresja — zaburzenia regulacji transkrypcji lub stabilności mRNA/proteiny prowadzą do zbyt dużej ilości aktywnego białka.
Przykłady onkogenów i ich rola
Wiele onkogenów zostało zidentyfikowanych i przypisanych do konkretnych nowotworów. Ważne przykłady obejmują:
- RAS (np. KRAS) — często zmutowany w raku trzustki, płuca i jelita; mutacja utrzymuje białko w stanie stale aktywnym, pobudzając sygnalizację proliferacyjną.
- MYC — proto-onkogen o roli w regulacji transkrypcji i cyklu komórkowego; amplifikacje/amplifikacje występują w wielu nowotworach.
- BCR-ABL — fuzja powstająca na skutek translokacji (Philadelphia chromosome) w przewlekłej białaczce szpikowej; aktywuje kinazę tyrozynową.
- ERBB2/HER2 — nadekspresja lub amplifikacja w niektórych nowotworach piersi i żołądka; powoduje nadmierną sygnalizację wzrostu.
- BRAF (np. V600E) — mutacja aktywująca kinazę w szlaku MAPK często występuje w czerniaku i innych nowotworach.
Rola onkogenów w diagnostyce i prognozowaniu
Wykrycie określonych onkogenów lub ich mutacji ma wartość zarówno diagnostyczną, jak i prognostyczną oraz predykcyjną (określa odpowiedź na leczenie). Typowe metody wykrywania to sekwencjonowanie DNA/RNA, FISH (hybrydyzacja in situ), IHC (immunohistochemia) oraz PCR. Wynik badania molekularnego może wskazywać na agresywność nowotworu, ryzyko nawrotu oraz największe szanse skuteczności określonej terapii celowanej.
Onkogeny jako cele terapii
Wiele nowoczesnych leków przeciwnowotworowych celuje w białka kodowane przez onkogeny lub w szlaki, które one aktywują. Przykłady terapii celowanych:
- Inhibitory kinaz tyrozynowych — np. imatinib (blokuje BCR-ABL), crizotinib i kolejne generacje inhibitorów ALK, inhibitory EGFR (gefitynib, erlotynib, osimertynib).
- Monoklonalne przeciwciała — np. trastuzumab (celuje w HER2/ERBB2), cetuximab (EGFR).
- Inhibitory specyficznych mutacji — np. inhibitory BRAF (vemurafenib, dabrafenib) stosowane przy mutacji BRAF V600E.
Terapie celowane często przynoszą znaczną poprawę przeżycia i jakości życia pacjentów, zwłaszcza gdy terapia jest dobrana do obecnego u chorego profilu molekularnego guza.
Opór na terapię i wyzwania
Nawet skuteczne terapie celowane napotykają problem nabywania oporności. Mechanizmy oporności obejmują powstawanie wtórnych mutacji w docelowym genie, aktywację alternatywnych szlaków sygnałowych, amplifikacje innych onkogenów oraz zmiany fenotypowe komórek nowotworowych. Z tego powodu stosuje się strategie łączenia leków, sekwencjonowania terapii oraz monitorowania zmian molekularnych podczas leczenia.
Historyczne odkrycie i znaczenie naukowe
W 1976 r. J. Michael Bishop i Harold E. Varmus z Uniwersytetu Kalifornijskiego w San Francisco wykazali, że onkogeny są aktywowanymi proto-onkogenami, występującymi w wielu organizmach, w tym u ludzi. Za to odkrycie Bishop i Varmus otrzymali w 1989 roku Nagrodę Nobla w dziedzinie fizjologii lub medycyny. Ich prace położyły podwaliny pod zrozumienie genetycznych podstaw raka i umożliwiły rozwój terapii celowanych.
Podsumowanie
Onkogeny to kluczowy element molekularnej patologii nowotworów — są to aktywowane formy normalnych genów regulujących wzrost i przeżycie komórek. Ich aktywacja może nastąpić przez różne mechanizmy (mutacje, amplifikacje, translokacje, wirusowe insercje), a rozpoznanie konkretnego onkogenu w guzie ma bezpośrednie implikacje diagnostyczne, prognostyczne i terapeutyczne. Postęp w badaniach nad onkogenami przyczynił się do opracowania skutecznych terapii celowanych, choć wyzwaniem pozostaje oporność i heterogeniczność nowotworów.