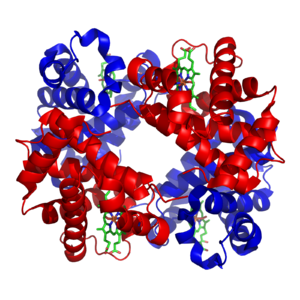
Białka kuliste są powszechnym rodzajem białka.
Są one jednym z trzech rodzajów białka. Pozostałe są białkami włóknistymi i błonowymi.
Ich struktura jest wynikiem fałdowania białka. Wykonane są one z łańcuchów polipeptydowych złożonych w zwarty kształt kuli.
Rozpuszczają się w wodzie z powodu hydrofilowych ("kochających wodę") łańcuchów bocznych, które wystają z zewnątrz cząsteczek. Odgrywają one ważną rolę w reakcjach metabolicznych.
W przeciwieństwie do białek, które pełnią jedynie funkcję strukturalną, białka kuliste mogą działać jak:
- Enzymy, poprzez katalizowanie reakcji organicznych zachodzących w organizmie w łagodnych warunkach i z dużą specyficznością. Różne esterazy spełniają tę rolę.
- Posłańcy, poprzez nadawanie komunikatów regulujących procesy biologiczne. Funkcja ta jest wykonywana przez hormony, tj. insulinę itp.
- Transportery innych molekuł przez membrany
- Zapasy aminokwasów.
- Regulacja innych molekuł odbywa się również za pomocą białek sferycznych, a nie białek włóknistych.
- Białka strukturalne, np. aktyna i tubulina, które są kuliste i rozpuszczalne jako monomery, ale polimeryzują tworząc długie, sztywne włókna.
Białka kuliste obejmują mioglobinę i hemoglobinę.
Budowa i właściwości
Białka kuliste mają złożoną strukturę trzeciorzędową (i często czwartorzędową), wynikającą z oddziaływań między resztami aminokwasów: wiązań wodorowych, oddziaływań jonowych, oddziaływań hydrofobowych oraz sił van der Waalsa. Często obecne są mostki dwusiarczkowe, które stabilizują strukturę. Wnętrze cząsteczki jest zwykle hydrofobowe, a powierzchnia — hydrofilowa, co tłumaczy ich rozpuszczalność w wodzie i obecność miejsc wiążących ligandy, kofaktory lub substraty enzymatyczne.
Wiele białek globularnych ma domeny funkcyjne — odrębne fragmenty sekwencji i struktury odpowiedzialne za konkretną funkcję (np. domena katalityczna enzymu, domena wiążąca DNA). Niektóre białka są również modyfikowane kowalencyjnie (np. glikozylacja, fosforylacja), co zmienia ich właściwości fizykochemiczne i aktywność.
Funkcje białek kulistych
Białka kuliste pełnią bardzo różnorodne role biologiczne, m.in.:
- Kataliza — jako enzymy przyspieszają reakcje biochemiczne, obniżając energię aktywacji i wykazując wysoką specyficzność wobec substratów.
- Przekazywanie sygnałów — hormony białkowe (np. insulina) i czynniki wzrostu przekazują informacje między komórkami i tkankami.
- Transport — białka transportowe przenoszą małe molekuły i jony przez krew (np. albumina transportuje fatty acids) lub przez błony komórkowe (kanały i przenośniki).
- Magazynowanie — niektóre białka magazynują aminokwasy lub gazy (np. mioglobina magazynuje tlen w mięśniach).
- Obrona immunologiczna — przeciwciała (immunoglobuliny) są białkami globularnymi, które rozpoznają i neutralizują antygeny.
- Ruch i motoryka — białka motorowe (np. miozyna, kinezyna) generują siłę i ruch w komórce.
- Regulacja — białka regulatorowe kontrolują aktywność enzymów, ekspresję genów i inne procesy komórkowe.
- Struktura dynamiczna — białka takie jak aktyna i tubulina występują jako rozpuszczalne monomery, które polimeryzują tworząc struktury cytoszkieletu; dzięki temu łączą cechy globularne i strukturalne.
Rodzaje i przykłady
Do białek kulistych należą m.in. enzymy trawienne (amylaza, lipaza), enzymy metaboliczne (dehydrogenazy, kinazy), hormony peptydowe (np. insulina — jak już wspomniano), białka transportowe (mioglobina, hemoglobina), albuminy, immunoglobuliny oraz białka regulatorowe. Wiele enzymów i receptorów błonowych ma dużą część globularną wystającą poza błonę, co umożliwia wiązanie ligandów.
Stabilność, denaturacja i utrata funkcji
Białka kuliste są wrażliwe na warunki środowiska: temperaturę, pH, stężenie soli, obecność detergentów lub czynników redukujących. Zmiany te mogą prowadzić do denaturacji — utraty natywnej struktury i funkcji. W niektórych przypadkach denaturację można odwrócić (refolding), ale często agregacja i tworzenie nierozpuszczalnych kompleksów uniemożliwiają powrót do funkcjonalnego stanu.
Znaczenie w medycynie i biotechnologii
Białka kuliste są kluczowymi celami terapeutycznymi (enzymy, receptory, hormony) oraz surowcami biotechnologicznymi (rekombinowane białka terapeutyczne, przeciwciała monoklonalne). Mutacje prowadzące do nieprawidłowego fałdowania białek są przyczyną wielu chorób (np. choroby prionowe, niektóre postacie choroby Alzheimera). Diagnostyka laboratoryjna często wykorzystuje pomiar stężeń specyficznych białek (np. markerów zapalenia, enzymów w surowicy).
Podsumowanie
Białka kuliste to rozpuszczalne, zazwyczaj sferyczne białka o złożonej strukturze i bardzo szerokim spektrum funkcji — od katalizy reakcji, przez transport i magazynowanie, aż po regulację i obronę immunologiczną. Ich struktura i aktywność zależą ściśle od prawidłowego fałdowania i warunków środowiskowych.