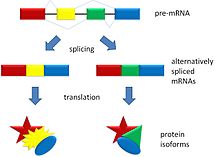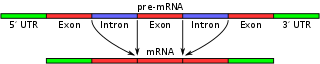
Alternatywne łączenie (ang. alternative splicing) to proces, dzięki któremu jeden gen może dawać początek wielu różnym formom mRNA, a w efekcie — różnym białkom (izoforom). Polega on na różnym łączeniu egzonów RNA posłańca podczas procesowania pre-mRNA, co prowadzi do powstawania różnych, dojrzałych wariantów mRNA z tej samej transkrypcji. W efekcie pojedynczy gen może kodować wiele białek o odmiennych właściwościach funkcjonalnych lub lokalizacjach w komórce.
Mechanizm
Proces splatania jest przeprowadzany przez kompleks zwany spliceosomem, złożony z małych nukleoproteinowych cząsteczek snRNP (m.in. U1, U2, U4/U6, U5) oraz licznych białek pomocniczych. Kluczowe elementy rozpoznawane przez spliceosom to miejsca 5' i 3' splicingowe oraz punkt odgałęzienia (branch point). W skrócie: U1 rozpoznaje 5' koniec intronu, U2 wiąże się z punktem odgałęzienia, a dalsze składniki przeprowadzają cięcia i połączenia, usuwając introny i łącząc egzony.
Rodzaje alternatywnego łączenia
Najczęściej obserwowane mechanizmy to:
- Przeskakiwanie egzonu (exon skipping) — egzon może być włączony lub pominięty w gotowym mRNA.
- Wybór alternatywnych miejsc 5' (alternative 5' splice site) — użycie różnych miejsc splicingowych na początku intronu.
- Wybór alternatywnych miejsc 3' (alternative 3' splice site) — użycie różnych miejsc na końcu intronu.
- Wzajemnie wykluczające się egzony (mutually exclusive exons) — z dwóch egzemplarzy wybierany jest jeden.
- Zatrzymanie intronu (intron retention) — intron pozostaje w mRNA i może wpływać na kodowanie białka.
Regulacja
Alternatywne łączenie jest kontrolowane przez kombinację elementów cis i trans:
- Elementy cis w obrębie pre-mRNA: motywy takie jak ESE (exonic splicing enhancers), ESS (exonic splicing silencers), ISE i ISS.
- Białka regulatorowe (trans): SR (seryna/arginina‑bogate) promujące użycie miejsc splicingowych oraz hnRNP działające często jako represory. Działanie tych czynników może być modyfikowane przez sygnały komórkowe (np. fosforylacje).
Znaczenie biologiczne
Alternatywne łączenie znacząco zwiększa różnorodność proteomu bez konieczności zwiększania liczby genów. U eukariontów, a szczególnie u ludzi, jest to powszechne — szacuje się, że ~95% genów z wieloma egzonami wykazuje alternatywne łączenie. Dzięki temu różne tkanki, etapy rozwoju czy stany fizjologiczne mogą wykorzystać odmienne izoformy białek o specyficznych funkcjach, lokalizacji lub stabilności.
Konsekwencje dla chorób i terapii
Zmiany w prawidłowym splataniu mogą prowadzić do chorób:
- Wiele zaburzeń genetycznych wynika z mutacji wpływających na miejsca splicingowe lub elementy regulatorowe (np. niektóre przypadki hemoglobinopatii, β‑talasemii czy mutacje w genie CFTR).
- Przykład kliniczny: w rdzeniowym zaniku mięśni (SMA) różnice w splataniu genu SMN2 prowadzą do pominięcia egzonu 7 — nowoczesne terapie (np. nusinersen/Spinraza) wykorzystują antysensowne oligonukleotydy do modyfikacji splatania i zwiększenia produkcji funkcjonalnego białka SMN.
- W nowotworach często obserwuje się aberracje splicingowe, które mogą promować proliferację, migrację lub unikanie odporności.
Dzięki zrozumieniu mechanizmów alternatywnego łączenia powstały strategie terapeutyczne: antysensowne oligonukleotydy wymuszające określony wzorzec splatania (np. w SMA, dystrofii mięśniowej Duchenne'a) oraz małe cząsteczki modulujące czynniki splicingowe.
Kontrola jakości
Nieprawidłowe produkty splatania są często wykrywane i eliminowane przez mechanizmy kontroli jakości, głównie przez ścieżkę nonsense‑mediated decay (NMD), która degraduje mRNA zawierające przedwczesne kodony stop. Dzięki temu komórka ogranicza produkcję nieprawidłowych lub potencjalnie szkodliwych białek.
Badania i techniki wykrywania
Obecnie zmiany w alternatywnym splicingu są intensywnie badane z użyciem technik wysokoprzepustowych, zwłaszcza RNA‑seq, które pozwala wykrywać i ilościowo oceniać izoformy mRNA w różnych tkankach i stanach. Analizy bioinformatyczne pomagają mapować miejsca splicingowe i przewidywać skutki mutacji.
Podsumowanie
Alternatywne łączenie to kluczowy mechanizm regulacji ekspresji i różnicowania białek w komórkach eukariotycznych. Dzięki niemu genom osiąga znacznie większą funkcjonalną złożoność. Jednocześnie jego zaburzenia są istotnym źródłem chorób, co czyni splicing atrakcyjnym celem diagnostycznym i terapeutycznym.