Telomeraza: definicja, funkcje i znaczenie w starzeniu oraz raku
Telomeraza — definicja, mechanizm i funkcje; rola telomerów w starzeniu i raku. Poznaj znaczenie enzymu dla zdrowia, długości życia i terapii przeciwnowotworowej.
Telomeraza to rybonukleoproteina — enzym zbudowany z podjednostki białkowej i matrycowego RNA. Dodaje powtarzalne sekwencje DNA na końcach nici DNA w regionach zwanych telomerami. W tekście cytowano typową powtarzalną sekwencję u kręgowców jako "TTAGG", którą telomeraza wykorzystuje (w praktyce sekwencja u wielu kręgowców, w tym u ludzi, występuje w formie powtórzenia hexanukleotydu). Dzięki swojej matrycowej RNA enzym kopiuje tę krótką sekwencję na końcu chromosomu, przeciwdziałając jego skracaniu.
Budowa i mechanizm działania
Telomeraza to holoenzym złożony z:
- podjednostki białkowej o aktywności odwrotnej transkryptazy (u ludzi nazywana TERT),
- matrycowego RNA (często określanego jako TERC lub RNA telomerazy),
- oraz białek pomocniczych (np. elementy kompleksu shelterin i białka takie jak dyskeryna), które stabilizują kompleks i kierują go do końców chromosomów.
Funkcja telomerów i telomerazy
Telomery działają jako buforowe regiony niekodującego DNA na końcach chromosomów eukariotycznych. Ich główna rola to:
- zapobieganie utracie istotnych sekwencji genowych podczas każdego cyklu replikacji — podczas kopiowania chromosomu tracimy zwykle kilkadziesiąt nukleotydów z końca, co bez telomerów prowadziłoby do postępującej utraty informacji;
- ochrona końców chromosomów przed łączeniem się ze sobą i przed aktywacją mechanizmów naprawczych, które traktowałyby je jako pęknięcia dwuniciowe.
Telomeraza a starzenie się
Już w 1973 roku radziecki biolog Aleksy Olovnikov zaproponował istnienie mechanizmu kompensującego skracanie telomerów oraz hipotezę łączącą skracanie telomerów ze starzeniem się. W komórkach somatycznych większość typów komórek ma niską aktywność telomerazy lub jej brak, co powoduje stopniowe skracanie telomerów po kolejnych podziałach. Kiedy telomery osiągają krytycznie krótką długość, komórka może wejść w stan:
- senescencji (stałego zatrzymania cyklu komórkowego),
- apoptozy (zaplanowanej śmierci komórki),
- lub—jeśli mechanizmy kontrolne są zaburzone—może dojść do niestabilności genomu.
Telomeraza i rak
Wiele nowotworów wykorzystuje telomerazę do uzyskania nieograniczonej zdolności do podziałów. U około 85–90% guzów obserwuje się rektywację lub aktywację telomerazy, co zapobiega skracaniu telomerów i pozwala komórkom rakowym proliferować niemal bez ograniczeń. Inne nowotwory mogą korzystać z mechanizmu zwanego ALT (Alternative Lengthening of Telomeres) — rekombinacyjnego wydłużania telomerów niezależnego od telomerazy (występuje u mniejszego odsetka nowotworów).
Skrócenie telomerów bez właściwej reaktywacji mechanizmów ochronnych prowadzi do niestabilności genomu, co z kolei może zwiększać ryzyko transformacji nowotworowej. Z drugiej strony nadmierna aktywność telomerazy sprzyja utrzymaniu klonu nowotworowego.
Gdzie występuje telomeraza i jak jest regulowana?
Telomeraza jest naturalnie aktywna w komórkach o dużym potencjale proliferacyjnym:
- komórki macierzyste (somatyczne i embrionalne),
- komórki zarodkowe i gamety,
- komórki układu odpornościowego o aktywności proliferacyjnej.
Znaczenie kliniczne i badania terapeutyczne
Ze względu na centralną rolę telomerazy w nowotworzeniu i starzeniu, ukierunkowanie na ten enzym jest przedmiotem intensywnych badań:
- inhibitory telomerazy — oligonukleotydy i inne związki (np. imetelstat) testowane są w leczeniu wybranych nowotworów i schorzeń mieloproliferacyjnych,
- terapie immunologiczne — szczepionki i terapie komórkowe skierowane przeciwko antygenom związanym z TERT,
- strategiczne hamowanie telomerazy jako sposób na ograniczenie nieograniczonej proliferacji komórek rakowych,
- próby aktywacji telomerazy w celu spowolnienia procesów starzenia lub leczenia chorób związanych z przedwczesnym skracaniem telomerów (np. dyskeratoza wrodzona) — podejścia te są jednak kontrowersyjne ze względu na ryzyko promowania transformacji nowotworowej.
Metody pomiaru i zastosowania diagnostyczne
W praktyce laboratoryjnej aktywność telomerazy i długość telomerów można oceniać różnymi metodami:
- TRAP (Telomeric Repeat Amplification Protocol) — test wykrywający aktywność telomerazy,
- pomiar długości telomerów technikami takimi jak Southern blot (meta-telomere), qPCR lub FISH (np. Q-FISH) — stosowane do badań naukowych i niektórych zastosowań klinicznych.
Historia odkrycia
Przewidywanie mechanizmu kompensującego skracanie telomerów wysunął Aleksy Olovnikov w 1973 roku, a sam enzym — telomeraza — został odkryty w 1984 roku przez Carol Greider i Elizabeth Blackburn w pierwotniaku Tetrahymena. Wraz z Jackiem Szostakiem Greider i Blackburn otrzymali w 2009 roku Nagrodę Nobla w dziedzinie fizjologii lub medycyny za wyjaśnienie mechanizmu utrzymania końców chromosomów.
Podsumowując, telomeraza jest kluczowym enzymem utrzymującym stabilność chromosomów i wpływającym zarówno na procesy starzenia, jak i na rozwój nowotworów. Zrozumienie jej działania i regulacji otwiera możliwości terapeutyczne, ale wymaga ostrożności ze względu na złożoność efektów biologicznych.
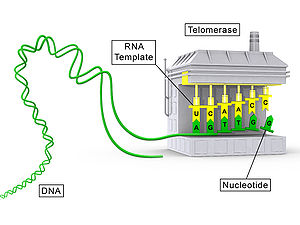
Schemat koncepcyjny przedstawiający składową białkową telomerazy (TERT) w kolorze szarym i składową RNA (TR) w kolorze żółtym
Pytania i odpowiedzi
P: Co to jest telomeraza?
O: Telomeraza to enzym białkowy RNA, który dodaje powtórzenia sekwencji DNA na końcu nici DNA w regionach telomerów.
P: Co to są telomery?
O: Telomery to jednorazowe bufory blokujące końce chromosomów eukariotycznych. Składają się z powtarzających się nukleotydów zawierających niekodujący DNA.
P: Jaka jest funkcja telomerów?
O: Funkcją telomerów jest unikanie utraty ważnego DNA z końców chromosomów poprzez kompensację 100-200 bezsensownych nukleotydów traconych podczas każdego cyklu replikacji.
P: Kto pierwszy przewidział mechanizm kompensacyjny dla skracania się telomerów?
O: Radziecki biolog Aleksiej Ołownikow w 1973 roku po raz pierwszy przewidział kompensacyjny mechanizm skracania telomerów.
P: Kto odkrył telomerazę?
O: Carol Greider i Elizabeth Blackburn odkryły telomerazę w 1984 r. w gliście Tetrahymena.
P: Za co Greider, Blackburn i Szostak otrzymali nagrodę?
O: Greider, Blackburn i Szostak otrzymali w 2009 roku Nagrodę Nobla w dziedzinie fizjologii lub medycyny za odkrycie telomerazy.
P: Jak działa telomeraza? O: Telomerazy przenoszą własną cząsteczkę RNA, która służy jako szablon do wydłużania skróconych telomerów po każdym cyklu replikacji.
Przeszukaj encyklopedię