Przegląd i definicja
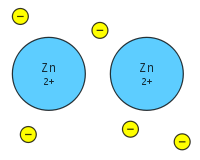
Wiązanie metaliczne to typ oddziaływania chemicznego występujący w metalach, który polega na wzajemnym przyciąganiu się dodatnio naładowanych jąder (jonów dodatnich) i zbioru zdelokalizowanych elektronów. Elektrony walencyjne nie są przypisane do pojedynczych atomów, lecz poruszają się swobodnie w całej sieci krystalicznej, tworząc tzw. „morze elektronów”. W efekcie atomy metalu zachowują się jak dodatnie centra, spajane przez ruchome ładunki ujemne. Ten model różni się od wiązań jonowych i kowalencyjnych, choć w pewnych sytuacjach obserwuje się cechy pośrednie.
Charakterystyka i mechanizm
Podstawą wiązania metalicznego jest pokrywanie się zewnętrznych orbitali atomowych: atomy oddają część swojej chmury elektronowej, a elektrony walencyjne tworzą wspólny zasób. Przenikanie orbitali i ich dyspergowanie w pasma energetyczne wyjaśnia przewodnictwo elektryczne i cieplne metali: swobodne elektrony mogą szybko przenosić ładunek i energię. W opisie teoretycznym używa się modeli klasycznych i kwantowych, od modelu Drude'a po teorię pasmową; kluczową rolę odgrywają tu orbitaly atomowe oraz gęstość stanów w pasmach energii.
Właściwości wynikające z wiązania metalicznego
Wspólny ruch elektronów i regularna sieć dodatnich jonów odpowiadają za zestaw cech przypisywanych metalom. Do najważniejszych należą:
- dobre przewodnictwo elektryczne i cieplne dzięki swobodnym elektronům;
- połysk metaliczny, czyli charakterystyczna odbijalność światła (połysk);
- ciągliwość i plastyczność (ciągliwość, plastyczność) – warstwy atomów mogą się przesuwać względem siebie bez łamania spoiwa, ponieważ elektrony nadal je spajają;
- wysoka wytrzymałość mechaniczną i często wysokie temperatury topnienia: siła wiązań metalicznych zależy od liczby elektronów walencyjnych i siły ich oddziaływania ze zjonizowanymi jądrami (wytrzymałość).
Historia koncepcji i rozwój teorii
Obraz „morza elektronów” był formułowany stopniowo wraz z rozwojem fizyki metali. W XIX i na początku XX wieku proponowano modele klasyczne tłumaczące przewodnictwo, a w XX wieku rozwinięto opis kwantowy: modele Drude'a i Sommerfelda oraz teoria pasmowa pozwoliły zrozumieć mechanizm zdelokalizacji elektronów oraz różnice między metalami, półprzewodnikami i izolatorami. Dziś teoria pasmowa oraz obliczenia pierwszych zasad (metody ab initio) służą do przewidywania własności nowych metali i stopów.
Przykłady, wyjątki i stopy
Typowe metale takie jak miedź, aluminium, żelazo czy złoto wykazują klasyczne wiązanie metaliczne i związane z nim cechy. Istnieją jednak wyjątki i niuanse: niektóre związki rtęci mogą tworzyć specyficzne wiązania jonów rtęci o charakterze bardziej kowalencyjnym, a niektóre niemetale, np. grafit, także przewodzą prąd dzięki zdelokalizowanym elektronům w płaskich warstwach. Stopy są mieszaninami metali, które zmieniają właściwości wyjściowe: dodatek niewielkiej ilości innego pierwiastka może zwiększyć twardość, odporność na korozję lub zmienić temperaturę topnienia. W praktyce przemysłowej wyróżnia się stopy zastępcze i wtrąceniowe, a mechanizmy ich działania opierają się na modyfikacji stopów sieci metalicznej.
Zastosowania i znaczenie
Zdolność przewodzenia prądu elektrycznego umożliwia szerokie zastosowanie metali w elektroenergetyce i elektronice (przewody, styki). Przewodnictwo cieplne i wytrzymałość sprawiają, że metale są materiałami konstrukcyjnymi w maszynach, budownictwie i transporcie. Ponadto właściwości powierzchniowe, jak połysk oraz zdolność do obróbki plastycznej, pozwalają na szerokie zastosowania dekoracyjne i użytkowe. Warto też pamiętać, że przenoszenie ładunku w przewodnikach odbywa się w postaci prądu z udziałem elektronów, a parametry wiązania są pochodną energii potrzebnej do oderwania elektronu, czyli energii jonizacji (energia jonizacji).
Podsumowując, wiązanie metaliczne to zjawisko kolektywne, którego zrozumienie łączy chemię i fizykę kwantową. Wyjaśnia ono fundamentalne właściwości metali i jest kluczowe dla projektowania nowych materiałów i stopów o pożądanych cechach.
Więcej informacji o poszczególnych aspektach można znaleźć w opracowaniach dotyczących struktury elektronowej, chemii metali oraz materiałoznawstwa; przydatne hasła związane z tematem obejmują: jon dodatni, prąd elektryczny, orbitaly atomowe i elektrony walencyjne.