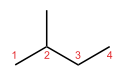Izomeryzm strukturalny (IUPAC nazywa to izomeryzmem konstytucyjnym) jest rodzajem izomerii. Dwa związki chemiczne w tym izomeryzmie mają ten sam wzór cząsteczkowy, ale cząsteczki połączyły się w różnej kolejności. Przeciwieństwem izomeryzmu strukturalnego jest stereoizomeryzm. Izomery konstytucyjne (strukturalne) różnią się rozmieszczeniem atomów i wiązań w obrębie cząsteczki, co prowadzi do istotnych różnic w właściwościach fizycznych i chemicznych.
Rodzaje izomerów konstytucyjnych
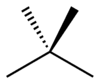
- Izomery szkieletowe (łańcuchowe) – różnią się strukturą łańcucha węglowego lub ogólnego szkieletu. Przykład: n-butanu (C4H10) i izobutanu (2-methylpropane) — mają ten sam wzór sumaryczny, ale inny układ atomów w łańcuchu.
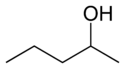
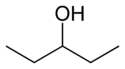
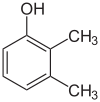
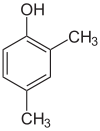
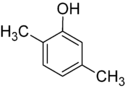
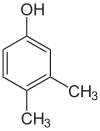
- Izomery pozycyjne (regioizomery) – atomy lub grupy funkcyjne są przyłączone w różnych pozycjach tego samego szkieletu. Przykłady: 1-propanol vs 2-propanol (oba C3H8O), lub położeniowe izomery dimetylobenzenu: orto-, meta- i para-ksyleny.
- Izomery funkcyjne – różne grupy funkcyjne, mimo tego samego wzoru sumarycznego. Klasyczny przykład: etanol (CH3CH2OH) i dimetylowy eter (CH3OCH3), oba o wzorze C2H6O, ale o innym typie wiązań i innych właściwościach.
- Tautomery – szczególny przypadek izomerii funkcyjnej, polegający na wzajemnej przemianie izomerów poprzez przesunięcie protonu (prototropia) i przesunięcie wiązań podwójnych. Najczęściej spotykana forma to keto–enol (np. enolizacja niektórych ketonów i β‑diketoni), a także formy tautomerowe w zasadach azotowych nukleotydów.
Przykłady i wyjaśnienia
- Izomery szkieletowe: C4H10 – n‑butan (łańcuch prosty) vs 2‑metylopropan (rozgałęziony). Różnice: temperatura wrzenia, gęstość, sposoby reakcji (np. produkty reakcji halogenowania).
- Izomery pozycyjne: 1‑buten vs 2‑buten – podwójne wiązanie położone w innym miejscu daje różne właściwości fizyczne i reaktivność. W aromatach: różne pozycje podstawników wpływają na zapach i aktywność biologiczną.
- Izomery funkcyjne: etanol vs dimetylowy eter (C2H6O) — eter jest związkiem lotnym i palnym o innym zapachu i innym punkcie wrzenia niż alkohol; etanol tworzy wiązania wodorowe, eter – w mniejszym stopniu.
- Tautomeria: przykład keto‑enol: acetoaceton (2,4‑pentandion) istnieje w formie keto i enol, które różnią się rozmieszczeniem wodoru i wiązań podwójnych; tautomery często współistnieją w równowadze i wpływają na reaktywność związku.
Różnice i konsekwencje
- Właściwości fizyczne: temperatury topnienia i wrzenia, rozpuszczalność, gęstość mogą się znacząco różnić między izomerami konstytucyjnymi.
- Reaktywność: różne rozmieszczenie grup funkcyjnych lub typu wiązań wpływa na mechanizmy reakcji i produkty (ważne w syntezie chemicznej).
- Nomenklatura i identyfikacja: różne izomery mają różne nazwy systematyczne według reguł IUPAC i różne wzory strukturalne.
Metody rozróżniania izomerów konstytucyjnych
- Spektroskopia NMR — pozwala ustalić łączność atomów (analiza przesunięć chemicznych i korelacji między protonami/węglami).
- IR (spektroskopia w podczerwieni) — różne grupy funkcyjne dają charakterystyczne pasma (np. OH, C=O, C–O), co pomaga rozróżnić izomery funkcyjne.
- Spektrometria mas — różnice w fragmentacji mogą wskazywać na różne układy strukturalne.
- Chromatografia (GC, HPLC) — izomery często separują się na kolumnie i dają osobne piki.
Znaczenie praktyczne
Izomery konstytucyjne mają duże znaczenie w chemii organicznej, syntezie leków, przemyśle petrochemicznym i materiałowym. Dwa izomery o takim samym wzorze sumarycznym mogą mieć zupełnie inne działanie biologiczne, toksyczność czy użyteczność technologiczna — dlatego ich rozpoznanie i kontrola są kluczowe w projektowaniu związków chemicznych.
Podsumowanie: izomery konstytucyjne to związki o tym samym wzorze sumarycznym, które różnią się sposobem połączenia atomów. Do podstawowych rodzajów należą izomery szkieletowe, pozycyjne i funkcyjne (w tym tautomery). Różnice te wpływają na właściwości i zastosowania związków oraz wymagają odpowiednich metod analitycznych do identyfikacji.