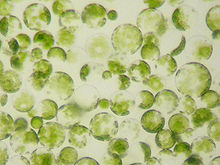
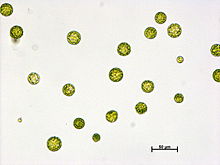
Protoplast we współczesnej biologii jest tym, co zostaje z komórki, gdy ściana komórkowa zostaje rozpuszczona. Pozostaje wtedy jądro komórkowe i otaczające je materiały protoplazmatyczne. W praktyce termin ten odnosi się do komórek roślinnych, grzybowych i niektórych bakterii, u których usunięto ścianę komórkową przy zachowaniu integralności błony plazmatycznej i podstawowych funkcji metabolicznych.
Definicja i zakres pojęcia
Protoplast to komórka roślinna, bakteryjna albo grzybowa, z której całkowicie albo częściowo usunięto ścianę komórkową sposobem mechaniczną albo enzymatyczną. W literaturze wyróżnia się też pojęcie sferoplastu – zwykle stosowane dla bakterii Gram-ujemnych, u których ściana komórkowa została tylko częściowo usunięta (pozostała część błony zewnętrznej).
Metody otrzymywania protoplastów
Proces izolacji protoplastów różni się w zależności od typu organizmu, ponieważ ściany komórkowe są zbudowane z różnych polisacharydów i białek. W związku z tym stosuje się różne enzymy i warunki:
- Enzymatyczne trawienie ściany komórkowej – najczęściej stosowane dla komórek roślinnych i grzybowych. Typowe enzymy to: cellulazy (trawią celulozę), pectinazy i preparaty komercyjne takie jak macerozyme czy driselase. Dla grzybów używa się też chitynazy i β-glukanaz.
- Metody chemiczne i enzymatyczno-chemiczne dla bakterii – do usuwania ściany peptydoglikanowej używa się m.in. lizozymu. W przypadku bakterii Gram-ujemnych często konieczne jest najpierw zastosowanie chelatorów (np. EDTA) lub innych czynników, które zaburzają błonę zewnętrzną, co prowadzi do powstania sferoplastów.
- Mechaniczne metody (rzadziej stosowane do otrzymywania żywych protoplastów) – obejmują delikatne rozcieranie tkanek, ultradźwięki lub wysokie ciśnienie; zwykle powodują większe uszkodzenia i niższą żywotność.
- Warunki osmotyczne – w każdym przypadku zabiegom towarzyszy użycie roztworów osmotycznie stabilizujących (np. mannitol, sorbitol, sacharoza) aby zapobiec lizie komórek pozbawionych ściany.
Procedura ogólna izolacji protoplastów
- Przygotowanie materiału wyjściowego (tkanki roślinnej, komórek w hodowli lub zawiesiny grzybowej).
- Inkubacja z mieszaniną enzymów w roztworze osmotycznym przy określonej temperaturze i czasie (zależne od gatunku i materiału).
- Selekcja i oczyszczanie protoplastów przez filtrację i/lub łagodną odwirowanie.
- Wielokrotne płukanie w buforach osmotycznych i ocena żywotności.
- Przygotowanie do dalszych zastosowań: fuzji, transformacji, hodowli w celu regeneracji ściany i całej rośliny lub badań biochemicznych.
Ocena jakości i żywotności protoplastów
Żywotność i jakość protoplastów ocenia się kilkoma metodami:
- Barwienia żywych i martwych komórek: fluoresceina diacetat (FDA) – sygnalizuje aktywność estraz (żywe komórki); błękit trypanu czy barwnik Evansa – przepuszczany przez uszkodzone błony (martwe komórki).
- Mikroskopia (światła i fluorescencyjna) – ocena kształtu, integracji błony i ewentualnej regeneracji ściany.
- Efektywność regeneracji i zdolność do tworzenia tkanek lub całych organizmów – szczególnie istotna w biotechnologii roślin.
Zastosowania w biologii i biotechnologii
Protoplasty są niezwykle przydatne w badaniach podstawowych i zastosowaniach praktycznych:
- Fuzja protoplastów – łączenie protoplastów różnych gatunków lub odmian w celu uzyskania somatycznych hybryd i cybridów (technika wykorzystywana do przenoszenia cech niemożliwych do uzyskania przez krzyżowanie płciowe).
- Transformacja genetyczna – wprowadzanie DNA metodami PEG-ochronnym, elektroporacji czy mikroiniekcji. Protoplasty ułatwiają transfer obcych genów i edycję genomu (np. CRISPR/Cas), ponieważ brak ściany zwiększa dostępność błony do manipulacji.
- Hodowla i regeneracja roślin – uzyskanie roślin z pojedynczych protoplastów wykorzystywane jest do klonowania, selekcji i tworzenia materiału roślinnego o pożądanych cechach.
- Badania biochemiczne i fizjologiczne – badanie transportu przez błonę, receptorów, metabolicznych szlaków komórkowych bez interferencji ściany komórkowej.
- Analizy molekularne na poziomie pojedynczych komórek – np. ekspresja białek znacznikowych (GFP) w układach transientnych, badania sygnalizacji komórkowej.
- Zastosowania w mikrobiologii – w obrębie bakterii i grzybów protoplasty/sferoplasty służą do badań nad syntezą ściany, do izolacji plazmidów, transformacji i badań nad odpornością na antybiotyki.
Regeneracja ściany komórkowej i ograniczenia
Po usunięciu ściany wiele protoplastów ma zdolność do jej regeneracji i powrotu do normalnego cyklu życiowego, co jest podstawą do regeneracji całych roślin z pojedynczych komórek. Jednak skuteczność regeneracji jest zależna od gatunku, etapu rozwojowego materiału i warunków hodowli — nie wszystkie gatunki są równie łatwe do odtworzenia. Główne ograniczenia techniczne to niska wydajność w niektórych gatunkach, podatność na zakażenia mikrobiologiczne, wrażliwość na warunki osmotyczne oraz utrata zdolności do dzielenia się po dłuższym czasie poza naturalną ścianą.
Praktyczne uwagi i bezpieczeństwo
- Praca z protoplastami wymaga sterylnych warunków i precyzyjnego doboru buforów osmotycznych; niewłaściwe warunki prowadzą do lizysu (pęknięcia) komórek.
- Do manipulacji genetycznych stosuje się procedury zapewniające zgodność z przepisami dotyczącymi GMO i bezpieczeństwa biologicznego.
- Dokładne dokumentowanie warunków enzymatycznych, stężeń osmootycznych i czasu inkubacji jest kluczowe dla powtarzalności wyników.
Podsumowując, protoplasty są cennym narzędziem badawczym — pozwalają na bezpośredni dostęp do błony i cytoplazmy komórkowej, ułatwiają manipulacje genetyczne i fuzję komórek, a także dostarczają informacji o biochemii i fizjologii komórek bez wpływu ściany komórkowej. Wybór metod i warunków izolacji zależy od budowy ściany danego organizmu i celu badania.